Тепловые характеристики продуктов сгорания
Энтальпией продуктов сгорания называют количество теплоты, которое содержится при постоянном давлении в газах, образовавшихся от сгорания 1 кг (1 м3) топлива, при нагревании их от 0 °С до температуры tг.
В случае адиабатического горения, когда вся теплота, выделяющаяся при сжигании 1 кг (1 м3) топлива, без потерь целиком переходит в продукты сгорания, последние имеют максимально возможную (теоретическую) энтальпию Hг . Энтальпия продуктов горения Hг, МДж/кг (МДж/м3), в общем виде запишется
. Энтальпия продуктов горения Hг, МДж/кг (МДж/м3), в общем виде запишется
Hг = tг ∑ υi сi , (29)
а в развернутом виде
Hг = (υсо ссо
ссо + υsо
+ υsо сsо
сsо + υN
+ υN сN
сN + υо
+ υо со
со +
+
+ υн осн
осн о+
о+ 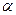 ун сзл Ар/100) tг , (30)
ун сзл Ар/100) tг , (30)
где υсо , υsо
, υsо , υN
, υN и т. д. – объемы соответствующих газов в продуктах сгорания, м3/кг (м3/м3); ссо
и т. д. – объемы соответствующих газов в продуктах сгорания, м3/кг (м3/м3); ссо , сsо
, сsо , сN
, сN и т. д. – средние в интервале температур от 0 до tг объемные теплоемкости соответствующих газов, МДж/(м3·К);
и т. д. – средние в интервале температур от 0 до tг объемные теплоемкости соответствующих газов, МДж/(м3·К); 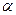 ун – доля золы топлива, уносимая продуктами сгорания; сзл – теплоемкость золы при tг, МДж/(кг·К).
ун – доля золы топлива, уносимая продуктами сгорания; сзл – теплоемкость золы при tг, МДж/(кг·К).
Энтальпию продуктов полного сгорания можно представить также в виде
Hг = Н°г + (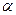 -1) H°ок + Hз , (31)
-1) H°ок + Hз , (31)
где H°г – энтальпия теоретического количества продуктов сгорания (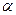 =1) при расчетной температуре tг , МДж/кг (МДж/м3); определяется по теоретическому выходу продуктов сгорания
=1) при расчетной температуре tг , МДж/кг (МДж/м3); определяется по теоретическому выходу продуктов сгорания
H°г = (υRO сRO
сRO + υ°N
+ υ°N сN
сN + υ°H
+ υ°H O cH
O cH O) tг ; (32)
O) tг ; (32)
где (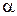 -1) H°ок – энтальпия избыточного, сверх теоретически необходимого количества окислителя;
-1) H°ок – энтальпия избыточного, сверх теоретически необходимого количества окислителя;
H°ок = H°сух.ок + H°Н О , (33)
О , (33)
где H°сух.ок – энтальпия теоретического объема сухого окислителя;
H°Н О – энтальпия водяных паров, содержащихся в окислителе.
О – энтальпия водяных паров, содержащихся в окислителе.
Энтальпия золы в уносе, МДж/кг,
Hзл = 0,01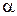 ун сзл Ар (34)
ун сзл Ар (34)
подсчитывается только в том случае, если
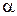 ун Ар · 103/ Qнр > 1,4. (35)
ун Ар · 103/ Qнр > 1,4. (35)