Из первого закона термодинамики
δQ = δL = p dV
Адиабатный процесс –это процесс без теплообмена с окружающей средой. (δQ = 0)
Из первого закона термодинамики:
δQ = m cv dT + p dV = 0 или m cv dT = - p dV
δQ = m cp dT – V dp = 0 или m cp dT = V dp
Разделим второе уравнение на первое: 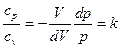 , где k – коэффициент Пуассона. Разделяя переменные и интегрируя в пределах от V1 до V2 и от p1 до p2, получим
, где k – коэффициент Пуассона. Разделяя переменные и интегрируя в пределах от V1 до V2 и от p1 до p2, получим
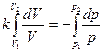 или
или 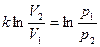
Вводя коэффициент k под знак логарифма, и приравнивая аргументы логарифмической функции, запишем:
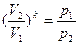 или p1 V1k = p2 V2k.
или p1 V1k = p2 V2k.
Последнее выражение представляет собой уравнение адиабаты:
p Vk = const (40)
Уравнение адиабаты представляет собой уравнение политропы с показателем политропы n = k. Поэтому коэффициент Пуассона k называют также показателем адиабаты. Работа в адиабатном процессе совершается за счет уменьшения внутренней энергии термодинамической системы. Теплоемкость адиабатного процесса равна нулю, так как δQ = 0.