рефераты конспекты курсовые дипломные лекции шпоры
- Раздел Философия
- /
- Вплив швидкості потоку і тиску газу-носія на ефективність розділення.
Реферат Курсовая Конспект
Вплив швидкості потоку і тиску газу-носія на ефективність розділення.
Вплив швидкості потоку і тиску газу-носія на ефективність розділення. - раздел Философия, Тема 1. Введення в фізико-хімічні методи аналізу З Раніше Виведених Залежностей (Ван Деємтер Запропонував Рівняння, Яке Пов'яз...
З раніше виведених залежностей (ван Деємтер запропонував рівняння, яке пов'язує BETT (H) з лінійною швидкістю (U) потоку рухомої фази: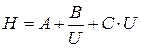 ) відомо, що ефективність колонки має складну залежність від швидкості потоку газу-носія, і що існує оптимальна швидкість, яка відповідає мінімальному значенню Н – ВЕТТ. Тому для успішного проведення експерименту з розділення суміші речовин необхідно вибрати швидкість потоку, яка відповідає мінімуму значення Н. Оптимальна швидкість газу-носія встановлюється експериментально.
) відомо, що ефективність колонки має складну залежність від швидкості потоку газу-носія, і що існує оптимальна швидкість, яка відповідає мінімальному значенню Н – ВЕТТ. Тому для успішного проведення експерименту з розділення суміші речовин необхідно вибрати швидкість потоку, яка відповідає мінімуму значення Н. Оптимальна швидкість газу-носія встановлюється експериментально.
Звичайний хроматографічний дослід проводиться при середньому тиску, який трохи перевищує атмосферний (760 мм рт. ст. або 101 кПа). Підвищення тиску приводить до зменшення Н, і відповідно, сприяє покращенню ефективності колонки. Підвищення тиску викликає додатковий ефект, зв’язаний з міжмолекулярною взаємодією речовин суміші з газом-носієм, і газ-носій не тільки переносить речовину, а й впливає на коефіцієнт Генрі і величину об’єму утримання. Підвищуючи тиск, можна підібрати такі умови досліду, які збільшать селективність нерухомої фази за рахунок зміни коефіцієнта Генрі. Застосування вакууму також сприяє в певних умовах кращому розділенню суміші речовин. Тому можливість зміни тиску газу-носія в широких межах, від вакууму до тиску в декілька сотень і навіть тисяч атмосфер, дозволяє вибрати оптимальні умови проведення досліду.
2.2. Селективність і тривалість розділення у газовій хроматографії. Як уже зазначалось, впливом рухомої фази на селективність розділення речовин, тобто на значення характеристик утримування, у газовій хроматографії можна нехтувати. Впливати на селективність можна:
· добором селективного сорбенту,
· для певної колонки зміною її температури під час аналізу, тобто застосуванням режиму програмування температури.
Тривалість розділення речовин (значення часів утримування) у газовій хроматографії залежить від:
· площі поверхні сорбенту. Відомо, що адсорбція тим більша, чим більша площа поверхні сорбенту. Отже, зменшивши площу поверхні, можна зменшити адсорбцію на вузькій ділянці нерухомої фази. Це призведе до прискорення проходження компонента суміші крізь сорбент, а отже до скорочення тривалості аналізу.
· температури. З підвищенням температури адсорбція зменшується. При цьому зменшується коефіцієнт розподілу речовини і виправлений час утримування. Отже, зменшити утримувані об'єми речовин, які сильно адсорбуються, можна підвищенням температури колонки або /і зменшенням питомої поверхні сорбенту.
2.3. Хроматографія з програмуванням температури.
Температура – один з основних факторів у газовій хроматографії, який визначає тривалість розділення, селективність колонки, розмиття смуг. Для речовин із близькою полярністю послідовність елюювання корелює з їхніми температурами кипіння.
Кожна пара речовин добре розділяється за деякої певної температури. Суміш речовин, які киплять у широкому діапазоні температур, розділити за сталої температури колонки складно, а часом неможливо. Наприклад, за низьких температур добре розділяються легкі компоненти, однак час елюювання сполук гомологічного ряду експоненціально зростає і загальна тривалість аналізу стає значною. В міру підвищення температури, коли важкі компоненти елюються відносно швидко, розділення легких компонентів погіршується. Легкі компоненти можуть взагалі не розділитися. Цей недолік можна усунути зміною сорбційної ємності в ході розділення за допомогою підвищення температури колонки за заданим законом.
Температура суттєво впливає як на коефіцієнт Генрі, відповідно на селективність сорбента, так і на коефіцієнт дифузії. З підвищенням температури зростає швидкість дифузійних процесів, які, залежно від визначальних стадій, можуть як збільшувати, так і зменшувати ефективність колонки. Зниження температури збільшує сорбційні здатності компонентів, тобто степінь розділення, але також збільшує тривалість аналізу. Тому оптимальна температура вибирається експериментально для кожної суміші компонентів, і повинна забезпечувати відсутність конденсації пари всіх компонентів та необхідне значення критерію розділення.
Хроматографічне розділення у більшості випадків проводиться в ізотермічному режимі – при постійній температурі впродовж всього досліду і по всій довжині колонки. В газових хроматографах для забезпечення ізотермічного процесу колонку поміщають в термостат.
У випадку аналізу сумішей, температури кипіння компонентів яких знаходяться в широкому діапазоні, найдоцільніше проводити розділення при поступовій зміні температури за певною програмою – у програмованому режимі.
Якщо процес починається при порівняно низьких температурах, то сорбованість більшості компонентів велика і швидкість їх хроматографічних зон в шарі сорбента мала. Із збільшенням температури внаслідок зменшення сорбованості і, відповідно, збільшення швидкості зон із колонки будуть виходити все більш важкі компоненти суміші.
Однак у хроматографії з програмуванням температури вибір нерухомих рідких фаз із необхідною термічною стійкістю є обмеженим через застосування високих температур.
3. Особливості газоадсорбційної хроматографії. Адсорбенти
У газоадсорбційній хроматографії нерухомою фазою є твердий адсорбент з великою питомою поверхнею (10-1000 м2/г), а рухомою – хімічно інертний газ-носій (азот, гелій, аргон, водень тощо).
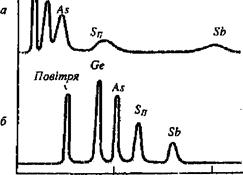
У газоадсорбційній хроматографії дуже ефективним є розділення речовин в умовах програмованої температури. Відомо, що з підвищенням температури повнота адсорбції зменшується, що впливає на час утримування in. У разі проведення розділення за сталої температури низькокиплячі сполуки елюються швидко, а висококиплячі затримуються в колонці довше, що призводить до розмивання їх кривих елюювання (рис. 16, а). Ця різниця швидкостей елюювання компонентів суміші значно зменшується, якщо в процесі розділення поступово підвищувати температуру колонки (рис. 16, б).
Ge
 0 5 10 tr
Рис. 16. Розділення гідридів елементів методом газової хроматографії на колонці з порапаком: за сталої температури колонки 85 0C (а) та за програмованої температури від 76 до 120 0C (8 ºС/хв) (б). Газ-носій – азот
0 5 10 tr
Рис. 16. Розділення гідридів елементів методом газової хроматографії на колонці з порапаком: за сталої температури колонки 85 0C (а) та за програмованої температури від 76 до 120 0C (8 ºС/хв) (б). Газ-носій – азот
|
Вид нерухомої фазивідіграє основну роль у розділенні компонентів суміші, оскільки від його властивостей залежить коефіцієнт селективності. Якщо він »0, то ніяким збільшенням ефективності колонки розділення не досягнути.
Адсорбенти (нерухома фаза) є тонкодисперсними неорганічними або органічними матеріалами з питомою поверхнею понад 50 м2/г. Грубодисперсні макропористі адсорбенти мають розміри гранул у межах 0,01-1,0 мм і питому площу поверхні 400-800 м2/г. Розміри гранул високодисперсних адсорбентів, наприклад аеросилів, виготовлених на основі кремнезему, коливаються у межах 0,1-1,0 мкм, їх питома поверхня – 100-700 м2/г.
Розрізняють зовнішню і внутрішню поверхні зерна адсорбенту, на яких відбувається адсорбція. У макропористих адсорбентах основна частка поверхні знаходиться всередині гранул. Швидкість адсорбції речовин на таких адсорбентах визначається в основному дифузією молекул у пори адсорбенту, і тому адсорбційна рівновага встановлюється повільно. Це призводить до розмивання кривих елюювання, тобто до зменшення ефективності розділення речовин.
Навпаки, на високодисперсних матеріалах адсорбція відбувається переважно на зовнішній поверхні мікрогранул, і тому адсорбційна рівновага встановлюється значно швидше. Внаслідок цього криві елюювання мають гостру форму, ефективність розділення підвищується. Саме високодисперсні адсорбенти використовують у сучасній високоефективній рідинній і газовій хроматографії, в якій необхідна швидкість потоку рухомої фази (елюенту) забезпечується підвищенням тиску в хроматографічній системі.
Адсорбенти мають виявляти такі основні властивості:
· хімічну інертність відносно компонентів суміші і рухомої фази;
· відсутність каталітичної активності;
· селективність;
· механічну стійкість;
· лінійність ізотерми адсорбції, що забезпечує сталість утримуваного об'єму за різних концентрацій адсорбату;
· доступність.
Адсорбенти різних типів виявляють неоднакову адсорбційну здатність (селективність) щодо різних хімічних сполук. Однак неможливо встановити однозначний кількісний зв'язок між хімічною будовою речовин та їх здатністю адсорбуватися на різних адсорбентах.
Загальноприйнятим є розподіл адсорбентів на дві групи – полярні (гідрофільні) та неполярні (гідрофобні) органічні й неорганічні. Полярні адсорбенти, такі як силікагель, оксид алюмінію, природні та штучні силікати тощо, виявляють селективність до полярних молекул, а неполярні – графітована сажа, активоване вугілля тощо – є селективними відносно неполярних молекул.
За геометричною структурою адсорбенти можна поділити на непористі з питомою поверхнею 0,01-100 м2/г (хлорид натрію, графітована сажа, аеросил) та пористі з різними розмірами пор і питомою поверхнею 100-1000 м2/г (ксерогелі, скло, активоване вугілля, цеоліти, тефлон).
Однією з важливих характеристик адсорбентів є адсорбційна ємність – кількість активних центрів на їх поверхні. Вона зумовлена способом виготовлення адсорбенту та його подальшої обробки. Адсорбенти стандартизують за адсорбційною активністю, на яку впливає вміст в них води. Зокрема, ступінь активності оксиду алюмінію (активність за Брокманом) виражають вмістом води у ньому, %: І – 0; IІ – 3; III – 6; ІV – 10; V – 15. Зростання активності сорбенту (збільшення вмісту в ньому води) зумовлює підвищення його сорбційної здатності до полярних адсорбатів. Неполярні краще адсорбуються на менш активних полярних адсорбентах, в яких вміст води менший або практично нульовий.
Полярні адсорбенти. В адсорбційній хроматографії найчастіше використовують такі полярні адсорбенти, як силікагель та оксид алюмінію. Останнім часом також широко застосовують адсорбенти, модифіковані ковалентно зв'язаними або адсорбованими на їх поверхні органічними аналітичними реагентами.
Силікагель (SіО2∙хН2О) – це сухий гель силіцієвої кислоти з аморфною структурою, гідрофільний сорбент з розвиненою пористою структурою. Отримують його в результаті конденсації ортосиліцієвої кислоти, яка утворюється внаслідок гідролізу її хлорангідриду або реакції розчинних силікатів із мінеральними кислотами.
На поверхні силікагелю є такі групи:
| силандіольна |
| силоксанова |
| силанольна |

Залежно від ступеня дегідроксилювання поверхні кремнезему співвідношення цих груп може помітно змінюватися. У гранично гідроксильованому кремнеземі на поверхні знаходяться 4,6-4,8 OH-груп/мм2. Наявність цих груп, що мають слабкокислотні властивості, та їх нерівномірне розміщення на поверхні зумовлюють неоднорідність властивостей поверхні адсорбенту.
Кислий гідратований силікагель (рН 3-5) називають також силіцієвою кислотою. Нейтральний силікагель використовують для розділення нейтральних сполук або сполук, які виявляють основні властивості, а для розділення сполук з кислотними властивостями застосовують силіцієву кислоту.
Нерухомі фази на основі силікагелю, особливо з модифікованою поверхнею, є найпоширенішими сорбентами у високоефективній рідинній і газовій хроматографії. Фірми, які випускають колонки для хроматографії, розробляють силікагель різноманітних марок, діаметр зерен яких варіює від 2 до 10 мкм, діаметр пор – від 3 до 75 нм, відповідно величина питомої поверхні – від 30 до 700 м2/г.
Силікагель є ефективним адсорбентом для розділення вуглеводневих компонентів нафти, карбонових кислот, естерів, ароматичних амінів, спиртів, фенолів, альдегідів, кетонів, амінокислот, пектинів, пестицидів та багатьох інших органічних речовин. Його використовують і для розділення неорганічних іонів, зокрема катіонів металів. Для цього ефективні також силікагелі, на поверхні яких іммобілізовані органічні реагенти, що містять певні функціонально-аналітичні угруповання (дитизон, оксихінолін, піридилазорезорцин, ксипеноловий оранжевий, арсеназо тощо). Максимальний вміст домішок у торгових препаратах силікагелю становить, (%): Fe (0,001-0,02); Al (0,05); Ті (0,05); Pb та інші важкі метали (0,001-0,004); Ca (0,01); Na (0,02); Сa (0,01-0,02); SO42- (0,003-0,005); водорозчинні речовини (до 0,2).
Недоліками силікагелю як сорбенту для хроматографії є: розчинність при рН менше 2 і більше 9; неоднорідність поверхневих силанольних груп, що призводить до викривлення форм піків; здатність швидко адсорбувати воду. Переваги силікагелю: можливість отримання зерен із фіксованим і відтворюваним діаметром пор; можливість хімічного модифікування; механічна стійкість до тиску 27,6 МПа; стійкість до широкого спектра органічних розчинників.
Оксид алюмінію, як і силікагель, є полярним адсорбентом. Крім того, він виявляє амфотерні властивості й може бути використаний як нейтральний, лужний або кислий адсорбент. Кислотність оксиду алюмінію визначають у його 10%-вій водній суспензії. рН водної суспензії нейтрального оксиду алюмінію знаходиться в межах 6,5-7,5, лужного – у межах 9,0-10,5, кислого – у межах 3,5-4,5. Лужний оксид алюмінію отримують обробкою Al2O3 розчином лугу, кислий – розчином нітратної кислоти з наступним відмиванням дистильованою водою від решток лугу чи кислоти.
Нейтральний оксид алюмінію використовують для хроматографічного розділення органічних речовин у неводних розчинах: вуглеводнів, альдегідів, кетонів, спиртів, фенолів, слабких органічних кислот та основ, етерів, барвників, вітамінів, алкалоїдів та ін. Лужний оксид алюмінію застосовують для розділення у водних та водно-органічних розчинах речовин, що виявляють основні властивості: аміни, аміди, основні амінокислоти, алкалоїди, інсектициди, основні барвники та ін. Кислий оксид алюмінію використовують для хроматографічного розділення речовин кислотного характеру: аліфатичних і ароматичних карбонових кислот, амінокислот, сульфокислот, кислотних барвників тощо. Лужний і кислий оксиди алюмінію виявляють також властивості відповідно катіоніту та аніоніту, їх застосовують для хроматографічного розділення катіонів та аніонів.
Максимальний вміст домішок в оксидах алюмінію різких марок становить, (%): SiO2 (0,01-0,25), Na2O (0,05-0,80), Fe2O3 (0,02-0,15), TiO2 (0,01), Сa (0,05-0,10), SO42- (0,2-0,5), втрата при прожарюванні (2).
Перевагою оксиду алюмінію порівняно із силікагелем є його стійкість у широкому діапазоні рН, недоліком – те, що всі спроби модифікувати оксид алюмінію призводять до утворення нестійких поверхневих сполук.
Кізельгур (целіт, діатомова земля) – це пористий матеріал, природного походження, утворений із скам'янілих діатомових водоростей. Матриця складається з mSiO∙nH2O та домішок оксидів алюмінію, феруму, кальцію, магнію.
Цеоліти (молекулярні сита) – синтетичні пористі адсорбенти, що складаються з атомів Al, Si, O та одно- або двовалентного металу. Оскільки цеоліти містять катіони, вони мають велику спорідненість до молекул, в яких електронна густина сконцентрована на периферії (молекули з π-зв'язками і вільними електронними парами). За своїми адсорбційними властивостями цеоліти значно відрізняються від інших адсорбентів. Завдяки однорідним розмірам пор вони адсорбують тільки ті молекули, розміри яких дають їм змогу проникати в ці пори. Цеоліти дуже гідрофільні. Сорбовані вода і вуглекислий газ змінюють утримувані об'єми, тому перед роботою їх треба видаляти.
Пористе скло. Натрієво-боросилікатне скло піддають термообробці при 500-700 °С, подрібнюють його у зерна, відсіюють фракцію 0,25-0,5 мм і обробляють 3M хлоридною кислотою при 50 0С. Скло відмивають від іонів хлору і висушують при 150-200 °С до сталої маси. За хімічною природою поверхні скло подібне до силікагелю. Його питома поверхня становить 30-100 м2/г.
У хроматографії використовують також інші адсорбенти, такі як оксиди й карбонати кальцію та магнію, тальк, крохмаль, природні адсорбенти – глини, мінерали тощо.
Неполярні адсорбенти. Як зазначалось, до неполярних адсорбентів належать графітована сажа, активоване вугілля та інші, які є неселективними до полярних молекул. Адсорбція на них відбувається за рахунок дисперсійних сил.
Графітовану сажу отримують обробкою звичайних саж при 3000 °С у вакуумі або інертному газі. Це непористі адсорбенти з питомою поверхнею 6-100 м2/г. Графітована сажа буває різних марок, залежно від розміру часточок і відповідно величини питомої поверхні. Плоска поверхня сажі вигідна для розділення просторових ізомерів. Через недостатню механічну стійкість до сажі потрібно додавати модифікатор, наприклад, високотемпературний силоксановий полімер.
Активоване вугілля – це пористий гідрофобний адсорбент, велика питома поверхня якого (400-1700 м2/г) зумовлює значні сили взаємодії з неполярними молекулами, що обмежує галузь використання немодифікованого вугілля аналізом легких газів. Адсорбент отримують висушуванням вугілля при 180 °С та прожарюванням його при 300 °С.
Тефлон (політетрафторетилен -(CF2-CF2)n – пористий синтетичний кристалічний полімер молекулярною масою 500000–2000000. Перевага тефлону порівняно з іншими органічними полімерами – висока термічна стійкість – до 300 °С. Питома поверхня його – до 10 м2/г.
Полістирол – пористий синтетичний органічний адсорбент з питомою поверхнею до 100 м/г. Фірмові назви адсорбентів на основі стиролу і дивінілбензолу – порапак, хромосорб, полісорб (різняться за пористістю).
Пінополіуретани – це пластичні матеріали, в яких частина твердої фази - поліуретану – заміщена газом у вигляді безлічі маленьких комірок. Ці матеріали добре адсорбують органічні аналітичні реагенти та їх комплексні сполуки з неорганічними й органічними лігандами. До їх складу входять уретанові угруповання та етерні (естерні) атоми кисню. За рН<3 відбувається протонізація етерних атомів кисню, внаслідок чого пінополіуретани набувають властивостей аніонообмінних сорбентів. Найширше пінополіуретани використовують як твердофазові сорбенти, модифіковані органічними або неорганічними реагентами.
Часто використовують модифікація адсорбентів:
1) обробка кислотами, лугами чи неорганічними речовинами –приводить до видалення домішок, в основному оксидів металів в силікагелях;
2) зв’язування гідроксильних груп хлорсиланами чи іншими речовинами – заміна активних груп поверхні адсорбентів на неактивні, наприклад, гідроксильних на метильні при силанізації силікагеля;
3) насичення парою води – дезактивація адсорбентів, як і нанесення нелетких органічних речовин;
4) геометрична модифікація – прокалювання при 900-1000 ºС. Це змінює структуру пор внаслідок спікання - залишаються тільки великі пори, що сприяє зменшенню розмивання хроматографічних зон і збільшенню швидкості аналізу.
Розглянуті вище адсорбенти застосовуються як в рідинній, так і в газовій хроматографії. Кожен з них дає змогу вирішити певні аналітичні задачі.
4. Особливості газорідинної хроматографії
В аналітичній практиці газорідинну хроматографію використовують значно частіше, ніж газоадсорбційну. Це зумовлено надзвичайно широким асортиментом рідких нерухомих фаз з урахуванням не тільки їх полярності, а й також хімічної природи. До того ж ізотерми сорбції при розділенні речовин у системі фаз "рідка-газова" є прямолінійними у ширшому інтервалі концентрацій, ніж у системі фаз "тверда - газова".
Для правильного вибору нерухомої фази в газорідинній хроматографії необхідно керуватися такими правилами:
1. Сили взаємодії компонентів з розчинником, який використовується в якості нерухомої фази, повинні діяти селективно, тобто вибірково. Важливе значення при виборі нерухомої фази мають полярність розчинника, здатність хімічно взаємодіяти з компонентами суміші чи утворювати водневі зв’язки і деякі інші.
2. Рідка фаза повинна бути малолеткою і не розкладатися при робочій температурі колонки.
3. Мають бути виключені необоротні реакції між речовиною рідкої фази і компонентами суміші, що аналізується, а також твердим носієм і газом-носієм.
Вибір рідкої фази в основному проводять емпірично, користуючись положеннями теорії розчинів та відомим літературними даними про фізико-хімічні властивості розчинника і речовин, що розчиняються. Якщо немає довідникових даних з абсорбційної здатності нерухомої фази, при її виборі користуються загальним принципом "подібне розчиняється у подібному". За цим правилом, для розділення суміші двох речовин необхідно вибрати нерухому фазу, яка схожа за хімічною природою і властивостями до одного з компонентів суміші. Наприклад, при розділенні таких різних за властивостями речовин як спирт і алкан, необхідно як нерухому фазу вибрати або речовину з функціональною групою – ОН, або алкан. В спирті спирт краще розчиняється, і відповідно, виходить останнім з хроматографічної колонки.
Рідкі нерухомі фази поділяють на три групи: неполярні (насичені вуглеводні), слабополярні (естери, нітрили тощо) і полярні (полігліколі, гідроксиламіни та ін.). Знаючи полярність нерухомої рідкої фази й полярність та хімічну природу речовин, які потрібно розділити, можна з певною ймовірністю вибрати найефективнішу рідку фазу для хроматографічного аналізу. Здебільшого добре розділення компонентів суміші спостерігається тоді, копи їх полярність близька до полярності нерухомої рідкої фази. Для речовин з близькою полярністю послідовність елюювання, як правило, корелює з їх температурою кипіння. Для розділення близькокиплячих речовин з різною полярністю використовують рідку фазу, яка селективно затримує компоненти суміші внаслідок диполь-дипольної взаємодії або утворення водневих зв'язків. Зі збільшенням полярності рідкої нерухомої фази час утримування полярних сполук збільшується.
Рідку нерухому фазу потрібно наносити на твердий носій (адсорбент) рівномірно. Для цього її змішують з летким розчинником, додають твердий носій, ретельно перемішують інагрівають до температури кипіння розчинника для його випарювання. При цьому рідка нерухома фаза, яка має значно вищу температуру кипіння, залишається на твердому адсорбенті.
У капілярних колонках рідка нерухома фаза закріплена безпосередньо на внутрішній поверхні капіляра.
Як рідкі нерухомі фази використовують: алкілові ефіри двоосновних органічних кислот (фталевої, себацинової, адипінової), полігліколі, ефіри полігліколів, високомолекулярні вуглеводні (сквалани, апієзони) (робоча температура – 100-160 ºС), полікарборанметилсилоксан (речовина з високою робочою температурою – 500 ºС).
Рідкі нерухомі фази перед вміщенням у хроматографічну колонку наносять на зерна твердого носія. До твердих носіїв ставляться такі вимоги:
1) розвинена питома поверхня – до 100 м2/г;
2) значний і по можливості однаковий об’єм пор – оптимальний діаметр від 0,5·10-3 до 1,5·10-3мм. При нанесенні рідини на такі носії більша частина рідини попадає в пори і тільки тонка плівка покриває решту поверхні, при цьому досягається висока ефективність розділення;
3) однакові за формою і за розмірами частинки. Для кожного діаметра колонки існує оптимальний розмір зерен твердого носія, необхідно добиватися якнайбільшої однорідності розмірів зерен носія. При звичайно застосовуваних діаметрах колонок (4-8 мм) оптимальний розмір зерен носія від 0,1 до 0,8 мм, оптимальний розмір – 0,15-0,3 мм;
4) хімічна і адсорбційна інертність. Силікатні носії або відщеплюють воду від спиртів, або здійснюють каталітичний вплив і викликають хімічні перетворення компонентів суміші. Ще частіше спостерігається адсорбційна взаємодія, внаслідок чого компонент не тільки розчиняється в плівці нерухомої рідини, але й адсорбується поверхнею твердого носія. Щоб звести до мінімуму небажану активність, присутню більшості твердих носіїв, їх хімічно або фізично модифікують. Хімічна модифікація полягає в обробці твердих носіїв мінеральними кислотами, лугами, органічними похідними силіцію – хлорсиланами, силозанами чи введення в молекулу носія алкільних груп. Фізичне модифікування відбувається шляхом попереднього нанесення на поверхню твердого носія полярних рідин чи полімерів;
5) здатність змочуватися рідкою нерухомою фазою;
6) механічна міцність.
Як тверді носії використовують: кізельгури, діатоміти (природні силікати з домішками заліза, кальцію, натрію, магнію), молекулярні сита, синтетичні пористі носії (тефлон, дивінілстирольні полімери).
– Конец работы –
Эта тема принадлежит разделу:
Тема 1. Введення в фізико-хімічні методи аналізу
ТЕМА РЕФРАКТОМЕТРИЧНИЙ МЕТОД АНАЛІЗУ... Метод що рунтується на вимірюванні показника заломлення називається рефрактометричним...
Если Вам нужно дополнительный материал на эту тему, или Вы не нашли то, что искали, рекомендуем воспользоваться поиском по нашей базе работ: Вплив швидкості потоку і тиску газу-носія на ефективність розділення.
Что будем делать с полученным материалом:
Если этот материал оказался полезным ля Вас, Вы можете сохранить его на свою страничку в социальных сетях:
| Твитнуть |
Хотите получать на электронную почту самые свежие новости?







Новости и инфо для студентов