рефераты конспекты курсовые дипломные лекции шпоры
Реферат Курсовая Конспект
Постулаты Бора. Спектр атома водорода по Бору.
Постулаты Бора. Спектр атома водорода по Бору. - Лекция, раздел Философия, Лекция 16. Теория атома водорода по Бору. Элементы квантовой механики. План лекции 2. Постулаты Бора. Спектр атома водорода по Бору 1. Электроны В Атоме Движутся По Строго Определенным Стационарным Орбитам, Не...
1. электроны в атоме движутся по строго определенным стационарным орбитам, не излучая и не поглощая при этом энергии.
 , (
, (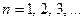 ),
),
где 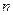 - номер орбиты;
- номер орбиты; 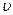 - скорость электрона;
- скорость электрона;  - радиус орбиты;
- радиус орбиты; 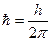 .
.
2. При переходе электрона с одной орбиты на другую атом излучает или поглощает энергию
 ,
,
где 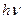 - энергия фотона;
- энергия фотона; 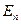 и
и 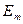 - энергии электрона на соответствующих орбитах.
- энергии электрона на соответствующих орбитах.
Постулаты Бора позволили ему теоретически рассчитать энергетический спектр атома водорода и водородоподобных атомов – атомов, состоящих из ядра с зарядом 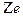 и одного электрона, движущегося вокруг ядра.
и одного электрона, движущегося вокруг ядра.
Можно доказать, что энергия электрона может принимать только определенные дискретные значения:
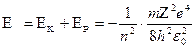 (n=1,2,3,….),
(n=1,2,3,….),
где 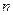 - номер стационарной орбиты, а знак минус означает, что электрон находится в связанном состоянии.
- номер стационарной орбиты, а знак минус означает, что электрон находится в связанном состоянии.
Из полученного выражения видно, что полная энергия электрона в водородоподобном атоме отрицательна и зависит от номера орбиты, по которой движется электрон, т.е. может принимать только дискретные значения.
При n=1 
Т.к. полная энергия отрицательна, то чем меньше её абсолютное значение, тем больше значение полной энергии. Следовательно, с ростом n энергия увеличивается.
При 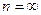
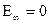 .
.
это и есть максимальное значение энергии системы, состоящей из ядра и одного электрона. Если электрону сообщить извне порцию энергии 13,55 эВ, то он уйдет с первой орбиты за пределы атома, а атом превратится в положительный ион. этот процесс отщепления электрона от атома называется ионизацией. Ионизация – это отщепление электронов от атомов, приводящее к образованию положительных ионов.
Величину энергии электрона в атоме часто отождествляют с энергией атома. Все возможные значения энергии атома, которыми он может обладать, называют энергетическими уровнями. Энергетические уровни атома изображают в виде горизонтальных прямых, расположенных друг относительно друга на расстояниях, пропорциональных разности энергий атома. Самая низшая прямая соответствует нормальному состоянию атома.
Используя теорию Бора и схему энергетических уровней атома, легко объяснить процессы испускания и поглощения излучения атомом.
Чтобы атом получил возможность испускать свет, его нужно возбудить, т.е. перевести электрон на более высокий энергетический уровень (нагреванием, освещением и т.д.). В возбужденном состоянии атом неустойчив и через t~ 10-8 c переходит на более близкую к ядру орбиту, испуская квант электромагнитного излучения (фотон) с энергией 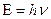 .
.
Согласно второму постулату Бора (для водорода  )
)
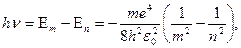
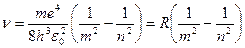 , (1)
, (1)
где  – постоянная Ридберга.
– постоянная Ридберга.
Исследования спектров излучения разряженных газов (т.е. отдельных атомов) показали, что каждому газу присущ определенный линейчатый спектр. Все обнаруженные серии в спектре атома водорода могут быть описаны одной эмпирической формулой , называемой обобщенной формулой Бальмера:
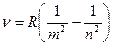 . (2)
. (2)
Для серии Лаймана (ультрафиолетовая область спектра) (рис. 2) m=1, n=2,3,4,…
Для серии Бальмера (видимая область спектра) m =2, n=3,4,5,…
Для серии Пашена (инфракрасная область спектра) m =3, n=4,5,6,…
Значения R в формулах (1) и (2) совпадают, что свидетельствует о правильности полученной Бором формулы (1).
 Теория Бора, на основе которой были рассмотрены спектры атома водорода и водородоподобных систем и вычислены частоты спектральных линий, не смогла объяснить интенсивности спектральных линий, вероятности возможных переходов и не позволила описать спектр атома гелия – одного из простейших атомов.
Теория Бора, на основе которой были рассмотрены спектры атома водорода и водородоподобных систем и вычислены частоты спектральных линий, не смогла объяснить интенсивности спектральных линий, вероятности возможных переходов и не позволила описать спектр атома гелия – одного из простейших атомов.
Все эти проблемы были решены в рамках квантовой механики.
– Конец работы –
Эта тема принадлежит разделу:
Лекция 16. Теория атома водорода по Бору. Элементы квантовой механики. План лекции 2. Постулаты Бора. Спектр атома водорода по Бору
гл... План лекции... Ядерная модель атома Резерфорда Постулаты Бора Спектр атома водорода по Бору...
Если Вам нужно дополнительный материал на эту тему, или Вы не нашли то, что искали, рекомендуем воспользоваться поиском по нашей базе работ: Постулаты Бора. Спектр атома водорода по Бору.
Что будем делать с полученным материалом:
Если этот материал оказался полезным ля Вас, Вы можете сохранить его на свою страничку в социальных сетях:
| Твитнуть |
Хотите получать на электронную почту самые свежие новости?







Новости и инфо для студентов