Определение объема кислорода для сжигания 1кг топлива
Каким бы сложным ни был состав углеводородного топлива, при его полном сгорании углерод окисляется до СО2, водород – до Н2О, сера – до SО2.
Рассмотрим стехиометрические уравнения реакций окисления:
 . (4.1)
. (4.1)
Для окисления одного кмоля углерода массой 12 кг требуется один кмоль кислорода, занимающего объем 22,4 м3. Следовательно, расход кислорода на полное сжигание 1 кг углерода равен  .
.
Тогда, если в 1 кг данного топлива содержится углерода (%)СР, то для его окисления потребуется кислорода:
 .
.
Здесь, как и в последующих формулах, коэффициент 0,01 необходим, поскольку при задании состава топлива доля углерода СР была задана в процентах.
Из второго уравнения (4.1) видно, что для окисления двух кмолей водорода массой 4 кг требуется один кмоль кислорода, т.е. на горение 1 кг водорода необходимо затратить кислорода 22,4/4 = 5,6 м3/кг.
Тогда для окисления водорода в количестве (%)НР, содержащегося в 1кг топлива, потребуется объем кислорода:
 .
.
Аналогично, для окисления (%)SР серы в 1кг топлива необходим кислород в объеме:
 .
.
В состав твердых и жидких топлив входит какое-то количество кислорода ОР, который при горении топлива может участвовать в реакциях окисления. Поэтому из суммарного объема кислорода, необходимого для горения 1 кг топлива, следует вычесть объем кислорода топлива. Найдем этот объем, используя мольное соотношение. Один кмоль кислорода массой 32 кг занимает объем 22,4 м3 , т.е. 1 кг кислорода имеет объем:
 .
.
Следовательно, объем кислорода, содержащегося в 1 кг топлива, составит:
 .
.
Отсюда общий расход кислорода, необходимого для полного сгорания 1 кг жидкого или твердого топлива, будет равен:
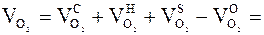
 . (4.2)
. (4.2)