МЕТОДИЧЕСКИЕ УКАЗАНИЯ И ЗАДАНИЯ К КУРСОВОЙ РАБОТЕ по дисциплине Основы информационных технологий и программирования Энергетический менеджмент , Теплоэнергетика
Министерство образования и науки Украины
Донецкий национальный технический университет
МЕТОДИЧЕСКИЕ УКАЗАНИЯ И ЗАДАНИЯ
К КУРСОВОЙ РАБОТЕ
по дисциплине «Основы информационных технологий и программирования»
для студентов специальностей
«Энергетический менеджмент», «Теплоэнергетика»
Утверждено
на заседании кафедры ВМиП
протокол № 3 от 09.10.2008 г.
Утверждено
методической комиссией ДонНТУ
протокол № от 2008 г.
Донецк – 2008
УДК 681.3.06 (071)
Методические указания и задания к курсовой работе по дисциплине «Основы информационных технологий и программирования» для студентов специальности «Энергетический менеджмент» / сост.: О.М.Копытова, С.В.Гридин. – Донецк: ДонНТУ, 2008 .- 76с.
Изложены цель и задачи курсовой работы, порядок выполнения, содержание и правила оформления. Приведены задания к курсовой работе, даны методические рекомендации по составу, выполнению и оформлению курсовой работы.
В приложениях дан справочный материал и рассмотрены примеры расчетов и оформления отдельных частей пояснительной записки.
Приведен список рекомендуемой литературы.
Авторы: О.М. Копытова, доц.,
С.В. Гридин, доц.
Отв. за выпуск В.Н. Павлыш, доц.
СОДЕРЖАНИЕ
1 ОБЩИЕ ПОЛОЖЕНИЯ.. 4
1.1 Цель и задачи курсовой работы.. 4
1.2 Организация выполнения курсовой работы.. 4
2 СОСТАВ КУРСОВОЙ РАБОТЫ И ТРЕБОВАНИЯ К ОФОРМЛЕНИЮ... 4
2.1 Структура пояснительной записки. 4
2.2 Требования к структурным элементам пояснительной записки. 5
2.3 Требования к оформлению пояснительной записки. 7
2.4 Рекомендации по разработке приложения для Windows. 7
3 КРАТКИЕ СВЕДЕНИЯ О ТОПЛИВЕ И ПРОЦЕССЕ ЕГО ГОРЕНИЯ.. 8
3.1 Введение. 8
3.2 Общие сведения о топливе. 9
3.3 Виды органического топлива. 9
3.4 Состав топлива. 10
3.5 Состояние топлива. 12
3.6 Удельная теплота сгорания топлива. 12
3.7 Цель и ограничения расчета процесса горения. 13
4 АНАЛИТИЧЕСКИЙ РАСЧЕТ ГОРЕНИЯ ТВЕРДОГО И ЖИДКОГО ТОПЛИВ 15
4.1 Определение объема кислорода для сжигания 1кг топлива. 15
4.2 Определение объема воздуха для сжигания 1 кг топлива. 16
4.3 Определение объема и состава продуктов сгорания. 17
5 АНАЛИТИЧЕСКИЙ РАСЧЕТ ГОРЕНИЯ ГАЗООБРАЗНОГО ТОПЛИВА.. 20
5.1 Расчет объема кислорода и воздуха для сжигания 1 м3 газа. 21
5.2 Расчет выхода продуктов сгорания. 22
6 ПРОВЕРКА ПРАВИЛЬНОСТИ РАСЧЕТА ПО МАТЕРИАЛЬНОМУ БАЛАНСУ 23
7 ЗАДАНИЕ К КУРСОВОЙ РАБОТЕ. 24
СПИСОК ЛИТЕРАТУРЫ.. 27
ПРИЛОЖЕНИЕ A. ГРАФИК ВЫПОЛНЕНИЯ КУРСОВОЙ РАБОТЫ.. 27
ПРИЛОЖЕНИЕ B. ПРИМЕРЫ ОФОРМЛЕНИЯ ОТДЕЛЬНЫХ ЭЛЕМЕНТОВ ПОЯСНИТЕЛЬНОЙ ЗАПИСКИ.. 28
ПРИЛОЖЕНИЕ С. ПРАВИЛА ОФОРМЛЕНИЯ ПОЯСНИТЕЛЬНОЙ ЗАПИСКИ 59
ПРИЛОЖЕНИЕ D. СПРАВОЧНЫЕ ТАБЛИЦЫ.. 62
ПРИЛОЖЕНИЕ E. ПРИМЕРЫ РАСЧЕТОВ ГОРЕНИЯ ТОПЛИВ.. 64
1 Расчет процесса горения жидкого топлива. 64
2 Расчет процесса горения природного таза. 68
ОБЩИЕ ПОЛОЖЕНИЯ
Цель и задачи курсовой работы
Курсовая работа выполняется на базе знаний, полученных при изучении курса «Основы информационных технологий и программирования» и общеобразовательных дисциплин.
Целью курсовой работы является закрепление теоретических знаний и практических навыков студентов по основам алгоритмизации, программирования и отладке программ при решении инженерной задачи.
Содержанием курсовой работы является расчетная технологическая задача одной из специальных дисциплин, читаемых студентам на старших курсах. В дальнейшем это позволит использовать результаты курсовой работы в научно-исследовательской работе студентов, в курсовом и дипломном проектировании.
Организация выполнения курсовой работы
Задание на выполнение курсовой работы выдается студенту руководителем. Студент оформляет лист задания, содержащий тему курсовой работы, дату выдачи, срок сдачи и исходные данные – в соответствии с темой и номером варианта. Лист задания подписывается руководителем курсовой работы.
При выдаче задания на курсовую работу руководителем устанавливается график выполнения работы (см. приложение А).
Основной формой выполнения курсовой работы является самостоятельная работа студента под руководством преподавателя. Курсовая работа должна быть выполнена в сроки, указанные в листе задания, и сдана на проверку руководителю. Оценка за выполнение курсовой работы выставляется комиссией, назначенной заведующим кафедрой. При неудовлетворительной оценке курсовая работа возвращается для исправления или дополнения либо студенту выдается новое задание.
СОСТАВ КУРСОВОЙ РАБОТЫ И ТРЕБОВАНИЯ К ОФОРМЛЕНИЮ
Структура пояснительной записки
Титульный лист
Лист задания
Реферат
Содержание
Введение
1. Постановка задачи
2. Контрольный пример
3. Блок-схема алгоритма
4. Описание алгоритма
5. Характеристика данных и их условные обозначения
6. Текст программы
7. Описание работы программы
8. График зависимости
9. Анализ результатов
Заключение
Список используемой литературы
Приложения
Требования к структурным элементам пояснительной записки
«Лист задания» (образец – в приложении В.2) отражает тему задания и исходные данные соответствующего варианта. «Реферат» (пример – в приложении В.3) предназначен для ознакомления с работой.… - сведения об объеме записки, количестве иллюстраций, таблиц, приложений, количестве источников по перечню ссылок;Требования к оформлению пояснительной записки
Пояснительная записка оформляется на листах формата А4 в текстовом редакторе WORD. Текст пояснительной записки должен быть набран 14 шрифтом и иметь следующие размеры полей: левое – 25мм., правое – 10мм., верхнее – 20мм., нижнее – 20мм., абзац – 15мм.
Каждый раздел пояснительной записки должен начинаться с новой страницы. Заголовки разделов нумеруются арабскими цифрами и отделяются от основного текста. Нумерация страниц сквозная, начиная с титульного листа. На титульном листе, листе задания, содержании и аннотации номера страниц не ставят, на последующих страницах номера указывают арабскими цифрами в правом верхнем углу.
Пояснительная записка представляется к защите в сброшюрованном виде.
В приложении С приведены подробные требования к оформлению.
Рекомендации по разработке приложения для Windows
1.Создать отдельный каталог для разрабатываемого приложения.
2.Создать в Delphi новый проект (команда File à New à Application) и сразу сохранить его в каталоге, созданном в п.1 [6,7].
3.Продумать и составить список действий, которые должны быть доступны будущему пользователю посредством различных элементов управления, как-то: кнопок, панелей инструментов, строки основного меню и др.
4.В компоненте ImageList подготовить список пиктограмм на кнопках для тех нестандартных действий, которые должны быть доступны из быстрых кнопок панели инструментов. Перенести на главную форму компонент диспетчеризации действий ActionList и связать его с ImageList.
5.Перенести на форму компонент MainMenu – главное меню и связать его с ImageList, а в его кнопках указать ссылки на действия, описанные в ActionList.
6.Создать на форме одну или несколько панелей инструментов, связав их с компонентами ActionList и ImageList.
7.Тщательно продумать и скомпоновать форму для каждого окна, которое будет выведено в приложении. Функционально связанные между собой элементы окна необходимо зрительно объединить в группы так, чтобы заголовок группы коротко и четко пояснял ее назначение. Для этого удобно использовать, например, панели Panel и GroupBox,расположенныена странице Standard.
8.Если пользователю необходимо выбирать некоторую информацию из нескольких заранее известных альтернатив, то рекомендуется использовать компонент ComboBox – выпадающий список. Для выбора одной из нескольких взаимоисключающих альтернатив следует использовать компонент RadioGroup.
9.Настроить свойства и указать методы каждого из объектов.
10.Написать и отладить все необходимые обработчики событий.
КРАТКИЕ СВЕДЕНИЯ О ТОПЛИВЕ И ПРОЦЕССЕ ЕГО ГОРЕНИЯ
Дальнейшее изложение основано на работах [1]÷[5], примеры конкретных расчетов горения топлива взяты из [3].
Введение
Человечество не может жить и развиваться без выработки и потребления тепловой энергии. За последние 30 лет мировое энергопотребление удвоилось и ежегодно составляет порядка 10 млрд. тонн в нефтяном эквиваленте. При нынешних темпах развития на рубеже 2050 года этот показатель может достигнуть уже 30 млрд. тонн. По оценкам экспертов, доказанные мировые запасы нефти сегодня составляют примерно 270 млрд. тонн, газа – 240 млрд. тонн н.э. Этого топлива хватит на 52-94 года, если сохранится существующий уровень потребления.
Сегодня источниками получения энергии являются, прежде всего, ископаемые топлива всех видов (95%), гидроэнергетика (около 4%) и атомная энергетика (немногим более 1%).
В технике одно из ведущих мест занимает процесс горения, являясь основой энергетики, транспорта, большинства технологических процессов и быта. По потреблению энергии можно судить об уровне развития страны. Поскольку природные запасы источников топливной энергии ограничены, важной задачею является экономное использование топливно-энергетических ресурсов.
С другой стороны, при сжигании топлива, вырабатываются продукты, вредно влияющие на окружающую среду. Поэтому еще одним важным моментом использования топлива в качества источника тепловой энергии является охрана окружающей среды.
Из сказанного вытекает следующий вывод: для экономичного и экологически чистого использования топлива необходимо уметь правильно рассчитывать процесс горения и грамотно управлять им.
Общие сведения о топливе
Топливом называют вещества, которые в результате физико-химических процессов способны выделять тепловую энергию и которые на данном уровне развития техники экономически целесообразно использовать для выработки энергии. Топливо, используемое для выработки электроэнергии и теплоты в промышленном масштабе, называют энергетическим.
Различают два вида топлива, отличающиеся по принципу освобождения энергии:
· органическое топливо, которое выделяет тепловую энергию в результате химических реакций окисления горючих компонентов, входящих в его состав. Окисление, протекающее с высокой скоростью, и называют горением;
· ядерное топливо, которое выделяет тепловую энергию в результате физических процессов преобразования вещества на ядерном уровне (деление ядер тяжелых элементов, синтез ядер легких элементов и т.п.).
К топливу предъявляется ряд требований:
· запасы топлива должны быть достаточны для экономически выгодной его добычи;
· продукты реакции должны легко удаляться из зоны реагирования;
· продукты реакции должны быть безвредны для окружающей среды и устройств, где происходит реагирование;
· процесс реакции должен быть легко управляемым.
Наилучшим образом в настоящее время этим требования удовлетворяет органическое топливо, в основе которого лежат органические вещества, содержащие углерод, водород, кислород и их соединения. Поэтому, несмотря на бурное развитие ядерной энергетики во второй половине ХХ века, сегодня доля выработки энергии на основе использования органического топлива остается преобладающей.
Виды органического топлива
По сфере потребления топлива разделяют на две группы: энергетические – потребляемые энергопредприятиями при выработке электроэнергии и теплоты; и… По агрегатному состоянию органическое топливо может быть твердым, жидким и… В настоящее время в основном используются следующие энергетические органические топлива: в качестве твердого топлива –…Состав топлива
Любое топливо можно рассматривать как вещество, состоящее из отдельных химических элементов. Поэтому, говоря о химическом составе, часто применяют… Состав твердого и жидкого топлива определяется в процессе лабораторного…Состояние топлива
CР + НР + SP + NР + ОР + АР + WР = 100%; (3.3) СС + НС + SC + NС + ОС + А С = 100%; (3.4) СГ + НГ + SГ + NГ + ОГ = 100%; (3.5)Удельная теплота сгорания топлива
Теплота сгорания топлива Q – это количество теплоты, выделяемое единицей топлива (1кг или 1м3) при его полном сгорании. В продуктах сгорания топлива всегда содержится водяной пар, образовавшийся при… В связи с этим различают высшую и низшую теплоту сгорания топлива.Цель и ограничения расчета процесса горения
Целью расчета горения топлива является определение следующих количественных характеристик:
· теплота сгорания топлива (  , кДж/кг или кДж/м3 );
, кДж/кг или кДж/м3 );
· теоретический и действительный расходы атмосферного воздуха, необходимого для полного сжигания единицы топлива (L, м3/кг или м3/м3);
· выход (V , м3/кг или м3/м3) и состав продуктов полного сгорания;
· проверка материального баланса и расчет неувязки (в процентах).
Расчет указанных характеристик будем осуществлять на основе предоставленного химического состава топлива (точные расчеты).
В процессе расчета будут действовать следующие допущения:
1) все расчеты ведутся на единицу топлива (1 кг для твердых и жидких и 1 м3 для газообразных топлив);
2) все газовые объемы рассчитываются при нормальных условиях, т.е. при 0°С и давлении 760 мм рт.ст.;
3) объем одного кмоля газов в этих условиях принимается равным 22,4 м3;
4) в качестве окислителя используется атмосферный воздух, состав которого считается постоянным: в единице объема воздуха – 21% кислорода и 79% азота. Соотношение азота и кислорода воздуха представляется в виде константы
 . (3.10)
. (3.10)
5) связь между количеством продуктов реакции и количеством реагирующих веществ устанавливается на основании следующих положений:
а) все химические соединения состоят из атомов отдельных элементов, связанных в определенных численных соотношениях;
б) атомы при химических реакциях сохраняют свою индивидуальность, т. е. при реакции происходит только перегруппировка атомов.
Для расчетов будем использовать балансовые уравнения, показывающие исходные и конечные состояния компонентов, участвующих в реакциях. Такие уравнения называются стехиометрическими, а характеристикам, полученным на основе стехиометрических соотношений, присваивают индекс "ноль".Так, количество воздуха, теоретически необходимоедля сжигания единицы топлива, будет обозначаться L0, а теоретический выход продуктов сгорания от сжигания единицы топлива будет обозначаться V0.
Однако на практике для полного сгорания топлива теоретически необходимого количества воздуха бывает недостаточно. Причинами этого могут быть неравномерная подача воздуха, плохое перемешивание воздуха с топливом, несовершенство сжигающих устройств и др. Поэтому в реальных условиях для обеспечения полного окисления горючих составляющих топлива воздух подают с некоторым избытком. Это действительное (практическое) количество введенного воздуха, необходимое для сжигания единицы топлива, обозначают La (м3/кг или м3/м3).
Отношение действительного количества воздуха к теоретически необходимому называют коэффициентом избытка воздуха(a):
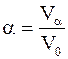 .
.
Коэффициент избытка воздуха зависит от вида топлива, способа его сжигания и т.д. Для газообразного топлива обычно a =1,05 ÷ 1,1; жидкого a =1,1 ÷ 1,3; твердого a =1,2 ÷ 1,7. Чем совершеннее топка и лучше горелочные устройства, тем меньше приходится подавать «лишнего» воздуха.
Действительный (практический) выход продуктов сгорания, который образуется при конкретном коэффициенте a, обозначается Va.
Для составления стехиометрических уравнений необходимо знать соотношение масс. Каждый атом определенного элемента в любом химическом соединении имеет одну и ту же массу. По уравнению химической реакции можно найти массы реагентов и продуктов реакции.
Атомные и молекулярные веса веществ, обычно образующихся при сгорании топлива, приведены в таблице D.4 приложения. Десятичными знаками обычно пренебрегают.
Рассмотрим точные расчеты горения топлив, основанные на стехиометрических соотношениях горючих составляющих и окислителя. Такие расчеты принято называть аналитическими.
АНАЛИТИЧЕСКИЙ РАСЧЕТ ГОРЕНИЯ ТВЕРДОГО И ЖИДКОГО ТОПЛИВ
Для аналитического расчета необходимо знать элементарный состав топлива (см. формулу 3.3):
CР + НР + SP + NР + ОР + АР + WР = 100%
В данной формуле состав топлива задан в процентах по массе. При этом кислород, необходимый для окисления горючих элементов, нужно определить по объему – в кубических метрах. Для перехода от одной единицы измерения к другой будем использовать мольное соотношение кислорода и горючего элемента в реакции окисления.
Определение объема кислорода для сжигания 1кг топлива
Рассмотрим стехиометрические уравнения реакций окисления: . (4.1) Для окисления одного кмоля углерода массой 12 кг требуется один кмоль кислорода, занимающего объем 22,4 м3.…Определение объема воздуха для сжигания 1 кг топлива
м3/кг, (4.3) где K = 3,76 (см. формулу(3.10)).Определение объема и состава продуктов сгорания
В результате полного сжигания топлива при a = 1 образуются продукты сгорания, содержащие СО2, SO2, Н2О и N2. Объем дымовых газов, образующихся при сгорании 1кг твердого или жидкого…АНАЛИТИЧЕСКИЙ РАСЧЕТ ГОРЕНИЯ ГАЗООБРАЗНОГО ТОПЛИВА
Влага в рабочем составе газообразного топлива находится в виде водяных паров. Содержание влаги зависит от температуры газа. В приложении D.5… Обычно влажный состав рассчитывают так же, как для твердого и жидкого топлива.… или (5.1)Расчет выхода продуктов сгорания
Объемы отдельных составляющих продуктов сгорания составляют: , м3/м3; (5.9) м3/м3; (5.10)ПРОВЕРКА ПРАВИЛЬНОСТИ РАСЧЕТА ПО МАТЕРИАЛЬНОМУ БАЛАНСУ
При правильном расчете количеств веществ, участвующих в процессе горения… Мтопл + Mвозд = Мгор ± DM, (6.1)ЗАДАНИЕ К КУРСОВОЙ РАБОТЕ
ТЕМА КУРСОВОЙ РАБОТЫ: «РАСЧЕТ ГОРЕНИЯ ТОПЛИВА»
ЗАДАНИЕ.В соответствии с вариантом разработать алгоритм и составить программу расчета горения топлива.
ПОСТАНОВКА ЗАДАЧИ.
I.Для заданного топлива и условий его сжигания вычислить следующие параметры горения:
1) состав топлива во влажном (рабочем) состоянии – если исходным является состояние, отличное от рабочего;
2) теплоту сгорания топлива (нижнюю);
3) теоретическое и действительное количества воздуха, необходимого для сжигания единицы топлива;
4) количество и состав продуктов сгорания единицы топлива без избыточного воздуха и с избыточным воздухом;
5) материальный баланс горения топлива: для жидких и твердых топлив вычислить баланс для топлива массой 1000 кг, для газообразных топлив – объем топлива принять равным 100 м3.
II.Построить в MS Excel диаграмму (диаграммы) – в соответствии с вариантом.
ТРЕБОВАНИЯ К ВЫПОЛНЕНИЮ.
2.В программе предусмотреть следующие пункты: a. Ввод исходных данных; b. Вычисление параметров процесса горения и вывод их в окно приложения;ВАРИАНТЫ ИСХОДНЫХ ДАННЫХ
Жидкое и твердое топливо
| Вариант | Состав, % ( массы) | a | dС.В., г/м3 | tС.В., 0С | ||||||
| CP | HP | OP | NP | SP | AP | WP | ||||
| Мазут | ||||||||||
| 1. | 88,0 | 8,5 | 0,4 | 0,3 | 0,5 | 0,3 | 2,0 | 1,30 | 14,0 | |
| 2. | 84,7 | 9,9 | 0,5 | 0,4 | 0,7 | 0,2 | 3,6 | 1,38 | 15,1 | |
| 3. | 86,2 | 9,7 | 0,3 | 0,5 | 0,4 | 0,1 | 2,8 | 1,26 | ||
| 4. | 87,0 | 8,6 | 0,2 | 0,3 | 0,6 | 0,3 | 3,0 | 1,37 | 13,2 | |
| 5. | 84,6 | 10,7 | 0,4 | 0,4 | 0,3 | 0,2 | 3,4 | 1,34 | 13,9 | |
| 6. | 87,6 | 8,3 | 0,5 | 0,4 | 0,5 | 0,1 | 2,6 | 1,27 | 15,3 | |
| 7. | 86,9 | 9,2 | 0,3 | 0,3 | 0,7 | 0,3 | 2,3 | 1,32 | 15,4 | |
| 8. | 85,5 | 10,3 | 0,2 | 0,4 | 0,5 | 0,2 | 2,9 | 1,29 | 13,4 | |
| 9. | 87,9 | 8,0 | 0,4 | 0,5 | 0,6 | 0,1 | 2,5 | 1,36 | ||
| Кокс | ||||||||||
| 10. | 91,8 | 1,3 | 1,1 | 1,3 | 1,1 | 0,4 | 3,0 | 1,46 | 15,2 | |
| 11. | 95,1 | 0,6 | 0,8 | 0,9 | 0,6 | 0,2 | 1,8 | 1,48 | 13,9 | |
| 12. | 93,6 | 1,0 | 0,9 | 1,1 | 0,7 | 0,3 | 2,4 | 1,52 | ||
| 13. | Каменный уголь | |||||||||
| 14. | 79,3 | 5,2 | 1,0 | 0,8 | 0,5 | 8,6 | 4,6 | 1,50 | 13,3 | |
| 15. | 83,9 | 3,8 | 0,9 | 1,2 | 0,8 | 5,6 | 3,8 | 1,47 | 14,5 | |
| 16. | 81,7 | 4,1 | 1,2 | 1,1 | 0,7 | 7,7 | 3,5 | 1,49 | 15,8 | |
| 17. | 79,8 | 5,0 | 0,8 | 1,3 | 0,6 | 8,4 | 4,1 | 1,45 | 13,8 | |
| 18. | 83,2 | 4,5 | 1,3 | 0,5 | 6,7 | 2,8 | 1,51 | 12,9 | ||
| 19. | 82,4 | 4,9 | 1,1 | 0,9 | 0,7 | 6,9 | 3,1 | 1,44 | 14,1 | |
| Торф | ||||||||||
| 20. | 49,1 | 6,1 | 6,5 | 0,8 | 0,1 | 6,2 | 31,2 | 1,51 | ||
| 21. | 50,4 | 5,9 | 6,8 | 0,9 | 0,1 | 3,9 | 32,0 | 1,46 | 12,1 | |
| 22. | 54,7 | 6,0 | 5,3 | 0,7 | 0,1 | 3,1 | 30,1 | 1,48 | 10,2 |
Газообразное топливо
| Вариант | Состав, % ( объема) | a | dС.Г., г/м3 | tС.В., 0С | |||||||

| 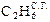
| 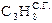
| 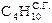
| 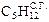
| 
| 
| 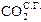
| ||||
| 23. | 88,0 | 1,9 | 0,2 | 0,3 | 9,3 | 0,3 | 1,2 | 5,0 | |||
| 24. | 76,7 | 4,5 | 1,7 | 0,8 | 0,6 | 1,0 | 14,5 | 0,2 | 1,3 | 5,0 | |
| 25. | 92,2 | 0,8 | 0,1 | 6,9 | 1,2 | 5,0 | |||||
| 26. | 94,0 | 4,5 | 0,7 | 0,4 | 0,2 | 0,2 | 1,15 | 5,0 | |||
| 27. | 97,9 | 0,1 | 1,8 | 0,2 | 1,1 | 5,0 | |||||
| 28. | 97,9 | 0,5 | 0,2 | 0,1 | 1,2 | 0,1 | 1,15 | 5,0 | |||
| 29. | 98,0 | 0,4 | 0,2 | 1,3 | 0,1 | 1,05 | 6,0 | ||||
| 30. | 93,5 | 4,0 | 1,0 | 0,5 | 0,5 | 0,4 | 0,1 | 1,1 | 5,0 | ||
| 31. | 95,5 | 1,0 | 0,2 | 0,1 | 3,1 | 0,1 | 1,2 | 5,0 | |||
| 32. | 97,5 | 0,6 | 0,3 | 0,2 | 0,2 | 1,1 | 0,1 | 1,1 | 5,0 | ||
| 33. | 97,2 | 0,4 | 0,9 | 0,6 | 0,5 | 0,3 | 0,1 | 1,2 | 6,0 | ||
| 34. 2 | 91,7 | 5,4 | 1,2 | 0,7 | 1,2 | 6,0 | |||||
| 35. | 94,0 | 3,3 | 0,3 | 0,2 | 1,7 | 0,5 | 1,3 | 6,0 | |||
| 36. | 86,43 | 4,84 | 1,48 | 0,452 | 1,267 | 4,95 | 0,581 | 1,2 | 6,0 | ||
| 37. | 98,0 | 1,8 | 0,2 | 1,15 | 6,0 | ||||||
| 38. | 97,7 | 1,6 | 0,7 | 1,1 | 6,0 | ||||||
| 39. | 60,0 | 40,0 | 1,15 | 6,0 | |||||||
| 40. | 97,9 | 0,5 | 0,2 | 0,05 | 1,3 | 0,05 | 1,05 | 6,0 |
Построить следующие диаграммы.
1) для вариантов 1÷ 22 – диаграммы, отображающие состав продуктов горения при a=1 и при a>1;
2) для вариантов 23 ÷ 40 – диаграммы, отображающие состав газа в сухом и в рабочем состоянии.
СПИСОК ЛИТЕРАТУРЫ
1. Теплотехника: Учеб. для вузов / А. П. Баскаков, Б. В. Берг, О. К. Витт и др.; Под ред. А. П. Баскакова, – 2-е изд., перераб. – М.: Энергоатомиздат, 1991. – 224 с: ил.
2. Белосельский Б.С. Технология топлива и энергетических масел: Учебник для вузов. М.: Изд-во МЭИ, 2003. – 340 с.
3. Гущин С.Н., Казяев М.Д. Расчеты горения топлив: Учеб. пособие. Екатеринбург: УГТУ-УПИ, 1995. – 38 с.
4. Григорьев К.А., Рундыгин Ю.А., Тринченко А.А. Технология сжигания органических топлив. Энергетические топлива: Учеб. пособие. СПб.:Изд-во Политехн. ун-та, 2009. – 92 с.
5. Методические указания по расчету горения газообразного топлива с применением ЭВМ (для студентов металлургических и энергетических специальностей) / Сост. Е.И.Казанцев, С.И.Гинкул, А.Н.Лебедев. – Донецк: ДПИ, 1988. – 24 с.
6. Архангельский А.Я. Язык Pascal и основы программирования в Delphi. Учебное пособие – М.:ООО "Бином-Пресс", 2004 г. – 496 с.
7. Методические указания и задания к лабораторным работам по алгоритмизации и программированию в среде Delphi (для студентов всех специальностей) / О.М.Копытова, Н. К. Шатохина. - Донецк: ДонНТУ, 2007. – 84 с.
ПРИЛОЖЕНИЕ A. ГРАФИК ВЫПОЛНЕНИЯ КУРСОВОЙ РАБОТЫ
| №п/п | Виды работ (наименование разделов) | Срок выполнения (неделя семестра) | Отметка о выполнении |
| 1. | Введение. Постановка задачи | 1-2 | |
| 2. | Контрольный пример: расчеты и формулы | 3-4 | |
| 3. | Построение диаграммы | ||
| 4. | Анализ результатов | ||
| 5. | Структура данных и их условные обозначения | ||
| 6. | Блок-схема алгоритма | ||
| 7. | Компоновка форм проекта | ||
| 8. | Составление и отладка программы | 10-12 | |
| 9. | Оформление пояснительной записки | 13-15 | |
| 11. | Защита курсовой работы | 16-17 |
ПРИЛОЖЕНИЕ B. ПРИМЕРЫ ОФОРМЛЕНИЯ ОТДЕЛЬНЫХ ЭЛЕМЕНТОВ ПОЯСНИТЕЛЬНОЙ ЗАПИСКИ
Приложение B.1. Титульный лист
Министерство образования и науки Украины
ДОНЕЦКИЙ НАЦИОНАЛЬНЫЙ ТЕХНИЧЕСКИЙ УНИВЕРСИТЕТ
Кафедра вычислительной
математики и программирования
ПОЯСНИТЕЛЬНАЯ ЗАПИСКА
К курсовой работе по дисциплине
«Основы информационных технологий и программирования»
студента ______________________________________
Группы фак-та
_______________________________________________
ФИО
(зачетная книжка№ )
Руководитель работы: _________________
ФИО руководителя
Донецк-200_
Приложение B.2. Лист задания
Министерство образования и науки Украины
ДОНЕЦКИЙ НАЦИОНАЛЬНЫЙ ТЕХНИЧЕСКИЙ УНИВЕРСИТЕТ
ЗАДАНИЕ
на курсовую работу по дисциплине
«Основы информационных технологий и программирования»
студенту ______________________________________
Группы фак-та
_______________________________________________
ФИО
ТЕМА КУРСОВОЙ РАБОТЫ:
«Расчет горения природного газа»
Дата выдачи задания: 15.09.2009
Срок сдачи работы: 15.12.2009
Исходные данные
Руководитель ___________________. . . . . .
50.Конец алгоритма.
Приложение B.8. Характеристика данных и их условные обозначения
| № п/п | Наименование данных и единица измерения | Обозначение в блок-схеме | Обозначение в программе | Тип переменной |
| Состав природного газа в сухом состоянии, % | СH4c.г. С3Н8с.г. С4Н10с.г. N2с.г. | СН4 С3Н8 С4Н10 N2 | real real real real | |
| Состав природного газа во влажном состоянии, % | СH4в.г. С3Н8в.г. С4Н10в.г. N2в.г. | СН4v С3Н8v С4Н10v N2v | real real real real | |
| Таблица D.5 – 2 строки: D5t – массив температур, 0C D5d – содержание влаги, г/м3 | D5t D5d | D5t D5d | array[1..9]of integer array[1..9]of real | |
| Содержание водяных паро в сухом газе, % | dс.г. | dsg | real | |
| … | … | … | … |
Приложение B.9. Текст программы
Основной модуль
interface uses Windows, Messages, SysUtils, Classes, Graphics, Controls, Forms,Модуль ввода исходных данных и пересчета на влажный газ
unit U_ish_dan; interfaceМодуль вычисления результата
unit U_rez;Модуль просмотра файла с решением в окне формы
unit U_resh; interfaceПРИЛОЖЕНИЕ С. ПРАВИЛА ОФОРМЛЕНИЯ ПОЯСНИТЕЛЬНОЙ ЗАПИСКИ
Пояснительную записку оформляют на листах формата А4 (210х297 мм) машинным (при помощи компьютерной техники) способом на одной стороне листа белой бумаги. Междустрочный интервал выбирают из расчета не более 40 строк на странице при условии равномерного ее заполнения и высоте букв не менее h=2,5 мм, соблюдая при этом следующие размеры полей: верхнее, левое и нижнее – не менее 20 мм, правое – не менее 10 мм.
Ошибки, описки и графические неточности допускается исправлять подчисткой или закраской белой краской и нанесением на том же месте или между строк исправленного изображения машинописным способом или от руки.
Каждый пункт, подпункт и перечисление записываются с абзацного отступа.
Разделы и подразделы должны иметь заголовки. Пункты, как правило, заголовков не имеют. Заголовки должны четко и кратко отражать содержания разделов и подразделов.
Заголовки структурных элементов записки и заголовки разделов следует располагать в середине строки и печатать прописными буквами без точки в конце, не подчеркивая. Заголовки подразделов, пунктов и подпунктов записки следует начинать с абзацного отступа и печатать кроме первой прописной строчными буквами, не подчеркивая, без точки в конце. Если заголовок состоит из двух предложений, их разделяют точкой. Расстояние между заголовком и текстом при выполнении записки должно быть не менее двух строк
Каждый раздел текстового документа следует начинать с нового листа. Переносы слов в заголовке не допускаются.
Текст пояснительной записки должен быть кратким, четким и не допускать различных толкований.
Структурные элементы «Реферат», «Введение», «Заключение», «Список литературы» не нумеруют, а их наименования служат заголовками структурных элементов. Разделы, подразделы, пункты, подпункты следует нумеровать арабскими цифрами, например 1, 2, 3, и т.д. Подразделы должны иметь порядковую нумерацию в пределах каждого раздела. Номер подраздела состоит из номера раздела и порядкового номера подраздела, разделенных точкой. После номера подраздела точку не ставят, например 1.1, 1.2 и т.д. Пункты должны иметь порядковую нумерацию в пределах каждого раздела или подраздела, например, 1.1, 1.2 или 1.1.1, или 1.1.2 и т.д.
Нумерация страниц записки
Страницы пояснительной записки следует нумеровать арабскими цифрами, соблюдая сквозную нумерацию по всему тексту. Номер страницы проставляют в правом верхнем углу страницы без точки в конце. «Титульный лист», «Лист задания» включают в общую нумерацию страниц записки. Номер страницы на титульном листе не проставляется. Иллюстрации и таблицы, расположенные на отдельных страницах, включают в общую нумерацию страниц записки.
Построение таблиц
Таблицы, за исключением таблиц приложений, можно нумеровать арабскими цифрами сквозной нумерацией и в пределах разделов. В последнем случае номер… Таблицы каждого приложения обозначают отдельной нумерацией арабскими цифрами с… На все таблицы должны быть приведены ссылки в тексте записки. При ссылке следует писать слово «таблица (табл. )» с…Формулы и уравнения
Формулы и уравнения в записке следует нумеровать порядковой нумерацией в пределах раздела. Номер формулы или уравнения состоит из номера формулы или… Пояснение значений символов и числовых коэффициентов, входящих в формулу или… Пояснения каждого символа и числового коэффициента следует давать с новой строки. Первую строку пояснений следует…Приложения
Материал, дополняющий текст пояснительной записки, допускается помещать в приложениях. Приложениями могут быть, например, графический материал, таблицы большого формата, расчеты, описания аппаратуры, описания алгоритмов и программ задач, решаемых на ЭВМ, если это не является основной задачей работы.
Приложения оформляют как продолжение данного документа на последующих его листах. Приложения должны иметь общую с остальной частью сквозную нумерацию страниц. В тексте пояснительной записки на все приложения должны быть даны ссылки. Приложения располагают в порядке ссылок на них в тексте пояснительной записки.
Каждое приложение следует начинать с новой страницы с указанием наверху посередине страницы слова «Приложение» и его обозначения. Приложение должно иметь заголовок, который записывают симметрично относительно текста с прописной буквы отдельной строкой.
ПРИЛОЖЕНИЕ D. СПРАВОЧНЫЕ ТАБЛИЦЫ
Таблица D.1
Виды органического топлива
| Aгpeгатнoe состояние | Природное топливо | Искусственное топливо |
| Твердое | Ископаемое: Торф Бурый уrоль Каменный уrоль Антpацит Горючий сланец Возобновляемое: Древесина | Торфяной брикет Буроуrольный брикет Кокс Полукокс Древесный уrоль Древесные отходы Гидролизный лигнин Сельскохозяйственные отходы |
| Жидкое | Нефть | Мазут Дизельное топливо Бензин Керосин Сланцевое масло |
| Газообразное | Газ: Природный Попутный | Газ: Сжиженный Коксовый Доменный Пиролизный |
Таблица D.2
Состав сухого воздуха
| О2 | N2 | А (аргон) | |
| Состав сухого воздуха по объему, % | 20,99 | 78,03 | 0,98 |
| Состав сухого воздуха по весу, % | 23,19 | 75,46 | 1,35 |
Таблица D.3
Формулы коэффициентов для пересчета состава топлива из одного состояния в другое
| Исходное состояние топлива | Пересчет в состояние топлива | ||
| рабочее | сухое | горючее | |
| рабочее | 
| 
| |
| сухое | 
| 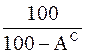
| |
| горючее | 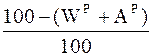
| 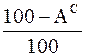
|
Таблица D.4
Атомные и молекулярные веса веществ, образующихся при сгорании топлива
| Элемент | Атомный вес | Вещество | Молекулярный вес |
| О | 16,000 | О2 | 32,000 |
| H | 1,008 | Н2 | 2,016 |
| N | 14,008 | N2 | 28,016 |
| С | 12,010 | CO2 | 44,010 |
| S | 32,070 | CO | 28,010 |
| Н20 | 18,016 | ||
| SO2 | 64,070 |
Таблица D.5
Влагосодержание сухого воздуха в зависимости от температуры
| t, °С | |||||||||
| dС.В., г/м3 | 4,9 | 7,0 | 9,8 | 19,0 | 35,1 | 63,1 | 111,3 | 197,0 | 356,0 |
ПРИЛОЖЕНИЕ E. ПРИМЕРЫ РАСЧЕТОВ ГОРЕНИЯ ТОПЛИВ
Расчет процесса горения жидкого топлива
Исходные данные
Задан химический состав мазута (в процентах по массе):
| CР | НР | SP | NР | ОР | АР | WР |
| 85,9 | 9,9 | 0,4 | 0,3 | 0,5 | 0,2 | 2,8 |
и следующие параметры:
коэффициент избытка воздуха a = 1,28;
влажность сухого воздуха dС.В. = 13,9 г/м3.
Расчет теплоты сгорания мазута
Низшую теплоту сгорания мазута вычислим по формуле (3.8):
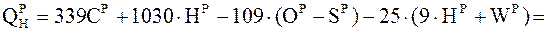
=339 × 85,9 + 1030 × 9,9 + 109 × (0,5-0,4) – 25 × (9 × 9,9+2,8) = 37008,7 кДж/кг.
Определение количества воздуха, необходимого для сжигания 1 кг мазута
= = 0,01× ( 1,867 × 85,9 + 5,6 × 9,9 + 0,7 × 0,4 - 0,7…Проверка материального баланса горения
Масса мазута равна 1000 кг. Для вычисления расхода воздуха произведем пересчет воздуха на влажную массу по… H2O В.В. = 100 × dС.В. /(803,6+dС.В.)=100 × 13,9/(803,6+13,9) = 1,7 %;Расчет процесса горения природного таза
Исходные данные
Сжигается природный газ, элементарный состав которого на сухую массу равен:
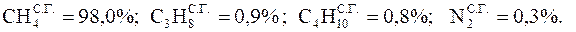
Влагосодержание сухого газа составляет dС.Г. = 5,0 г/м3 .
Коэффициент избытка воздуха a = 1,15.
Температура атмосферного воздуха равна t = 10°С.
Пересчет состава газа на рабочую (влажную) массу
. По формуле (5.2) вычислим коэффициент пересчета с сухого газа на влажный: .Расчет теплоты сгорания природного газа
=358×97,394+913×0,894+1185×0,796=36625,5 кДж/м3.Проверка материального баланса горения
Плотность топлива по формуле (6.3) равна: rтопл = 16 × CH4В.Г.+44 × C3H8 В.Г. +58 × C4H10 В.Г. +28… = 16 × 97,394% +44 × 0,894% +58 × 0,795% +28 × 0,298% +18 × 0,618% =МЕТОДИЧЕСКИЕ УКАЗАНИЯ И ЗАДАНИЯ
К КУРСОВОЙ РАБОТЕ
по дисциплине «Основы информационных технологий и программирования»
для студентов специальности
«Энергетический менеджмент»
Составители: Копытова Ольга Михайловна, к.ф.-м.н., доцент,
Гридин Сергей Васильевич, к.т.н., доцент
Формат 60х84 1/16, усл. печ. лист. – 4
Тираж –75 экз.
83000, г. Донецк, ул. Артема, 58, ДонНТУ