рефераты конспекты курсовые дипломные лекции шпоры
- Раздел Философия
- /
- Сущность фармакологии как науки. Разделы и области современной фармакологии. Основные термины и понятия фармакологии – фармакологическая активность, действие, эффективность химических веществ.
Реферат Курсовая Конспект
Сущность фармакологии как науки. Разделы и области современной фармакологии. Основные термины и понятия фармакологии – фармакологическая активность, действие, эффективность химических веществ.
Сущность фармакологии как науки. Разделы и области современной фармакологии. Основные термины и понятия фармакологии – фармакологическая активность, действие, эффективность химических веществ. - раздел Философия, 1. Сущность Фармакологии Как Науки. Разделы И Области Современной Фар...
1. Сущность фармакологии как науки. Разделы и области современной фармакологии. Основные термины и понятия фармакологии – фармакологическая активность, действие, эффективность химических веществ.
Фармакология – наука о лекарствах во всех аспектах – теоретическая основа терапии:
а) наука о взаимодействии химических веществ с живыми системами
б) наука об управлении процессами жизнедеятельности организма с помощью химических веществ
Развитие фармакологии идет по двум главным направлениям: фундаментальные исследования для выяснения принципов и механизмов действия ЛС и разработка эффективных препаратов как основы лечения заболеваний.
Фармакологию подразделяют на:
1. Общую - изучает общие закономерности взаимодействия лекарственных веществ с живыми организмами.
Частную – рассматривает конкретные фармакологические группы и отдельные препараты
2. Экспериментальную (базисную) фармакологию – изучает действие лекарств в эксперименте.
Клиническую фармакологию – изучает клиническую эффективность и безопасность
применения лекарств у пациентов, оптимизирует программу лечения пациента с учетом
его состояния.
Токсикологию – изучает токсическое действие на органы различных веществ (в том числе
и лекарственных).
Разделы современной фармакологии:
1) фармакодинамика – изучает а) воздействие ЛС на организм человека, б) взаимодействие различных ЛС в организме при одновременном их назначении, в) влияние возраста и различных заболеваний на действие ЛС
2) фармакокинетика – изучает всасывание, распределение, метаболизм и экскрецию ЛС (т.е. как организм больного реагирует на ЛС)
3) фармакогенетика– изучает роль генетических факторов в формировании фармакологического ответа организма на ЛС
4) фармакоэкономика– оценивает результаты использования и стоимость ЛС для принятия решения о последующем их практическом применении
5) фармакоэпидемиология – изучает применение ЛС и их эффекты на уровне популяций или больших групп людей для обеспечения применения наиболее эффективных и безопасных ЛС
Основные термины и понятия:
Фармакологическая (биологическая) активность – свойство вещества вызывать изменения в биосистеме (организме человека). Фармакологические вещества = биологически активные вещества (БАВ)
Фармакологическое действие – влияние ЛС на объект и его мишени
Фармакологический эффект – результат действия вещества в организме (модификация физиологических, биохимических процессов, морфологических структур) – количественное, но не качественное изменение в состоянии биосистем (клеток, тканей, органов).
Эффективность ЛС – способность ЛС вызывать определенные необходимые в данном случае фармакологические эффекты в организме. Оценивается на основе «существенных доказательств» - адекватных хорошо контролируемых исследований и клинических испытаний, проводимых экспертами с соответствующей научной подготовкой и опытом в исследовании лекарств данного типа {FDA}
2. Источники и этапы создания лекарств. Лекарства – генерики, плацебо - эффекты Определение понятий лекарственное вещество, лекарственное средство, лекарственный препарат и лекарственная форма.
Источники создания ЛС:
а) натуральное сырье: растения, животные, минералы, Продукты жизнедеятельности микроорганизмов {сердечные гликозиды, свиной инсулин, АБ}
б) модифицированные природные БАВ
в) продукты химического синтеза ( методы: фармакологический скрининг, молекулярное конструирование, воспроизведение биогенных аминов, целенаправленная модификация молекул с уже известной активностью, синтез фармакологически активных метаболитов, случайные находки («серендипитный» метод))
г) продукты генной инженерии {рекомбинантный инсулин, интерфероны}
Этапы создания ЛС:
1. Синтез ЛС в химической лаборатории
2. Доклиническая оценка активности и нежелательных эффектов ЛС Минздравов и др. организмациями
3. Клинические испытания ЛС Экспертиза документации Фармакологическим комитетом проводится после завершения каждой фазы. Лекарство может быть отозвано на любом этапе. (I фаза – оценка переносимости на здоровых добровольцах 20-25 лет, II фаза – на больных добровольцах численностью менее 100 человек, страдающих определенным заболеванием, III фаза - мультицентровые клинические исследования на больших группах людей (до 1000 человек), IV фаза – мониторинг препарата на протяжении 5 лет после его официального разрешения (выполняют на большом числе пациентов (не менее 1.000-5.000 человек). После завершения III фазы клинических испытаний документация вновь поступает в Фармакологический комитет (объем полного досье может составлять до 1 млн. страниц) и в течение 1-2 лет регистрируется в Государственном реестре лекарственных средств и изделий медицинского назначения. Только после этого фармакологический концерн имеет право начать промышленный выпуск лекарственного средства и его распространение через аптечную сеть.
Лекарство-генерик – это непанентованный лекарственный препарат, являющийся воспризведением оригинального препарата, на действующее вещество которого истек срок патентной защиты. Может отличаться от оригинального препарата по составу вспомогательных веществ. Необходимое требование для продажи генериков – доказательная фармацевтическая, биологическая и терапевтическая эквивалентность исходному препарату. Генериковые лекарства всегда дешевле их брендовых аналогов, т.к. фирма не тратит средства на 10-15 летние исследования лекарства, а пользуется готовыми данными
Плацебо – любой компонент терапии, не оказывающий никакого специфического биологического воздействия на болезнь, являющуюся объектом лечения.
Применяется с целью контроля при оценке действия ЛС и для того, чтобы принести пользу больному без каких-либо фармакологических средств в результате только психологического воздействия (т.е. плацебо-эффекта).
Все виды лечения имеют психологический компонент, либо доставляющий удовлетворения (плацебо-эффект), либо вызывающий беспокойство (ноцебо-эффект). Пример плацебо-эффекта: быстрое улучшение у больного вирусной инфекцией при применении антибиотиков. Благоприятность плацебо-эффекта связана с психологическим воздействием на пациента. Он будет максимальным лишь при его использовании в сочетании с методами лечения, имеющими выраженный специфический эффект. Дорогостоящие вещества в качестве плацебо также способствуют достижению большего ответа.
Показания к применению плацебо:
1) слабые психические нарушения
2) психологическая поддержка пациента с неизлечимой хронической болезнью или с подозрением на тяжелый диагноз
Лекарственное средство – любое вещество или продукт, используемые, чтобы модифицировать или исследовать физиологические системы или патологические состояния для блага реципиента (по ВОЗ, 1966 г.); индивидуальные вещества, смеси веществ или композиции неизвестного состава, обладающие доказанными лечебными свойствами.
Лекарственное вещество – индивидуальное химическое соединение, используемое в качестве лекарственного средства.
Лекарственная форма – удобная для практического применения форма, придаваемая лекарственному средству для получения необходимого лечебного или профилактического эффекта.
Лекарственный препарат – лекарственное средство в определенной лекарственной форме, разрешенное органом государственного управления.
Например: лекарственным веществом является антибиотик ампициллин, лекарственным средством – ампициллина тригидрат, который может выпускаться в форме таблеток или капсул. Лекарственным препаратом являются таблетки ампициллина тригидрата по 0,25 г.
Пути введения лекарств в организм и их характеристика. Пресистемная элиминация лекарств.
а. энтеральный путь введения: перорально, сублингвально, трансбуккально, ректально, через зонд б. парентеральный путь введения: внутривенно, подкожно, внутримышечно,… 2. Для местного воздействия: накожно (эпикутарно), на слизистые, в полости (брюшную, плевральную, суставную), в ткани…Перенос лекарств через биологические барьеры и его разновидности. Основные факторы, влияющие на перенос лекарств в организме.
1) Фильтрация (водная диффузия) – пассивное перемещение молекул вещества по градиенту концентрации через заполненные водой поры в мембране каждой… 2) Пассивная диффузия (липидная диффузия) - основной механизм переноса ЛВ,… 3) Транспорт при помощи специфических переносчиков – перенос ЛВ при помощи встроенных в мембрану переносчиков (чаще…Перенос через мембраны лекарственных веществ с переменной ионизацией (уравнение ионизации Гендерсона-Гассельбальха). Принципы управления переносом.
Все ЛС - слабые кислоты или слабые основания, имеющие свои значения константы ионизации (рК). Если значение рН среды равно значению рК лекарства, то 50% его молекул будет находится в ионизированном и 50% в неионизированном состоянии и среда для лекарства будет нейтральной.
В кислой среде (рН меньше рК), там где имеется избыток протонов, слабая кислота будет находиться в недиссоциированной форме (R-COOH), т.е. будет связана с протоном – протонирована. Такая форма кислоты незаряжена и хорошо растворима в липидах. Если рН сместиться в щелочную сторону (т.е. рН станет больше рК), то кислота начнет диссоциировать и лишится протона, перейдя при этом в непротонированную форму, которая имеет заряд и плохо растворима в липидах.
В щелочной среде, там где имеется дефицит протонов, слабое основание будет находиться в недиссоциированной форме (R-NH2), т.е. будет непротонировано и лишено заряда. Такая форма основания хорошо растворима в липидах и быстро абсорбируется. В кислой среде имеется избыток протонов и слабое основание начнет диссоциировать, связывая при этом протоны и образуя протонированную, заряженную форму основания. Такая форма плохо растворима в липидах и слабо абсорбируется.
Следовательно, абсорбция слабых кислот протекает преимущественно в кислой среде, а слабых оснований – в щелочной.
Особенности метаболизма слабых кислот (СК):
1) желудок: СК в кислом содержимом желудка неионизирована, а в щелочной среде тонкого кишечника она будет диссоциациировать и молекулы СК приобретут заряд. Поэтому, абсорбция слабых кислот будет наиболее интенсивной в желудке.
2) в крови среда достаточно щелочная и всосавшиеся молекулы СК перейдут в ионизированную форму. Фильтр клубочков почек пропускает как ионизированные, так и неионизированные молекулы, поэтому, несмотря на заряд молекулы, СК будут выводиться в первичную мочу
3) если моча щелочная, то кислота останется в ионизированной форме, не сможет реабсорбироваться обратно в кровоток и выделится с мочой; мочи кислая, то лекарство перейдет в неионизированную форму, которая легко реабсорбируется обратно в кровь.
Особенности метаболизма слабых оснований: противоположно СК (абсорбция лучше в кишечнике; в щелочной моче подвергаются реабсорбции)
Т.о., чтобы ускорить выведение из организма слабой кислоты мочу необходимо ощелачивать, а чтобы ускорить выведение слабого основания ее необходимо подкислить (детоксикация по Попову).
Количественную зависимость процесса ионизации лекарства при различном рН среды позволяет получить уравнение Henderson-Hasselbach:
 , где pKa соответствует значению pH, при котором концентрации ионизированной и неионизированной форм находятся в равновесии.
, где pKa соответствует значению pH, при котором концентрации ионизированной и неионизированной форм находятся в равновесии.
Уравнение Гендерсона-Гассельбаха позволяет оценить степень ионизации ЛС при данном значении рН и предсказать вероятность его проникновения через клеточную мембрану.
(1)Для разбавленной кислоты, A,
HA ↔ H+ + A- , где HA – концентрация неионизированной (протонированной) формы кислоты и A- - концентрация ионизированной (непротонированной) формы.
(2) Дляслабого основания, B,
BH+ ↔ H+ + B, где BH+ - концентрация протонированной формы основания, B - концентрация непротонированной формы
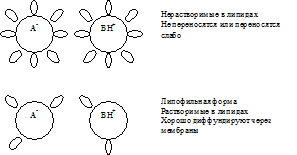
Зная рН среды и рКа вещества, можно по вычисленному логарифму определить степень ионизации лекарства, а значит, и степень его всасывания из желудочно-кишечного тракта, реабсорбции или экскреции почками при разных значениях рН мочи и т. д.
Принципы управлением переносом.
- для ускорения всасывания
Ø слабых кислот (АСК) – рН желудочного сока должен быть кислым;
Ø слабых основаный – рН желудочного сока должен быть нейтральным.
- для ускорения выведения
Ø слабых кислот – мочу подщелачивают;
Ø слабых оснований – мочу подкисляют.
Перенос лекарств в организме. Водная диффузия и диффузия в липидах (закон Фика). Активный транспорт.
Перенос ЛС в организме может осуществляться водной и липидной диффузией, активным транспортом, эндо- и пиноцитозом.
Особености перенос ЛС в организме водной диффузией:
1. Эпителиальные покровы (слизистые ЖКТ, полости рта и др.) – водная диффузия только очень малых молекул (метанол, ионы лития и т.д.)
2. Капилляры (кроме мозговых) – фильтрация веществ с молекулярной массой до 20-30 тыс. Да.
3. Капилляры мозга – в основном не имеют водных пор, за исключением областей гипофиза, эпифиза, зоны IV желудочка, хориоидного сплетения, медианного возвышения
4. Плацента – не имеет водных пор (хотя вопрос спорный).
5. Связывание ЛС с белками крови препятствует их выходу из кровяного русла, а значит, и водной диффузии
6. Диффузия в воде зависит от размеров молекул ЛС и водных пор
Особенности липидной диффузии:
1. Основной механизм переноса ЛС через клеточные мембраны
2. Определяется липофильностью диффундируемого вещества (т.е. коэффициентом распределения «масло/вода») и градиентом концентрации, может быть ограничена очень низкой растворимостью вещества в воде (что препятствует проникновению ЛС в водную фазу мембран)
3. Легко диффундируют неполярные соединения, трудно – ионы.
Любая диффузия (и водная, и в липидах) подчиняется закону диффузии Фика:
 , где
, где
Скорость диффузии – количество переносимых в единицу времени молекул лекарства; С1 - концентрация вещества снаружи мембраны;С2 - концентрация вещества изнутри мембраны.
Следствие из закона Фика:
1) фильтрация ЛС тем выше, чем больше его концентрация в месте введения {S абсорбируемой поверхности в кишечнике больше, чем в желудке, поэтому абсорбция ЛС в кишечника более быстрая}
2) фильтрация ЛС тем выше, чем больше концентрация ЛС в месте введения
3) фильтрация ЛС тем выше, чем меньше толщина преодолеваемой биологической мембраны {толщина барьера в альвеолах легких значительно меньше, чем кожи, поэтому скорость абсорбции выше в легких}
Активный транспорт – перенос ЛC независимо от градиента концентрации с использованием энергии АТФ, характерен для гидрофильных полярных молекул, ряда неорганических ионов, сахаров, аминокислот, пиримидинов.
Характеризуется: а) избирательностью к определенным соединениям б) возможностью конкуренции двух веществ за один транспортный механизм в) насыщаемостью при высоких концентрациях вещества г) возможностью транспорта против градиента концентрации д) затратой энергии.
7. Центральный постулат фармакокинетики концентрация лекарства в крови – основной параметр для управления терапевтическим эффектом. Задачи, решаемые на основании знания этого постулата.
Центральный постулат (догма) фармакокинетики: концентрация ЛВ в плазме крови детерминирует (количественно определяет) фармакологический эффект.
В большинстве случаев скорость всасывания, распределения, метаболизма и экскреции ЛС пропорциональна их концентрации в плазме крови (подчиняется закону действующих масс), поэтому зная ее возможно:
1) определить период полуэлиминации (для ЛС с кинетикой первого порядка)
2) объяснить длительность некоторых токсических эффектов ЛС (для ЛС в высоких дозах с кинетикой насыщения)
3) рассчитать загрузочную и поддерживающие дозы ЛС, необходимые для обеспечения адекватного терапевтического действия
[C]плазма→ [C]на мишени→ эффект
↓ ↓ ↓
Определяются законами определяется з-нами фармодинамики
Распределения
Задачи: научиться управлять концентрацией лекарства в крови.
Фармакокинетические модели (однокамерная и двухкамерная), количественные законы всасывания и элиминации лекарств.
Весь организм – единый однородный контейнер. Допущения: 1) устанавливается быстрое динамическое развитие между содержанием препарата в… 2) ЛС быстро и равномерно распределяется по всему объему кровиРаспределение лекарств в организме. Отсеки, лиганды. Основные детерминанты распределения.
Отсеки распределения: 1. Внеклеточное пространство (плазма, межклеточная жидкость) 2. Клетки (цитоплазма, мембрана органелл)Константа элиминации, ее сущность, размерность, связь с другими фармакокинетическими параметрами.
Константа скорости элиминации (kel, мин-1) – показывает, какая часть ЛС элиминируется из организма в единицу времени Þ Kel = Aвыд/Аобщ, где Авыд – количество ЛС, выделяемое в ед. времени, Аобщ – общее количество ЛС в организме.
Значение kel обычно находят путем решения фармакокинетического уравнения, описывающего процесс элиминации лекарства из крови, поэтому kel называют модельным показателем кинетики. Непосредственного отношения к планированию режима дозирования kel не имеет, но ее значение используют для расчета других фармакокинетических параметров.
Константа элиминации прямо пропорциональна клиренсу и обратно пропорционально объему распределения (из определения клиренса): Kel=CL/Vd; [Ke] = час-1/мин-1=доля в час.
Период полувыведения лекарств, его сущность, размерность, взаимосвязь с другими фармакокинетическими параметрами.
Период полуэлиминации (t½, мин) – это время, необходимое для снижения концентрации ЛС в крови ровно наполовину. При этом не играет роли каким путем достигается снижение концентрации – при помощи биотрансформации, экскреции или же за счет сочетания обоих процессов.
Период полуэлиминации определяют по формуле:
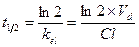
Период полувыведения – важнейший фармакокинетический параметр, позволяющий:
а) рассчитать время наступления равновесной концентрации (равно 5 периодам полуэлиминации)
б) определить время полной элиминации препарата
в) предсказать концентрацию ЛС в любой момент времени (для ЛС с кинетикой первого порядка)
Клиренс как главный параметр фармакокинетики для управления режимом дозирования. Его сущность, размерность и связь с другими фармакокинетическими показателями.
Клиренс (Cl, мл/мин) - объем крови, который очищается от ЛС за единицу времени.
Т.к. плазма (кровь) - «видимая» часть объема распределения, то клиренс – фракция объема распределения, из которой лекарство выделяется в единицу времени. Если обозначить общее количество лекарства в организме через Аобщ, а количество, которое выделилось через Авыд, то :
 С другой стороны, из определения объема распределения следует, что общее количество лекарства в организме составляет Аобщ=Vd´Cтер/плазма. Подставляя это значение в формулу клиренса, мы получим:
С другой стороны, из определения объема распределения следует, что общее количество лекарства в организме составляет Аобщ=Vd´Cтер/плазма. Подставляя это значение в формулу клиренса, мы получим:
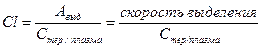 .
.
Таким образом, клиренс – отношение скорости выведения лекарственного средства к его концентрации в плазме крови.
В таком виде формулу клиренса используют для расчета поддерживающей дозы лекарства (Dп), т.е той дозы лекарственного средства, которая должна скомпенсировать потерю лекарства и поддержать его уровень на постоянном уровне:
Скорость введения = скорость выведения = Cl´Cтер (доза/мин)
Dп = скорость введения´t (t - интервал, между приемом лекарства)
Клиренс аддитивен, т.е. элиминация вещества из организма может происходить с участием процессов, идущих в почках, легких, печени и других органах: Clсистемный = Clпочечн. + Clпечени + Clдр.
Клиренс связан с периодом полуэлиминации ЛС и объемом распределения: t1/2=0,7*Vd/Cl.
Доза. Виды доз. Единицы дозирования лекарственных средств. Цели дозирования лекарств, способы и варианты введения, интервал введения.
Действие ЛС на организм в большей степени определяется их дозой.
Доза - количество вещества, введенное в организм за один прием; выражается в весовых, объемных или условных (биологических) единицах.
Виды доз:
а) разовая доза – количество вещества на один прием
б) суточная доза - количество препарата, назначаемое на сутки в один или несколько приемов
в) курсовая доза - общее количество препарата на курс лечения
г) терапевтические дозы - дозы, в которых препарат используют с лечебными или профилактическими целями (пороговые, или минимальные действующие, средние терапевтические и высшие терапевтические дозы).
д) токсические и смертельные дозы – дозы ЛВ, при которых они начинают оказывать выраженные токсические эффекты или вызывать смерть организма.
е) загрузочная (вводная) доза – кол-во вводимого ЛС, которое заполняет весь объем распределения организма в действующей (терапевтической) концентрации: ВД = (Css * Vd)/F
ж) поддерживающая доза – систематически вводимое количество ЛС, которое компенсирует потери ЛС с клиренсом: ПД = (Css * Cl * DT)/F
Единицы дозирования ЛС:
1) в граммах или долях грамма ЛС
2) количество ЛС в расчете на 1 кг массы тела (например, 1 мг/кг) или на единицу поверхности тела (например, 1 мг/м2)
Цели дозирования ЛС:
1) определить количество ЛС, необходимое для того, чтобы вызвать нужный терапевтический эффект с определенной длительностью
2) избежать явлений интоксикации и побочных эффектов при введении ЛС
Способы введения ЛС: 1) энтерально 2) парентерально (см. в. 5)
Варианты введения ЛС:
а) непрерывный (путем длительных внутрисосудистых инфузий ЛС капельно или через автоматические дозаторы). При непрерывном введении ЛС его концентрация в организме изменяется плавно и не подвергается значительным колебаниям
б) прерывистое введение (инъекционным или неинъекционным способами) - введение лекарства через определенные промежутки времени (интервалы дозирования). При прерывистом введении ЛС его концентрация в организме непрерывно колеблется. После приема определенной дозы она вначале повышается, а затем постепенно снижается, достигая минимальных значений перед очередным введением лекарства. Колебания концентрации тем значительнее, чем больше вводимая доза лекарства и интервал между введениями.
Интервал введения – интервал между вводимыми дозами, обеспечивающий поддержание терапевтической концентрации вещества в крови.
15. Введение лекарств с постоянной скоростью. Кинетика концентрации препарата в крови. Стационарная концентрация препарата в крови (Css), время ее достижения, расчет и управление ею.
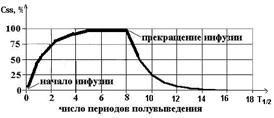 Особенность введения ЛС с постоянной скоростью - плавное изменение его концентрации в крови при введении, при этом:
Особенность введения ЛС с постоянной скоростью - плавное изменение его концентрации в крови при введении, при этом:
1) время достижения стационарной концентрации лекарства составляет 4-5t½ и не зависит от скорости инфузии (величины вводимой дозы)
2) при увеличении скорости инфузии (вводимой дозы) величина СSS также увеличивается в пропорциональное число раз
3) элиминация лекарства из организма после прекращения инфузии занимает 4-5t½.
Сss – равновесная стационарная концентрация – концентрация ЛС, достигаемая при скорости введения равной скорости выведения, поэтому:

 (из определения клиренса)
(из определения клиренса)
За каждый последующий период полувыведения концентрация ЛС прирастает на половину от оставшейся концентрации. Все ЛС, подчиняющиеся закону элиминации первого порядка, будут достигать Css через 4-5 периодов полувыведения.
Подходы к управлению уровнем Сss: изменить вводимую дозу ЛС или интервал введения
16. Прерывистое введение лекарств. Кинетика концентрации препарата в крови, терапевтический и токсический диапазон концентраций. Расчет стационарной концентрации (C ss), границ ее колебаний и управление ею. Адекватный интервал введения дискретных доз.
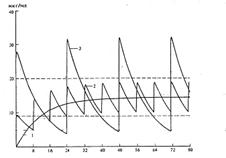 Колебания концентрации ЛС в плазме крови: 1 - при постоянном внутривенном капельном введении; 2 —при дробном введении той же суточной дозы с интервалом 8 ч;3 — при введении суточной дозы с интервалом 24 ч.
Колебания концентрации ЛС в плазме крови: 1 - при постоянном внутривенном капельном введении; 2 —при дробном введении той же суточной дозы с интервалом 8 ч;3 — при введении суточной дозы с интервалом 24 ч.
Прерывистое введение ЛС – введение определенного количества ЛС через некоторые промежутки времени.
Равновесная стационарная концентрация достигается через 4-5 периодов полуэлиминации, время ее достижения не зависит от дозы (в начале, когда уровень концентрации ЛС невысок, скорость его элиминации также невысока; по мере увеличения количества вещества в организме нарастает и скорость его элиминации, поэтому рано или поздно наступит такой момент, когда возросшая скорость элиминации уравновесит вводимую дозу ЛС и дальнейший рост концентрации прекратиться)
 ,Css прямо пропорциональна дозе ЛС и обратно пропорциональна интервалу введения и клиренсу ЛС.
,Css прямо пропорциональна дозе ЛС и обратно пропорциональна интервалу введения и клиренсу ЛС.
Границы колебаний Css: 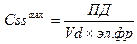 ; Cssmin = Cssmax × (1 – эл. фр.). Колебания концентрации ЛС пропорциональны
; Cssmin = Cssmax × (1 – эл. фр.). Колебания концентрации ЛС пропорциональны  T/t1/2.
T/t1/2.
Терапевтический диапазон (коридор безопасности, терапевтическое окно) – это интервал концентраций от минимальной терапевтической до вызывающей появление первых признаков побочных действий.
Токсический диапазон – интервал концентрации от высшей терапевтической до смертельной.
t
Адекватный режим введения дискретных доз: такой режим введения, при котором флюктуация концентрации препарата в крови укладывается в терапевтический диапазон. Для определения адекватного режима введения ЛС необходимо рассчитать. Разница между Cssmax и Cssmin при этом не должна превысить 2Css.
Управление колебаниями Css:
Размах колебаний Css прямо пропорционален дозе ЛС и обратно пропорционален интервалу его введения.
1. Изменить дозу ЛС: при увеличении дозы ЛС диапазон колебаний его Css пропорционально увеличивается
2. Изменить интервал введения ЛС: при увеличении интервала введения ЛС диапазон колебаний его Css пропорционально уменьшается
Одновременно изменить дозу и интервал введения
Вводная (загрузочная) доза. Терапевтический смысл, расчет по фармакокинетическим параметрам, условия и ограничения ее использования.
Вводная (загрузочная) доза – доза, вводимая за один прием и заполняющая весь объем распределения в действующей терапевтической концентрации. ВД=(Css*Vd)/F ; [Css]=мг/л, [Vd]=л/кг
Терапевтический смысл: вводная доза быстро обеспечивает действующую терапевтическую концентрацию ЛС в крови, что позволяет, например, быстро купировать приступ БА, аритмии и т.д.
Вводная доза может быть введена за один раз лишь тогда, когда игнорируется процесс распределения вещества
Ограничение использования ВД: если распределение ЛС происходит значительно медленнее, чем его поступление в кровь, введение сразу всей загрузочной дозы (особенно внутривенно) создаст концентрацию значительно выше терапевтической и обусловит возникновение токсических эффектов. Условие использования ВД: поэтому введение нагрузочных доз всегда должно быть медленным или дробным.
Поддерживающие дозы, их терапевтический смысл и расчет для оптимального режима дозирования.
Терапевтический смысл: ПД компенсирует потери с клиренсом за интервал между введениями препарата. Расчет для оптимального дозирования ЛС (для быстрого купирования приступа): … 1. Рассчитываем ВД: ВД=(Css*Vd)/FИндивидуальные, возрастные и половые различия фармакокинетики лекарств. Поправки для расчета индивидуальных значений объема распределения лекарств.
2. Половые различия в действии лекарств. Для женщин характерна меньшая масса тела, чем для мужчин, поэтому и величина доз лекарства для них должна… 3. Патологические состояния организма и действие лекарств а) заболевания печени: F ЛС из-за выключения пресистемного метаболизма, фракция несвязанного ЛС из-за недостатка…Почечный клиренс лекарств, механизмы, их количественные и качественные характеристики.
Механизмы почечного клиренса и их характеристика: 1. Фильтрация: ЛС, выделяемоетолько фильтрацией {инсулин} будет иметь клиренс,… Определяется: почечным кровотоком, несвязанной фракцией ЛС и фильтрационной способностью почек.Факторы, влияющие на почечный клиренс лекарств. Зависимость клиренса от физико-химических свойств лекарственных средств.
а) гломерулярная фильтрация б) скорость почечного кровотока в) максимальная скорость секрецииПеченочный клиренс лекарств, его детерминанты и ограничения. Энтерогепатический цикл лекарственных средств.
1) метаболизм (биотрансформация) путем окисления, восстановления, алкилирования, гидролиза, коньюгации и т.д. Основная стратегия метаболизма ксенобиотиков: неполярные вещества ® полярные… 2) секреция (выведение нетрансформированных веществ в желчь)Коррекция лекарственной терапии при поражении печени и других патологических состояниях.
Коррекцию режима дозирования при заболевании почек см. выше в в.26, общие принципы коррекции – в.25. Коррекция режима дозирования под контролем общего клиренса препарата: Коррекция дозы: Динд.=Дтипичн.×Clинд./Clтипичн.Коррекция режима дозирования под контролем остаточной функции почек.
Нам известно: а) остаточная функция почек, определяющаяся клиренсом креатинина у данного… б) общий клиренс данного ЛС (СlЛС/общий) и доля почечного клиренса ЛС в общем клиренсеСтратегия индивидуальной лекарственной терапии.
Признание важной роли концентрации как связующего звена фармакокинетики и фармакодинамики способствует созданию стратегии целевой концентрации - оптимизации дозы у данного больного на основе измерения концентрации ЛС. Она складывается из следующих этапов:
1. Выбор целевой концентрации
2. Расчет Vd и Cl на основе типовых значений и внесения поправок с учетом таких факторов как масса тела и функция почек.
3. Ввод загрузочной дозы или поддерживающей дозы, рассчитанных с учетом значений TC, Vd и Cl.
4. Регистрация реакции больного и определение концентрации ЛС
5. Пересмотр Vd и Cl на основе результатов измерения концентрации.
6. Повтор шагов 3-6 с целью подбора необходимой для оптимальной реакции на лекарство поддерживающей дозы.
Биотрансформация лекарственных средств, ее биологический смысл, основная направленность и влияние на активность лекарств. Основные фазы метаболических превращений лекарств в организме.
Биотрансформация ЛС – химические превращения ЛС в организме.
Биологический смысл биотрансформации ЛС: создание субстрата, удобного для последующей утилизации (в качестве энергетического или пластического материала) или в ускорении выведения ЛС из организма.
Основная направленность метаболических превращений ЛС: неполярные ЛС → полярные (гидрофильные) метаболиты, выводимые с мочой.
Выделяют две фазы метаболических реакций ЛС:
1) метаболическая трансформация (несинтетические реакции, фаза 1) - превращение веществ за счет микросомального и внемикросомального окисления, восстановления и гидролиза
2) конъюгация (синтетические реакции, фаза 2) - биосинтетический процесс, сопровождающийся присоединением к лекарственному веществу или его метаболитам ряда химических группировок или молекул эндогенных соединений путем а) образования глюкуронидов б) эфиров глицерина в) сульфоэфиров г) ацетилирования д) метилирования
Влияние биотрансформации на фармакологическую активность ЛС:
1) чаще всего метаболиты биотрансформации не обладают фармакологической активностью или их активность снижена по сравнению с исходным веществом
2) в некоторых случаях метаболиты могут сохранять активность и даже превосходить по активности исходное вещество (кодеин метаболизируется до более фармакологически активного морфина)
3) иногда в ходе биотрансформации образуются токсичные вещества (метаболиты изониазида, лидокаина)
4) иногда в ходе биотрансформации образуются метаболиты с противоположными фармакологическими свойствами (метаболиты неселективных агонистов b2- адренорецепторов обладают свойствами блокаторов этих рецепторов)
5) ряд веществ является пролекарствами, которые исходно не дают фармакологических эффектов, но в ходе биотрансформации преобразуются в БАВ (неактивная L-допа, проникая через ГЭБ, превращается в мозге в активный дофамин, при этом нет системных эффектов дофамина).
Клиническое значение биотрансформации лекарств. Факторы,влияющие на их бтотрансформацию. Метаболическое взаимодействие лекарств.
Влияние на биотрансформацию ЛС различных факторов: а) функциональное состояние печени: при ее заболеваниях клиренс ЛС обычно… б) влияние факторов среды: курение способствует индукции цитохрома P450, в результате чего ускоряется метаболизм ЛС в…Пути и механизмы выведения лекарств из организма. Возможности управления выведением лекарств.
Пути и механизмы выведения ЛС: элиминация ЛС печенью и почками и некоторыми другими органами:
а) почками путем фильтрации, секреции, реабсорбции
б) печенью путем биотрансформации, экскреции с желчью
в) через легкие, слюну, пот, молоко и т.д. путем секреции, испарения
Возможности управления процессами выведения ЛС:
1. управление pH: в щелочной моче повышается выведение кислых соединений, в кислой – выведение основных соединений
2. применение желчегонных препаратов (холензим, аллохол)
3. гемодиализ, перитонеальный диализ, гемосорбция, лимфосорбция
4. форсированный диурез (в/в NaCl или глюкоза для водной нагрузки + фуросемид или маннитол)
5. промывание желудка, применение клизм
Концепция рецепторов в фармакологии, молекулярная природа рецепторов, сигнальные механизмы действия лекарств (типы трансмембранной сигнализации и вторичные посредники).
Рецепторы – молекулярные компоненты клетки или организма, которые взаимодействуют с ЛС и индуцируют ряд биохимических событий, ведущих к развитию фармакологического эффекта.
Концепция рецепторов в фармакологии:
1. Рецепторы детерминируют количественные закономерности действия ЛС
2. Рецепторы ответственны за селективность действия ЛС
3. Рецепторы посредники действия фармакологических антагонистов
Концепция рецепторов - основа целенаправленного применения лекарственных средств, влияющих на регуляторные, биохимические процессы и коммуникации.
Молекулярная природа рецепторов:
1. регуляторные белки, посредники действия различных химических сигналов: нейромедиаторов, гормонов, аутокоидов
2. ферменты и трансмембранные белки переносчики (Na+, K+ АТФаза)
3. структурные белки (тубулин, белки цитоскелета, клеточная поверхность)
4. ядерные белки и нуклеиновые кислоты
Сигнальные механизмы действия лекарств:
1) проникновение растворимых в липидах лигандов через мембрану и их действие на внутриклеточные рецепторы.
2) сигнальная молекула связывается с внеклеточным доменом трансмембранного белка и активирует ферментативную активность его цитоплазматического домена.
3) сигнальная молекула связывается с ионным каналом и регулирует его открытие.
4) сигнальная молекула связывается с рецептором на поверхности клетки, который сопряжен с эффекторным ферментом посредством G-белка. G-белок активирует вторичный посредник.
Типы трансмембранной сигнализации:
а) через 1-TMS-рецепторы, обладающие и не обладающие тирозинкиназной активностью
б) через 7-ТMS-рецепторы, связанные с G-белком
в) через ионные каналы (лиганд-зависимые, потенциал-зависимые, щелевые контакты)
Вторичные посредники: цАМФ, ионы Ca2+, ДАГ, ИФ3.
Физико-химические и химические механизмы действия лекарственных веществ.
Основные фармакологические эффекты: 1) наркотическое 2) обще депрессивное 3) парализующее 4) местно раздражающее 5) мембранолитическое действия. Химическая природа веществ: химически инертные углеводороды, эфиры, спирты,… Механизм действия – обратимое деструирование мембран.Селективность и специфичность действия лекарств. Терапевтические, побочные и токсические эффекты лекарств, их природа с позиций концепции рецепторов. Терапевтическая стратегия борьбы с побочными и токсическими эффектами лекарств.
Специфичность –связывание ЛС со строго специфичным ему типом рецептора.
Селективность - способно связываться ЛС с одним или несколькими типами рецепторов более точно, чем с другими.
Более предпочтительно использовать термин селективность, т.к. маловероятно, что любая молекула ЛС может связаться только с одним типом рецепторных молекул, поскольку число потенциальных рецепторов у каждого пациента имеет астрономическое значение.
Терапевтическое действие — основной желательный фармакологический эффект, ожидаемый от данного фармакологического препарата.
Побочные эффекты– те эффекты, которые возникают при применении веществ в терапевтических дозах и составляют спектр их фармакологического действия.
Токсические эффекты – нежелательные эффекты, проявляющиеся у данного ЛС при выходе из терапевтического диапазона.
Связи терапевтического и токсического эффектов ЛС на основе анализа рецепторно-эффекторных механизмов:
1) терапевтический и токсический эффекты, опосредуемые одним и тем же рецепторно-эффекторным механизмом {празозин действует как альфа-селективный антагонист на рецепторы ГМК сосудов и оказывает гипотензивное действие при эссенциальной гипертензии, но при его большой дозе у больного может возникнуть постуральная гипотензия}
2) терапевтический и токсический эффекты, опосредуемые идентичными рецепторами, но различными тканями или различными эффекторными путями {сердечные гликозиды используют для увеличения сократительной способности миокарда, в тоже время они нарушают функцию ЖКТ, зрения за счет блокады Na+/K+-АТФазы клеточной мембраны}
3) терапевтический и токсический эффекты, опосредуемый различными типами рецепторов {например, норадреналин оказывает гипертензивное действие через a1-Ар, но при этом вызывает тахикардию через b1-Ар}
Терапевтическая стратегия борьбы с терапевтическими и побочными эффектами ЛС:
1. ЛС всегда следует вводить в наименьшей дозе, которая вызывает приемлемый терапевтический эффект
2. Снижение дозы одного ЛС за счет назначения другого ЛС со сходным действием, но через иные рецепторы и с иным профилем токсичности.
3. Селективность действия ЛС может быть увеличена путем управления концентрацией ЛС в районе рецепторов различных отделов организма (местное применение ЛС – ингаляционное применение сальбутамола при бронхиальной астме)
32. Термины и понятия количественной фармакологии: эффект, эффективность, активность, агонист (полный, частичный), антагонист. Клиническое различие понятий активность и эффективность лекарств.
 Эффект (ответ) – количественный выход реакции взаимодействия клетки, органа, системы или организма с фармакологическим агентом.
Эффект (ответ) – количественный выход реакции взаимодействия клетки, органа, системы или организма с фармакологическим агентом.
Эффективность – мера реакции по оси эффекта – величина отклика биологической системы на фармакологическое воздействие; это способность ЛС оказывать максимально возможное для него действие. Т.е. фактически это максимальная величина эффекта, которую можно достигнуть при введении данного лекарства. Численно характеризуется величиной Еmax. Чем выше Еmax, тем выше эффективность лекарства
Активность – мера чувствительности к ЛС по оси концентраций, характеризует аффинность (сродство лиганда к рецептору), показывает, какая доза (концентрация) ЛС способна вызвать развитие стандартного эффекта, равного 50% от максимально возможного для этого лекарства. Численно характеризуется величиной ЕС50 или ED50. Чем выше активность ЛС, тем меньшая его доза требуется для воспроизведения терапевтического эффекта.
Эффективность: 1=2>3
Активность: 1>3>2
В клинической деятельности важнее знать эффективность, а не активность, т.к. нас больше интересует способность ЛС вызывать определенное действие в организме.
Агонист – лиганд, который связывается с рецептором и вызывает биологическую реакция, срабатывание физиологической системы. Полный агонист – максимальный отклик, частичный – вызывают меньшую реакцию даже при оккупации всех рецепторов.
 Антагонист - лиганды занимающие рецепторы или изменяющие их таким образом, что они утрачивают способность взаимодействовать с другими лигандами, но сами не вызывающие биологической реакции (блокируют действие агонистов).
Антагонист - лиганды занимающие рецепторы или изменяющие их таким образом, что они утрачивают способность взаимодействовать с другими лигандами, но сами не вызывающие биологической реакции (блокируют действие агонистов).
Конкурентные антагонисты - взаимодействуют с рецепторами обратимо и тем самым конкурируют с агонистами. Увеличение концентрации агониста может полностью устранить эффект антагониста. Конкурентный антагонист сдвигает кривую «доза-эффект» для агониста, увеличивает EC50, не влияет на Emax.
Неконкурентные антагонисты - необратимо изменяют сродство рецепторов к агонисту, связывание часто происходит не с активным участком рецептора, увеличение концентрации агониста не устраняет действие антагониста. Неконкурентный антагонист снижает Emax, не изменяет EC50, кривая «доза-эффект» сжимается относительно вертикальной оси.
33. Количественные закономерности действия лекарств. Закон уменьшения отклика биологических систем. Модель Кларка и ее следствия. Общий вид зависимости концентрация – эффект в нормальных и логнормальных координатах.
Модель Кларка-Ариенса:
1. Взаимодействие между лигандом (L) и рецептором (R) обратимы.
2. Все рецепторы для данного лиганда – эквивалентны и независимы (их насыщение не влияет на другие рецепторы).
3. Эффект прямо пропорционален числу занятых рецепторов.
4. Лиганд существует в двух состояниях: свободном и связанном с рецептором.
А)  , где Kd – константа равновесия, Ke – внутренняя активность.
, где Kd – константа равновесия, Ke – внутренняя активность.
Б) Т.к. при возрастании количества лигандов в какой-то момент времени все рецепторы окажутся заняты, то максимально возможное количество образованных комплексов лиганд-рецептор описывается формулой:
[RL] = [R] × 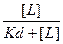 (1)
(1)
Эффект определяется вероятностью активации рецептора при связывании с лигандом, т.е. его внутренней активностью (Ке), поэтому E = Ke×[RL]. При этом эффект максимален при Ке=1 и минимален и Ке=0. Естественно, что максимальный эффект описывается соотношением Emax = Ke×[Rобщий], где [Rобщий] – общее число рецепторов для данного лиганда
Эффект зависит и от концентрации лиганда на рецепторах [С], поэтому
E = Emax  (2)
(2)
Из приведенных соотношений вытекает, что EC50=Kd
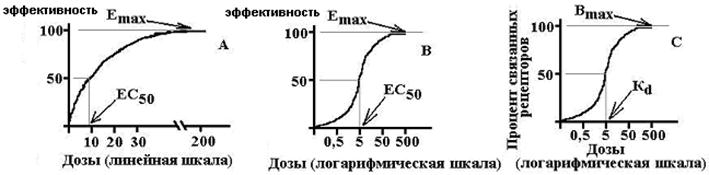
Emax – максимальный эффект, Bmax – максимальное число связанных рецепторов, EC50 – концентрация ЛС, при которой возникает эффект, равный половине от максимального, Kd – константа диссоциации вещества от рецептора, при которой связано 50% рецепторов.
Закону убывания откликасоответствует параболическая зависимость «концентрация – эффективность». Ответ на малые дозы ЛС обычно возрастает прямо пропорционально дозе. Однако при увеличении дозы прирост ответной реакции снижается и в конечном счете может быть достигнута доза, при которой не происходит дальнейшего увеличения ответа (за счет оккупации всех рецепторов для данного лиганда).
Градуальная и квантовая оценка эффекта, сущность и клинические приложения. Количественная оценка активности и эффективности лекарств в экспериментальной и клинической практике.
Все фармакологические эффекты можно условно разделить на две категории:
а) градуальные (непрерывные, интегральные) эффекты – такие эффекты ЛС, которые могут быть измерены количественно ( действие гипотензивных ЛС – по уровню АД). Описываются градуальной «кривой доза-эффект» (см. в. 33), на основе которой можно оценить: 1) индивидуальную чувствительность к ЛС; 2) активность ЛС; 3) максимальную эффективность ЛС.
б) квантовые эффекты – такие эффекты ЛС, которые являются дискретной величиной, качественным признаком, т.е. описываются всего лишь несколькими вариантами состояний (головная боль после приема анальгетика или есть, или нет). Описывается квантовой кривой доза-эффект, где отмечают зависимость проявления эффекта в популяции от величины принимаемой дозы ЛС. График зависимости доза-эффект при этом имеет куполообразный вид и идентичен Гауссовой кривой нормального распределения. На основе квантовой кривой можно : 1) оценить популяционную чувствительность ЛС; 2) отметить наличие эффекта при данной дозе; 3) выбрать среднюю терапевтическую дозу.
Различия между градуальной и квантовой характеристикой «доза-эффект»:
| Параметр | Градуальная кривая | Квантовая кривая |
| Характер эффекта | Количественный | Качественный |
| Возможность построения | У индивидуума | В популяции |
| Сила ЛС | Определяется величиной EC50 (ED50) | Определяется величиной EC50 (ED50) |
| Эффективность | Определяется величиной Emax | Не может быть определена без специального анализа |
| Вид кривой | Экспоненциальная зависимость (S-образная в полулогарифмических координатах) | Кривая Гауссова распределения |
Количественная оценка активности и эффективности ЛС проводится на основе построения кривых «доза-эффект» и их последующей оценке (см. в.32)
Виды действия лекарственных средств. Изменение действия лекарств при их повторном применении.
1. По локализации: · местное – действие, возникающее на месте приложения ЛС (обычно кожа и… · резорбтивное – это действие, которое ЛС оказывает, когда всасывается в кровоток или непосредственно вводится в…Зависимость действия лекарств от возраста, пола и индивидуальных способностей организма. Значение суточных ритмов.
· дети – область фармакологии, занимающаяся изучением особенностей действия ЛС на детский организм, называется педиатрическая фармакология.… · пожилые люди – в пожилом и старческом возрасте фармакокинетические… 2. Пол – эксперименты на животных и клинические наблюдения свидетельствуют, что существуют половые различия в…Вариабельность и изменчивость действия лекарств. Гипо- и гиперреактивность, толерантность и тахифилаксия, гиперчувствительность и идиосинкразия. Причины вариабельности действия лекарств и рациональная стратегия терапии.
Вариабельность действия ЛС – отражает различие фармакологических эффектов одного ЛС у разных индивидуумов.
Изменчивость действия ЛС – отражает способность ЛС оказывать действие, которое отличается от его типичных фармакологических эффектов.
Варианты вариабельности и изменчивости действия ЛС:
1. Гипореактивность – снижение эффекта данной дозы ЛС по сравнению с тем эффектом, который наблюдается у большинства больных.
2. Гиперреактивность - повышение эффекта данной дозы ЛС по сравнению с тем эффектом, который наблюдается у большинства больных.
3. Толерантность - снижение ответной реакции организма на повторные введения ЛС; для того, чтобы восстановить реакцию на ЛС, его приходится вводить во все бóльших и бóльших дозах.
4. Тахифилаксия – состояние, при котором частое введение ЛС вызывает развитие толерантности уже через несколько часов, но при достаточно редких введения ЛС его эффект сохраняется в полной мере. Развитие тахифилаксии обычно связано с истощением эффекторных систем.
5. Гиперчувствительность – развитие аллергической или другой иммунной реакции на повторное введение ЛС.
6. Идиосинкразия – извращенная реакция организма на ЛС, связанное с генетическими особенностями метаболизма ЛС или индивидуальной иммунологической реактивностью.
Основные причины вариабельности действия ЛС:
1) изменение концентрации вещества в зоне рецептора – из-за различий в скорости всасывания, его распределения, метаболизма, элиминации
2) вариации в концентрации эндогенного лиганда - рецептора – пропранолол (β-адреноблокатор) замедляет ЧСС у людей с повышенным уровнем катехоламинов в крови, но не влияет на фоновую ЧСС у спортсменов.
3) изменение плотности или функции рецепторов.
4) изменение компонентов реакции, расположенных дистальнее рецептора.
Рациональная стратегия терапии: состоит в том, что для назначения ЛС и для того, чтобы оно оказало ожидаемый эффект, необходимо учитывать индивидуальные факторы организма (возраст, пол и др.), суточные ритмы человека, наличие у него хронических заболеваний и других отклонений. Также необходимо прогнозировать развитие нехарактерных эффектов, учитывая все возможные варианты изменчивости действия ЛС.
Оценка безопасности лекарств. Терапевтический индекс и стандартные границы безопасности.
На создание и внедрение нового ЛС затрачиваются огромные средства – от 100 до 350 млн долларов и более. Эти расходы включают труд, затраченный на… Для того, чтобы пройти все этапы оценки ЛС должно соответствовать основному… Оценка безопасности новых ЛС проводится в 2 этапа:Фармакокинетическое взаимодействия лекарственных средств (примеры).
Фармакокинетическое взаимодействие ЛС является разновидностью фармакологического взаимодействия, т.е. взаимодействие лекарств, которое проявляется только при их совместном поступлении в организм человека.
Фармакокинетическое взаимодействие осуществляется на этапе всасывания, распределения и депонирования, метаболизма и выведения.
1. На этапе всасывания – этот вид взаимодействия может приводить к увеличению или уменьшению их всасывания. Его можно избежать, если делать интервал между приемами ЛС не менее 4 часов.
При введении препарата per os его всасывание детерминируют:
· рН среды – неионизированные ЛС всасываются в ЖКТ лучше ионизированных, поэтому повышение рН желудочного сока повышает всасывание слабых оснований и снижает всасывание слабых кислот. Пример: антациды, блокаторы Н2-гистаминовых рецепторов тормозят всасывание кетоконазола и др. противогрибковых препаратов, непрямых антикоагулянтов, ацетилсалициловой кислоты, барбитуратов (почти полностью предотвращают их снотворное действие); повышение рН среды улучшает всасывание глибутида, ускоряет растворение оболочки кишечно-растворимых веществ.
· прямое взаимодействие в ЖКТ – образование хелатных комплексов и соединений, не всасывающихся в ЖКТ. Примеры: активированный уголь образует нерастворимые соединения с ЛС, предотвращая их всасывание при отравлении; тетрациклины взаимодействуют с кальцием, аллюминием, железом, магнием с образованием хелатных комплексов, поэтому их всасывание снижается при применении антацидов, препаратов висмута; фторхинолоны + антациды или сукралфат = снижение эффективности антибактериальной терапии.
· моторика ЖКТ – может вызывать либо ускорение, либо замедление всасывания ЛС. Примеры: прокинетики (метоклопромид) ускоряют всасывание быстро всасывающихся ЛС ( этанол, парацетамол, тетрациклин) и замедляют у медленно всасывающихся ( дигоксин, циметидин); слабительные средства снижают всасывание и биодоступность ЛС; при приеме антихолинергических ЛС, блокаторов Н2-гистаминовых рецепторов (удлинение времени прохождения ЛС по ЖКТ) повышается биодоступность и всасывание сердечных гликозидов, препаратов железа, что может привести в проявлению токсических эффектов.
· кишечная микрофлора – она принимает непосредственное участие во всасывании ЛС, поэтому любой дисбактериоз проявляется нарушениями всасывания ЛС. Примеры: дигоксин + эритромицин = повышение концентрации дигоксина в крови и развитие нежелательных эффектов; пероральные конрацептивы + АБ широкого спектра = снижение эффекта контрецепции
· повреждение СО кишечника – тормозит всасывание некоторых ЛС. Примеры: цитостатики (циклофосфамид) тормозят всасывание дигоксина; нарушение всасывания препаратов железа, цианокобаламина, фолиевой кислоты.
На этапе распределения и депонирования
· конкурентное вытеснение из связи с альбуминами плазмы крови – если ЛС связано с белками менее 90%, то вытеснение из связи с ним не приведет к… · вытеснение из связи с белками в тканях: хинидин вытесняет дигоксин +… 3. На этапе метаболизма – ЛС могут повышать либо снижать активность ферментных систем, участвующих в метаболизме ЛС (…На этапе выведения
· изменение канальцевой секреции – хинидин + дигоксин = повышение концентрации дигоксина в крови и развитие токсических эффектов (хинидин… · изменение канальцевой реабсорбции – реабсорбции подвергаются только… 40.Фармакодинамическое взаимодействие лекарственных веществ. Антагонизм, синергизм, их виды. Характер изменения…Побочные и токсические эффекты лекарственных веществ. Тератогенное, эмбритоксическое, мутагенное действие лекарств. Медицинские и социальные аспекты борьбы с лекарственной зависимостью, наркоманиями и алкоголизмом. Понятие о токсикоманиях.
Побочные эффекты – те эффекты, которые возникают при применении веществ в терапевтических дозах и составляют спектр их фармакологического действия, могут быть первичными и вторичными:
а) первичные побочные эффекты – как прямое следствие влияния данного препарата на определенный субстрат {гипосаливация при применении атропина для устранения брадиаритмии}
б) вторичные побочные эффекты – косвенно возникающие неблагоприятные влияния {АБ, подавляя нормальную микрофлору, могут привести к суперинфекции}
Токсические эффекты – нежелательные эффекты, проявляющиеся у данного ЛС при выходе из терапевтического диапазона {передозировка ЛС}
Избирательность действия ЛС зависит от его дозы. Чем выше доза препарата, тем менее избирательным он становится.
Тератогенное действие– способность ЛС при назначении его беременной женщине вызывать анатомические аномалии развития плода {талидомид: фокомелия, противобластомные ЛС: множественные дефекты}
Эмбриотоксическое действие – неблагоприятное воздействие, не связанное с нарушением органогенеза в первые три месяца беременности. На более поздних сроках проявляется фетотоксическое действие.
Мутагенное действие ЛС – повреждение зародышевой клетки и ее генетического аппарата ЛС, что проявляется изменением генотипа потомства {адреналин, цитостатики}.
Канцерогенное действие ЛС – способность некоторых ЛС индуцировать канцерогенез.
1) Лекарственная зависимость – состояние психики и/или физическое состояние, которое является следствием воздействия на организм ЛС и характеризуется специфическими поведенческими реакциями, трудно преодолимым стремлением повторно принимать ЛС, чтобы добиться особого психического эффекта или избежать дискомфорта при отсутствии ЛС в организме. Лекарственная зависимость характеризуется:
а) психологической зависимостью – развитием эмоционального дистресса при прекращении приема ЛС. Человек ощущает себя опустошенным, погружается в депрессию, испытывает чувство страха, тревоги, его поведение становится агрессивным. Все эти психопатологические симптомы возникают на фоне мыслей о необходимости ввести себе ЛС, вызвавшее зависимость. Стремление к приему ЛС может колебаться от простого желания до страстной жажды приема ЛС, которая поглощает все остальные потребности и превращается в смысл жизни человека. Считают, что психологическая зависимость развивается тогда, когда у человека появляется сознание того, что оптимального самочувствия он может достигнуть исключительно благодаря введению ЛС. Основа психологической зависимости - вера человека в действие лекарства (в литературе описаны случаи развития психологической зависимости к плацебо).
б) физической зависимостью - нарушением нормального физиологического состояния организма, которое требует постоянного присутствия в нем ЛС для поддержания состояния физиологического равновесия. Прекращение приема лекарства вызывает развитие специфического симптомокомплекса - абстинентного синдрома – комплекса психических и нейровегетативных расстройств в виде нарушения функции в сторону, противоположную той, которая характерна для действия {морфин устраняет боль, угнетает дыхательный центр, суживает зрачки, вызывает запор; при абстиненции у пациента возникают мучительные боли, частое шумное дыхание, зрачки расширены и развивается упорная диарея}
в) толерантностью. Толерантность к средствам, вызывающим лекарственную зависимость зачастую носит перекрестный характер, т.е. возникает не только к данному химическому соединению, но и ко всем структурно подобным соединениям. Например, у пациентов с лекарственной зависимостью к морфину толерантность возникает не только к нему, но и к другим опиоидным анальгетикам.
Для развития лекарственной зависимости наличие всех 3 критериев не является необходимым условием.
Опиоиды, барбитураты, алкоголь вызывают сильные физическую, психологическую зависимости и толерантность. Анксиолитики (диазепам, альпразолам) преимущественно вызывают психологическую зависимость.
2) Наркомания (наркотическая зависимость)– это крайне тяжелая форма лекарственной зависимости, компульсивное применение ЛС, характеризующееся все возрастающим, непреодолимым влечением к введению данного лекарства все увеличивая его дозы. Компульсивность влечения означает, что потребность во введении лекарства доминирует у пациента над всеми другими (даже витальными) потребностями. С позиций данного определения, влечение к морфину – наркомания, тогда как влечение к никотину – лекарственная зависимость.
3) Пристрастие к лекарству - характеризует менее интенсивное влечение к приему лекарств, когда отказ от лекарства вызывает только ощущение легкого дискомфорта, без развития физической зависимости или развернутой картины психологической зависимости. Т.о. пристрастие охватывает ту часть лекарственной зависимости, которая не подпадает под определение наркомании. Например, упомянутая выше лекарственная зависимость к никотину – форма пристрастия.
4) Злоупотребление лекарственными средствами – самовольное применение лекарственных средств в таких дозах и такими способами, которые отличаются от принятых медицинских или социальных стандартов в данной культуре и в данное время. Т.о. злоупотребление ЛС охватывает только социальные аспекты применения лекарств. Примером злоупотребления является использование анаболических стероидов в спорте или для улучшения телосложения молодыми мужчинами.
5) Алкоголизм – хроническое злоупотребление алкоголя (этилового спирта), приводящее со временен к поражению ряда органов (печени, ЖКТ, ЦНС, сердечно-сосудистой системы, иммунной системы) и сопровождающееся психико-физической зависимостью.
6) Токсикомания – хроническое злоупотребление различными ЛС (в т.ч. наркотиками, алкоголем, галлюциногенами), проявляющееся многообразными психическими и соматическими расстройствами, нарушением поведения, социальной деградацией.
Лечение лекарственной зависимости трудная и неблагодарная задача. До сих пор не создано эффективной методики, которая бы обеспечивала бы успех лечения более чем у 30-40% пациентов. Достижение сколько-нибудь заметных результатов возможно только при полной кооперации усилий пациента, врача и того социального окружения, в котором находится заболевший (принцип добровольности и индивидуальности). В основе современных методик лежат следующие принципы:
-психотерапевтические и трудотерапевтические методы;
-групповое лечение и реабилитация (общества анонимных алкоголиков, наркоманов)
-постепенная или резкая отмена препарата на фоне детоксикационной терапии
-проведение заместительной терапии (замена наркотического средства медленно и длительнодействующими аналогами с их последующей отменой; например, т.н. программа метадоновой заместительной терапии у героиновых наркоманов)
-лечение специфическими антагонистами (налоксоном и налтрексоном) или сенсибилизирующими средствами (тетурамом)
-нейрохирургический методы криодеструкции поясной извилины и гиппокампа
42.Фармацевтическое взаимодействие лекарственных средств. Предупреждения и меры предосторожности при проведении инфузионной терапии.
Фармацевтическое взаимодействие -вид взаимодействия, связанный с физико-химической реакцией между ЛС в процессе изготовления лекарственного препарата, еще до введения этих средств в организм человека
а) типичные ошибки, приводящие к фармацевтической несовместимости: выписывание сложных рецептов, неправильное хранение, не учитывается возможность адсорбции ЛС на поверхности пластмассы {органические нитраты}
б) проблемы при инфузионной терапии: смешивание растворимых солей, производных нерастворимых слабых кислот или оснований приводит к их преципитации; в жидких лекарственных формах гидролизуются сердечные гликозиды и алкалоиды, разрушаются АБ; рН среды (в щелочной среде выпадают в осадок алкалоиды)
в) рекомендации: 1) Все смеси лучше готовить ex tempore 2) Наиболее надежен раствор с одним ЛС 3) Все растворы перед употреблением необходимо проверить на наличие взвесей 4) Взаимодействие может происходить без видимых изменений растворов 5) Нельзя добавлять ЛС в кровь и растворы АК 6) При отсутствии специальных указаний препараты следует растворять в 5%-ом р-ре глюкозы (рН 3,5-6,5), изотоническом растворе NaCl (рН 4,5-7,0).
Раствор глюкозы, стабилизированный HCl, несовместим с адреналином, бензилпенициллином, апоморфином, канамицином, витамином С, олеандомицином, сердечными гликозидами. Сердечные гликозиды несовместимы с атропином, папаверином, платифиллином. АБ несовместимы с гепарином, гидрокортизоном. Витамины группы В несовместимы между собой, с витаминами PP, С. Витамин РР и С также между собой несовместимы.
Нельзя смешивать ни с какими другими препаратами: фенотиазид, хлорпромазин, барбитураты, препараты витамина С, амфотерицин В, фуросемид, сульфадиазин, аминофиллин, адреномиметики.
Виды фармакотерапии. Деонтологические проблемы фармакотерапии.
1. этиотропная ФТ – коррекция и устранение причины заболевания {АБ при инфекционных заболеваниях} 2. патогенетическая ФТ – воздействие на механизм развития болезни {ингибиторы… 3. симптоматическая ФТ – устранение симптомов заболевания при невозможности влияния на его причину или патогенез {НПВС…Основные принципы лечения и профилактика отравлений лекарственными веществами. Антидотная терапия(примеры).
Классификация отравляющих веществ (ОВ):
1. По принадлежности к определенным классам химических соединений: барбитураты, бензодиазепины, цианиды.
2. По происхождению: небиологической природы (кислоты, щелочи, соли тяжелых металлов), токсические продукты жизнедеятельности некоторых МБ (ботулотоксин), растительного происхождения (алколоиды, гликозиды), животного происхождения (яды змей, пчел)
3. По степени токсичности: а) чрезвычайно токсические (DL50 < 1 мг/кг) б) высоко токсические (1-50) в) сильно токсические (50-500) г) умеренно токсические (500-5000) д) мало токсические (5000-15000) е) практически нетоксические (> 15.000)
4. По токсикологическому действию: а) нервно-паралитического (бронхоспазм, удушье) б) кожно-резорбтивные в) общетоксические (гипоксические судороги, кома, параличи) г) удушающие д) слезоточивые и раздражающие е) психотропные (нарушение психической активности, сознания)
5. В зависимости от сферы преимущественного использования: промышленные яды, ядохимикаты, бытовые яды, боевые отравляющие вещества, лекарственные вещества.
6. В зависимости от токсичности ЛС: список А – ЛС, назначение, применение, дозирование и хранение которых в связи с высокой токсичностью должны производиться с высокой осторожностью. К этому же списку относятся ЛС, вызывающие наркоманию; список В - ЛС, назначение, применение, дозирование и хранение которых должны производиться с предосторожностью в связи с возможными осложнениями при их применении без медицинского контроля.
Избирательно токсическое действие ЛС.
а) кардиотоксическое: сердечные гликозиды, препараты калия, антидепрессанты
б) нейротоксическое: психофармакологические средства, оксихинолины, аминогликозиды
в) гепатотоксические: тетрациклины, левомицетин, эритромицин, парацетамол
г) нефротоксическое: ванкомицин, аминогликозиды, сульфаниламиды
д) гастроентеротоксическое: стероидные противовоспалительные средства, НПВС, резерпин
е) гематотоксическое: цитостатики, левомицетин, сульфаниламиды, нитраты, нитриты
ж) пневмотоксические
Токсикокинетика– изучает всасывание, распределение, метаболизм и выведение ЛС, принятых в токсических дозах.
Поступление отравляющих веществ в организм возможно а) энтерально б) парентерально. Скорость и полнота всасывания отражает скорость развития токсического эффекта и его выраженность.
Распределение в организме: Vd=D/Cmax – действительный объем, в котором распределяется в организме отравляющее вещество. Vd > 5-10 л/кг – ОВ трудно допустимо для его удаления (антидепрессанты, фенотиазины). Vd < 1 л/кг – ОВ легче удалить из организма (теофиллин, салицилаты, фенобарбитал).
Передозировка – изменение фармакокинетических процессов: растворимости, связи с белками, метаболизма ® значительное повышение свободной фракции ЛС ® токсические эффект.
Кинетика первого порядка при увеличении концентрации ЛС переходит в кинетику нулевого порядка.
Токсигенная стадия – дезинтоксикационная терапия, соматогенная стадия – симптоматическая терапия.
Токсикодинамика. Основные механизмы токсического действия:
а) медиаторный: прямой (по типу конкурентной блокады – ФОС, психомиметики) и непрямой (активаторы или ингибиторы ферментов)
б) взаимодействие с биомолекулами и внутриклеточными структурами (гемолитические вещества)
в) метаболизм по типу летального синтеза (этиловый спирт, тиофос)
г) ферментный (яды змей и др.)
Виды действия: местное, рефлекторное, резорбтивное.
Классификация отравлений:
1. Этиопатогенетическая:
а) случайное (самолечение, ошибочный прием)
б) преднамеренное (с целью самоубийства, убийства, развития у пострадавшего беспомощного состояния)
2. Клиническая:
а) в зависимости от скорости развития отравления: острое (поступление однократно или с коротким интервалом времени токсической дозы вещества), подострое (замедленное развитие клинической картины после однократного приема), хроническое
б) в зависимости от проявления основного синдрома: поражение ССС, поражение ДС и др.
в) в зависимости от тяжести состояния больного: легкой, средней, тяжелой, крайне тяжелой
3. Нозологическая: учитывает название ЛС, название группы веществ
Общий механизм смерти при отравлении:
а) поражение ССС:
1) снижение АД, гиповолемия периферических сосудов, коллапс, бради- или тахикардия (трициклические антидепрессанты, бета-блокаторы, блокаторы кальциевых каналов)
2) аритмии (желудочковая тахикардия, фибрилляция – трициклические антидепрессанты, теофиллин, амфетамин)
б) поражение ЦНС: ступор, кома ® угнетение дыхания (наркотики, барбитураты, алкоголь, гипно-седативные ЛС)
в) судороги, мышечная гиперреактивность и ригидность ® гипертермия, миоглобинурия, почечная недостаточность, гиперкалиемия
Токсикологическая триада:
1) длительность применения, доза и вещество ® анамнез.
2) оценка состояния сознания по симптомам: дыхания, АД, температура тела
3) лабораторные данные
Основные принципы лечения:
I. Первая неотложная помощь: искусственное дыхание, массаж сердца, противошоковая терапия, контроль за водно-электролитным балансом
II. Задержка всасывания и удаление из организма не всосавшегося ОВ:
Цель: прекратить контакт с ОВ
1. Парентеральный путь:
а) через легкие:
1) прекратить ингаляцию
2) раздражающие вещества (нашатырный спирт, формальдегид) ® закрепить активные движения, согреть, дать кислород и пеногасители (у нашатырного спирта пеногаситель уксус, а у формальдегида – разбавленный раствор нашатырного спирта)
б) через кожу: смыть обильным количеством теплой воды с мылом или моющим средством, специфические противоядия, нейтрализация и прекращение воздействия ОВ на кожу (ФОС: обмывают водой, удаляют с помощью 10-15% нашатырного спирта или 5-6% раствора гидрокарбоната натрия с водой; фенолкрезол: растительное масло или этиленгликоль, но нельзя вазелиновое масло, KMNO4: 0,5-1%-ый раствор аскорбиновой кислоты или равные объемы 3% перекиси водорода и 3% раствора уксусной кислоты, CCl4, скипидар, бензин: теплая мыльная вода)
в) при инъекции в конечность: жгут выше места инъекции
г) при попадании в глаза: промывание теплым физраствором или молоком в течении 10-20 минут, закапать местный анестетик; при попадании кислот и щелочей нельзя нейтрализовать. Обязательна консультация офтальмолога.
2. Энтеральный путь: освободить желудок от ОВ, ускорить пассаж
а) удаление ОВ:
1) предварительно прием воды. Нельзя принимать молоко (исключение – едкие отравляющие вещества) и этанол (исключение –метанол).
2) рвота – показана преимущественно при отравлении крупными таблетками или капсулами, которые не могут пройти через зонд. Можно спровоцировать рефлекторно или рвотными средствами (NaCl: 1 столовая ложка на 1 стакан воды; сироп ипекакуаны: взрослым 2 столовые ложки, детям 2 чайные ложки; горчица: 1-2 чайные ложки на стакан воды; апоморфин: 5-10 мг/кг подкожно, кроме детей до 5 лет). Нельзя вызывать рвоту после приема: органических растворителей – опасность ингаляций, моющих средств – пенообразование, судорожных ОВ – опасность аспирации, едких веществ – повреждение пищевода)
3) зондовое промывание желудка – является экстренным и обязательным мероприятием. Желудок промывают, если с момента отравления прошло не более 4-6 часов, иногда до 10 часов; при отравлении ацетилсалициловой кислотой – через 24 часа. Предварительно интубируют пациента трубкой с раздувной манжетой: в коматозном состоянии при отсутствии кашлевого и ларингеального рефлекса. Желудок промывают водой или физраствором 30° С, время процедуры 4 часа и более. В конце промывания – активированный уголь и сульфат натрия.
б) снижения всасывания из ЖКТ: активированный уголь внутрь после опорожнения желудка + сульфат натрия или магния. Особенности мероприятий по снижению всасываемости:
1) органические растворители: нельзя вызывать рвоту, промывание желудка после интубации, активированный уголь + вазелиновое масло
2) моющие средства: нельзя вызывать рвоту и промывать желудок, необходимо давать много воды + пеногасители (симетикон)
3) кислоты и щелочи: нельзя вызывать рвоту, промывание желудка через зонд, смазанный растительным маслом после введения наркотического анальгетика – единственное показание для дачи молока. При отравлении кислотами – антациды, при отравлении щелочи – лимонная или уксусная кислоты.
III. Удаление из организма всосавшегося ОВ
а) форсированный диурез (условия: достаточный почечный кровоток и клубочковая фильтрация; за 24 часа влить-вылить 20-25 литров)
б) перитонеальный гемодиализ
в) гемосорбция
г) обменное переливание крови
д) форсированная гипервентиляция
IV. Симптоматическая терапия функциональных нарушений.
2) токсикокинетические – ускоряют биотрансформацию ОВ (тримедоксима бромид, натрия тиосульфат, этанол, АО) 3) фармакологические – атропин, налоксон 4) иммунологические противоядияПравила выписывания ядовитых, наркотических и сильнодействующихсредств.
Рецепты на наркотические в-ва (морфин, омнопон, промедол, фенамин, кокаин и др.) и приравненные к ним независимо от лек. ф-мы выписывают на спец.… В случае, если лек. ср-во содерж. спирт, то ставится печать леч. учрежд. «Для… В тех случаях, когда макс. дозу ядовитых или сильнод. в-в превышают, необх. указать их кол-во прописью с добавлением…– Конец работы –
Используемые теги: Сущность, фармакологии, науки, разделы, области, современной, фармакологии, основные, термины, понятия, фармакологии, фармакологическая, Активность, действие, эффективность, химических, веществ0.176
Если Вам нужно дополнительный материал на эту тему, или Вы не нашли то, что искали, рекомендуем воспользоваться поиском по нашей базе работ: Сущность фармакологии как науки. Разделы и области современной фармакологии. Основные термины и понятия фармакологии – фармакологическая активность, действие, эффективность химических веществ.
Что будем делать с полученным материалом:
Если этот материал оказался полезным для Вас, Вы можете сохранить его на свою страничку в социальных сетях:
| Твитнуть |
Хотите получать на электронную почту самые свежие новости?







Новости и инфо для студентов