Работа 4. Исследование нестационарной диффузии хронопотенциометрическим методом
Хронопотенциометрия – метод исследования электрохимических процессов, основанный на определении зависимости потенциала от времени при постоянной плотности тока или при изменении ее во времени по определенному (например, линейному) закону. В условиях, когда скорость какого-либо электрохимического процесса определяется скоростью подвода реагирующего вещества к поверхности электрода из объема раствора, хронопотенциометрический метод можно использовать для аналитических целей (измерения концентрации ионов), а также для определения коэффициентов диффузии ионов и суммарного числа электронов, участвующих в электродной реакции. Анализ экспериментально полученных хронопотенциограмм дает возможность определить условия, при которых скорость электродной реакции лимитируется массопереносом.
Рассмотрим самый простой вариант хронопотенциометрического метода – так называемый гальваностатический метод (хронопотенциометрия при постоянном токе).
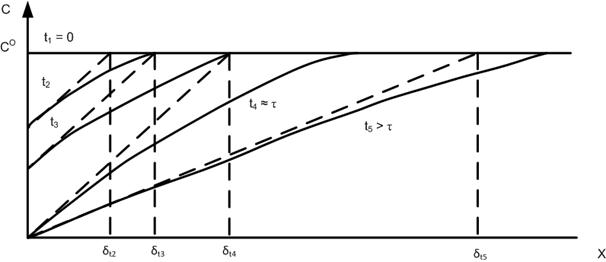
Рис. 1. Распределение концентрации реагирующего вещества в приэлектродной зоне раствора в разные моменты времени после включения тока постоянной плотности: t1 < t2 < t3 < t4 < t5.
На рис. 1 показано схематическое распределение концентрации реагирующего вещества в приэлектродной зоне раствора в различные моменты времени t после включения тока. Поскольку i = const, градиент концентрации у поверхности электрода (при Х → 0) должен сохраняться неизменным (см. кривые для t2, t3 и t4):
i = nFDi grad Ci, x→0, (1)
где i – плотность
n – суммарное число электронов, участвующих в электродной реакции;
Di – коэффициент диффузии i – х частиц;
Ci – их концентрация.
Эффективная толщина диффузионного слоя при этом меняется согласно уравнению:
 (2)
(2)
Постоянство градиента концентрации у поверхности электрода при i = const обеспечивается за счет непрерывного падения концентрации реагента у электрода:
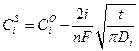 , (3)
, (3)
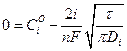 . (3а)
. (3а)
В момент времени t4 = τ, называемый переходным временем, СiS упадет до нуля (кривая t4) и после этого grad Ci, x→0 начнет уменьшаться (кривая t5). Плотность тока рассматриваемой электродной реакции при t > τ должна постепенно уменьшаться в соответствии со снижением grad Ci, x→0. Поэтому при t > τ постоянство плотности тока на электроде поддерживается за счет протекания каких-либо других электрохимических реакций (разряда ионов фонового электролита и т.д.).
Так как при t > τ CiS → 0, то в соответствии с уравнением диффузионного перенапряжения:
 (4)
(4)
(индексы O и S относятся, соответственно, к объему раствора и внешней нранице двойного электрического слоя) диффузионное перенапрядение обращается в бесконечность. Действительно, на хронопотенциограмме (см. рис. 2) наблюдается скачок потенциала при t > τ. Второй участок медленного изменения потенциала определяется природой второй электрохимической реакции, доля которой в суммарной плотности тока при t > τ будет непрерывно возрастать.
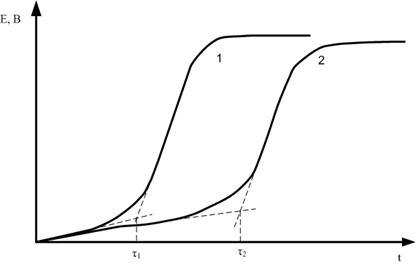
Рис. 2. Гальваностатические кривые (хронопотенциограммы) при плотности тока: 1- i1 = 1,75iпр., 2- i2 = 1,25iпр.
Предполагая, что отклонение потенциала электрода от равновесного значения обусловлено исключительно изменением концентрации реагентов у поверхности электрода, т.е. рассматривая перенапряжение как чисто диффузионное, можно, комбинируя уравнение Нернста и уравнения (3) и (3а), получить уравнение, описывающее изменение потенциала во времени при t < τ (уравнение Караогланова):
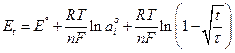 ; (5)
; (5)
при равновесии (t = 0)
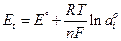 ; (5а)
; (5а)
Если лимитирующей стадией какой-либо электрохимической реакции является массоперенос, то кривые 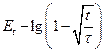 должны совпадать при различных значениях i и иметь линейный характер. Экстраполяция прямой к оси ординат должна отсекать на последней Et=0 = EP.
должны совпадать при различных значениях i и иметь линейный характер. Экстраполяция прямой к оси ординат должна отсекать на последней Et=0 = EP.