ИСТИННАЯ И СРЕДНЯЯ ТЕПЛОЕМКОСТИ
Теплоемкости могут быть массовые, объемные, молярные. Теплоемкость 1 кг газа называется массовой: она обозначается буквой с и измеряется в Дж/(кг . К).
Теплоемкость 1 м3 газа, взятого при нормальных условиях (r = 760 мм рт. ст., t = 0 0С), называется объемной. Она обозначается буквой с¢ и измеряется в Дж/(м3 . К).
Теплоемкость 1 киломоля газа называется молярной, обозначается mс и измеряется в Дж/(кмоль . К).
Зависимость между удельными теплоемкостями следующая:
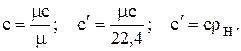 (22)
(22)
Здесь 22,4 м3 и rн – соответственно объем 1 киломоля газа и плотность при нормальных условиях. Теплоемкость газов – величина переменная, зависит от температуры и давления. Если для идеальных газов зависимость теплоемкости от давления ничтожна и ею пренебрегают, то для реальных газов, особенно при высоких давлениях, ошибка в расчетах может быть существенной.
Зависимость теплоемкости газов от температуры выражается в том, что в процессе нагревания единицы газа на 1 К расходуется разное количество теплоты.
Различают теплоемкости средние (см. приложения 2, 3, 4) и истинные. Средней теплоемкостью сm называется количество теплоты, которое расходуется при нагревании единицы газа (1 кг, 1 м3, 1 моль) на 1 К от t1 до t2:
cm = q / t2 – t1. (23)
Чем меньше разность температур t2 – t1, тем больше значение средней теплоемкости приближается к истинной с. Следовательно, истинная теплоемкость будет иметь место при t2 – t1, приближающемся к нулю.