Расчет шахтной печи
Исходные данные [6]:
нагрузка по сухому газу 126376 нм3/ч;
состав сухого газа (об. %): СН4 10;
N2 1,6;
Н2 69,15;
СО 9,45;
СО2 9,81;
отношение пар:газ 0,7771;
состав воздуха (об. %): N2 78;
О2 21;
Ar 1;
давление 4,07 МПа;
температура газа на входе 860 °С;
температура газа на выходе 1000 °С;
концентрация метана на выходе 0,3 об.%
Рассчитаем константу равновесия (3.6) [1]:

Расчет материального баланса ведем на 100 нм3 сухого газа.
Введем обозначения: c – объем водорода на выходе, нм3; b – объем СО на выходе, нм3; а – объем СО2 на выходе, нм3; d – объем образовавшейся воды, нм3; V – объем сухого газа на выходе, нм3; у – объем воздуха на оксиление.
Соотношение суммы монооксида углерода и водорода в прореагировавшей смеси должно составлять 3.
С учетом принятых обозначений составляем балансовые уравнения по элементам, входящим в состав реагирующих веществ, общий баланс и условие равновесия:
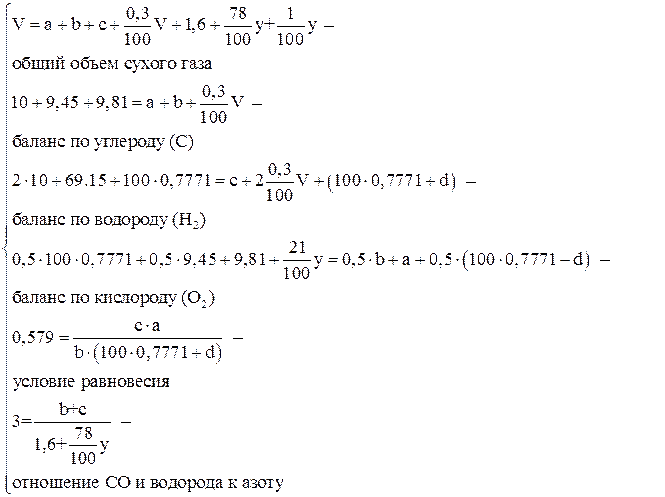
Решая полученную систему, имеем:
а = 10,77; b = 18,06; с = 81,75; d = 6,53; V = 144,69; у = 40,6.
Объем водяных паров на выходе
100×0,7771 + 6,53 = 84,24 м3.
Объем метана на выходе
0,3/100×144,69 = 0,43 нм3.
Объем кислорода, поступающего с воздухом
21/100×40,6 = 8,53 нм3.
Объем азота, поступающего с воздухом
78/100×40,6 = 31,67 нм3.
Объем аргона, поступающего с воздухом
1/100×40,6 = 0,41 нм3.
Результаты расчета сведем в таблицу 3.3.