Строение чистых металлов
Большинство металлов и сплавов имеют кристаллическое строение. Свойства кристаллов зависят от ряда факторов и поэтому могут рассматриваться с разных позиций:
- пространственного расположения частиц в кристалле (определяет его геометрическое строение);
- электронного строения атомов и характера взаимодействия их в кристалле (определяется типом химической связи между атомами);
- химического состава (чистый металл или сплав).
Взаимодействие этих факторов и описывается понятием строение.
Упорядоченность расположения частиц характерна для металлов. Она образует кристаллическую пространственную структуру, которая определяет геометрическое строение кристалла.
Если соединить атомы воображаемыми линиями в трех взаимно перпендикулярных направлениях, получиться пространственная кристаллическая решетка. Её наименьшим структурным образованием является элементарная ячейка, которая представляет собой простую геометрическую фигуру: куб, параллелепипед, шестигранную призму и другие. Многократные повторения примыкающих друг к другу ячеек в пространстве и образует кристалл. В вершинах простых геометрических фигур находятся атомы. Они образуют узлыкристаллической пространственной решетки.
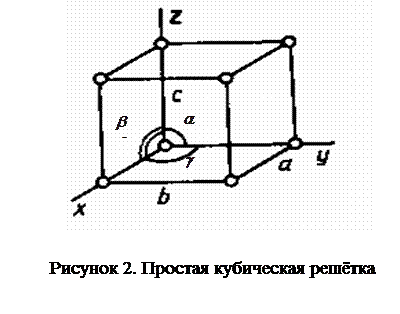 |
Наиболее простой кристаллической решеткой у металлов является кубическая (рисунок 2), в узлах ячейки которой находятся по 1 атому, всего в ячейке - 8 атомов. Проведя через ребра куба три оси (направления) x, y, z, как указано на
рисунке 2, положение узлов элементарной ячейки можно описать шестью величинами: тремя отрезками, равными расстояниям а, в, с, и тремя углами a, b, gмежду этими отрезками. Расстояния между атомами ячейки кристаллической решетки а, в, с, называют периодами (параметрами) решетки. Соотношения между этими величинами определяют систему. Если, а = в = с; a=b = g = 90о, то такая кристаллическая система называется кубической, например, у марганца. Если а = в¹ с; a = b = g = 90о – тетрагональная система (элементарная ячейка представляет собой параллелепипед); а = в ¹ с; a = b = 90о, g = 120о – система гексагональная (элементарная ячейка – шестигранная призма). На рисунке 3 приведены основные типы элементарных ячеек металлов: объемно - центрированная кубическая (ОЦК–молибден, вольфрам, α-железо) – рисунок 3,а; гранецентрированная кубическая (ГЦК –медь, никель, алюминий, свинец, кобальт, γ-железо) – рисунок 3,б; гексагональная плотноупакованная (ГП – бериллий, кадмий, магний, цинк) – рисунок 3,в, которые имеют более сложное строение, чем простая кубическая (рисунок 2). Частицы могут находиться не только, в узлах, но и на гранях и в центре элементарной ячейки.
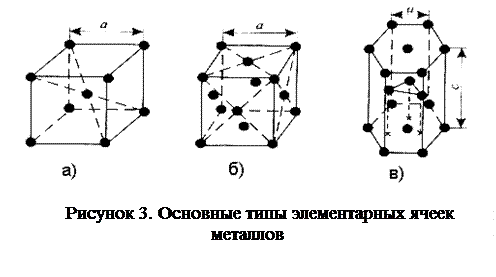 |
О степени сложности строения решеток судят по числу частиц, приходящихся на одну элементарную ячейку. В простой кубической решетке на одну ячейку приходится одна частица, в ОЦК – две, ГЦК ячейке – четыре. ОЦК решетку имеют Mo, V, a - Fe, ГЦК решетку имеют Cu, Ni, Al, Pb, Co, g- Fe, ГП – Ве, Cd, Mg, Zn и другие. металлы. Система, период и число частиц на одну элементарную ячейку полностью определяют расположение частиц в кристалле. Для описания различных явлений, происходящих в кристаллах, особенностей свойств кристаллических тел вдоль различных направлений и плоскостей, используются понятия кристаллографические направления и плоскости.