При медленном охлаждении
Диаграмма состояния показывает, как указывалось ранее, изменение равновесного состояния сплавов в зависимости от температуры и концентрации. Равновесным является такое состояние, при котором наблюдается минимум свободной энергии. Практически равновесное состояние достигается тогда, когда нагрев и охлаждение проводят с очень малыми скоростями.
По структуре в медленно-охлажденном состоянии углеродистые стали делятся на три группы: 1) эвтектоидная (С=0,8 %); 2) доэвтектоидные (С от 0,02 до 0,8 %); 3) заэвтектоидные (С от 0,8 до 2,14 %).
Рассмотрим фазовые превращения в сталях при охлаждении.
1) Доэвтектоидная сталь с содержанием С=0,6 % (I) (рис. 5.4).
| |
| |
|
|
|
| |
|
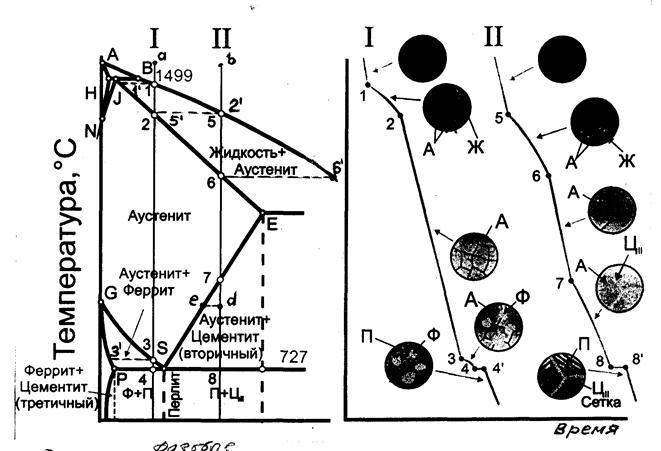
Рис. 5.4. Кривые охлаждения углеродистых сталей
Обозначим на диаграмме критические точки данного сплава, то есть температуры, при которых в сплаве происходят фазовые превращения:
а –1: простое охлаждение Ж;
1–2: 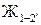 ®
®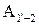 (происходит кристаллизация аустенита, при этом концентрация жидкой фазы меняется по линии ликвидус (1–2¢), а аустенита – солидус (1¢–2);
(происходит кристаллизация аустенита, при этом концентрация жидкой фазы меняется по линии ликвидус (1–2¢), а аустенита – солидус (1¢–2);
2–3: простое охлаждение А.
При переохлаждении ниже точки 3 из аустенита начинает выделяться феррит:
3–4: А3–S ® 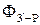 ;
;
точка 4: а) при достижении этой точки сталь состоит из ФР и АS;
б) происходит при этой температуре эвтектоидное превращение:
АS → ФР+ЦК;
в) после окончания его сталь состоит из ФР и П(ФР+ЦК).
Следовательно, любая доэвтектоидная сталь имеет структуру Ф+П(Ф+Ц).
2) Заэвтектоидная сталь с содержанием С=1,5 % (II) (см. рис. 5.4).
b–5: простое охлаждение Ж
5–6: 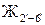 ®
®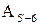
6–7: простое охлаждение А.
Ниже точки 7 у данного сплава аустенит становится пересыщенным. Например, при температуре, соответствующей точке d, в аустените углерода может находиться в равновесии в количестве, соответствующем точке е (меньше 1,5 %). Поэтому при медленном охлаждении от точки 7 до точки 8 этот избыточный углерод должен постепенно выделяться из кристаллической решётки аустенита. Но так как в данной системе нет фазы, представляющей собой чистый углерод, то этот избыточный углерод выделяется в виде самой высокоуглеродистой фазы – цементита:
7–8: А7–8 → ЦII.
Этот цементит называют вторичным. Первичным называют цементит, который выделяется из жидкой фазы.
Таким образом, линия ES показывает предельную растворимость углерода в аустените в интервале температур 1147…727 °С.
При достижении точки 8 (t=727 °С) сталь состоит из двух фаз: аустенита и вторичного цементита:
точка 8: а) АS ,ЦII .
При этой температуре происходит эвтектоидное превращение аустенита (PSK)
б) АS → ФР + ЦК , (ФР + ЦК – перлит).
После окончания этого превращения сплав состоит из:
в) П(ФР +ЦК), ЦII.
Ниже точки 8 превращений нет. Следовательно, конечная структура стали (С=1,2 %): П(Ф + Ц) + ЦII.
Таким образом, любая заэвтектоидная сталь после медленного охлаждения при комнатной температуре имеет структуру П(Ф + Ц) + ЦII.
Аналогичным образом можно рассмотреть формирование структуры эвтектидной стали, которая состоит из П(Ф + Ц).
Если линия, соответствующая данному сплаву, пересекает наклонную линию диаграммы, то в этой точке на кривой охлаждения будет перегиб, а если она пересекает горизонтальную линию, то будет горизонтальная площадка.
На рис. 5.5 показаны схемы структур сталей в равновесном состоянии.
| |

Рис. 5.5. Схемы структур сталей в равновесном состоянии:
а – техническое железо; б…г – доевтектоидные стали (б – 0,2 % С; в – 0,4 % С;
г – 0,6 % С); д – эвтектоидная сталь (0,8 %С); е – заэвтектоидная сталь (1,2 % С).
Светлые зерна – феррит; темные участки – перлит; светлая сетка
на рис. е – вторичный цементит