Тема: Приготовление рассола и наполнение им системы.
Цель работы:
Изучить основные положения приготовления рассола и наполнения им системы.
Теоретическая часть:
Приготовление рассола и наполнение им системы
1. В качестве охлаждающего вещества (хладоносителя) в судовых холодильных установках применяются водные растворы солей (рассолы), в основном хлористого кальция (СаСl2).
На некоторых судах иностранной постройки применяется рассол «Айсзоль-экстра» на основе водного раствора хлористого кальция с антикоррозионными добавками.
В качестве низкотемпературного хладоносителя на некоторых судах применяется хладон-11 (R11), а в качестве высокотемпературного хладоносителя — пресная вода (см. приложение 2).
Температура замерзания рассола понижается по мере увеличения содержания в нем соли. Эта закономерность сохраняется до определенного значения массовой концентрации (эвтектический раствор), выше которого температура замерзания рассола начинает повышаться.
Под массовой концентрацией рассола понимается число весовых частей безводной соли, приходящихся на сто весовых частей рассола. При постоянной температуре рассола какой-либо концентрации соответствует вполне определенная плотность.
Плотность рассола замеряется ареометром и измеряется в г/см3 или градусах Боме (°Бе).
Переход от плотности в г/см3 к плотности в °Бе производится по формуле:
п= 144,3 (1-1/γ);
где п — плотность, °Бе; V — плотность, г/см3.
При замере плотности ареометром отсчет ведется по нижнему краю мениска рассола.
Плотность рассола помимо массовой концентрации зависит также от его температуры. Поскольку значения плотности рассола приведены при температуре 15°С, температуру пробы рассола перед замером плотности необходимо довести до этой температуры.
2. Массовая концентрация рассола обычно выбирается с таким расчетом, чтобы температура его замерзания была на 5—10°С ниже рабочей температуры кипения хладагента.
Необходимое для конкретной установки значение плотности рассола или массовой концентрации, как правило, приводится в технической документации на эту установку.
3. Требуемую концентрацию рассола в системе в процессе эксплуатации необходимо поддерживать постоянной.
Недостаточная массовая концентрация рассола, а следовательно, и повышенная температура замерзания его может привести к размораживанию трубок испарителя. При поддержании массовой концентрации рассола большей, чем требуется, увеличивается расход соли. Кроме того, с увеличением концентрации рассола уменьшается его теплоемкость, что вызывает необходимость подачи увеличенного количества рассола в охлаждающие батареи, и возрастает потребная мощность для привода рассольного насоса. При массовой концентрации выше эвтектической в рассоле может начаться кристаллизация, и кристаллы, отлагаясь на трубках испарителя и стенках рассольных трубопроводов, могут вызвать их закупорку.
4. Масса безводной соли (в кг) для приготовления необходимого количества рассола требуемой концентрации
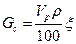
где 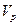 — необходимое количество рассола, л (при первоначальном заполнении
— необходимое количество рассола, л (при первоначальном заполнении 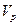 — вместимость рассольной системы);
— вместимость рассольной системы); 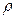 — плотность рассола при 15°С, кг/л (численно равна плотности в г/см3);
— плотность рассола при 15°С, кг/л (численно равна плотности в г/см3); 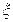 —массовая концентрация рассола, %.
—массовая концентрация рассола, %.
5. Хлористый кальций (СаС12) технический по ГОСТ 450—77 подразделяется на кальцинированный (порошок, гранулы), плавленый (порошок, чешуйки, гранулы) и жидкий.
Рекомендуется применять кальцинированный хлористый кальций высшего сорта. Допускается применять кальцинированный хлористый кальций первого сорта и плавленый хлористый кальций первого сорта.
6. Для снижения коррозионного действия на металл в растворы солей следует добавлять вещества, замедляющие коррозию. Такие вещества называются ингибиторами (пассиваторами). Снижение коррозионного воздействия осуществляется а счет обеспечения нейтральной или слабощелочной реакции рассола с водородным показателем рН = 7...8.
Рассол считается кислым, если рН<7, и щелочным, если рН>8. Рассол, в котором рН = 7...8, не содержит свободной активной кислоты или щелочи и является нейтральным или слабощелочным.
7. Для определения рН к пробе фильтрованного рассола
(примерно 10 см3), разбавленного равным количеством дистиллированной воды, следует прибавить 10—12 капель индикатора. Содержимое в пробирке перемешать до установления устойчивой окраски раствора. Значение рН определяется путем сравнения цвета содержащейся в пробирке пробы с эталонными цветами, характерными для определенной реакции рассола.
8. С достаточной для рассольных систем точностью можно определить рН с помощью универсального индикатора, который получается растворением в 500 мл этилового спирта следующих компонентов:
0,1 г — бромтимола синего (дибромтимолсульфофталеин);
0,1 г — метила красного (диметиламиноазобензолкарбоновая кислота);
0,1 г — нафтолфталеина;
0,1 г — тимолфталеина;
0,1 г — фенолфталеина.
Этот индикатор окрашивает пробу- в следующие цвета (табл. 1).
9. Для приближенного определения реакции рассола в качестве индикаторов применяются фенолфталеин и лакмус. Изменение цвета фенолфталеина начинается при рН 8, а лакмуса— при рН= 7 (табл. 2).
10. Для рассолов СаС12 и «Айсзоль-Экстра» в качестве ингибитора может быть использована каустическая сода (NaОН). Каустическая сода растворяется в пресной воде
(в соотношении 0,5 кг на 20 л воды), и полученный раствор добавляется в циркулирующий рассол до получения (после тщательного перемешивания) нейтральной реакции рассола.