Элементы химической термодинамики и термохимии
Химическая термодинамика – это часть термодинамики, рассматривающая превращения энергии и работы при химических реакциях. Термохимия– раздел химической термодинамики в приложении к тепловым эффектам химических реакций.
Тепловой эффект химической реакции – это количество теплоты, которое выделяется или поглощается при реакции. При этом происходит изменении внутренней энергии системы (U)–суммы кинетической и потенциальной энергий всех частиц, составляющих систему: ∆U = U2 – U1 (U1 – начальное состояние системы, U2 – конечное состояние системы).
В соответствии с первым законом термодинамики (законом сохранения энергии) изменение внутренней энергии закрытой системы определяется количеством теплоты Q,полученной системой из окружающей среды, и работой A, произведенной системой над окружающей средой:
∆U = Q – A, (1)
где A = P ∆V – механическая работа расширения.
Для изобарных процессов (Р = const, ∆V ≠ 0) в термодинамике вводится новая функция энтальпия H = U + PVи Q определяется как изменение энтальпии
∆H = H2 – H1:
QP = ∆H, (2)
где ∆H – тепловой эффект химической реакции при P = const.
Реакции, протекающие с выделением теплоты, называются экзотермическими. В экзотермических реакциях внутренняя энергия и энтальпия системы уменьшаются, ∆H < 0. Реакции, протекающие с поглощением теплоты, называются эндотермическими. В эндотермических реакциях внутренняя энергия и энтальпия системы увеличиваются, ∆H > 0.
В основе термохимических расчетов лежит закон Гесса:тепловой эффект химической реакции зависит только от природы и физического состояния исходных веществ и продуктов реакции и не зависит от пути реакции, т.е. числа промежуточных стадий. Закон Гесса констатирует тот факт, что U и Hявляются функциями состояния системы,т.е. их изменение (∆U и ∆H) зависит только от начального и конечного состояния системы.
Следствие из закона Гесса:
Тепловой эффект химической реакции равен разности между суммой энтальпий образования продуктов реакции и суммой энтальпий образования исходных веществ:
∆H0298 = ∑ν ∆H0f, 298 – ∑ν′ ∆H0f, 298 , (3)
продукты исходные
реакции вещества
(конечное состояние (начальное состояние
системы) системы)
где ν и ν′ - стехиометрические коэффициенты в уравнении реакции;
∆H0f,298 – стандартная энтальпия образования вещества, кДж/моль.
Стандартная энтальпия образования вещества (∆H0f,298) – это тепловой эффект образования одного моля данного вещества из простых веществ в стандартных условиях (Т = 298К, Р = 1 атм.). Значения ∆H0f, 298 приводятся в справочной литературе (см. табл. 2). Для простых веществ ∆H0f, 298 = 0.
Наблюдения показывают, что самопроизвольно, т.е. без затраты работы извне, могут идти как экзотермические, так и эндотермические реакции, если последние сопровождаются увеличением неупорядоченности системы (например, реакции, в которых из твердых веществ образуются газообразные вещества).
Степень неупорядоченности системы выражается термодинамической величиной – энтропией S. Чем выше неупорядоченность системы, тем больше ее энтропия. S также, как U и H, является функцией состояния системы. Для вычисления изменения энтропии (∆S =S2 – S1) в химических реакциях используют следствие из закона Гесса:
∆S0298 = ∑ν ∙S0 298 - ∑ν′ ∙ S0 298 , (4)
продукты исходные
реакции вещества
где ∆S0298 – изменение энтропии реакции при стандартных условиях, Дж/моль;
ν и ν′ – стехиометрические коэффициенты в уравнении реакции;
S0 298 – стандартная энтропия вещества, Дж/моль∙К.
Известны абсолютные значения энтропии веществ, они приводятся в справочной литературе (см. табл. 2).
Термодинамическая величина, связанная с энтальпией и энтропией, называется энергией Гиббса (изобарно-изотермическим потенциалом) и обозначается буквой G:
G = H – T∙S.В изобарно-изотермических условиях
∆G = ∆H – T×∆S (5)
Величина ∆G является критерием направления и предела самопроизвольного протекания химических реакций в закрытых системах при Р,Т = const:∆G ≤ 0.
Если ∆G < 0, то реакция протекает самопроизвольно в прямом направлении (ему отвечает убыль энергии G2 < G1); если ∆G > 0, то самопроизвольно протекает обратная реакция (G2 > G1); если ∆G = 0, то система находится в состоянии равновесия, при котором G = Gmin. Так как G является функцией состояния системы, то для стандартных условий изменение энергии Гиббса химической реакции ∆G0298 рассчитывается следующим образом:
∆G0298 = ∑ν ∙ ∆G0f, 298 – ∑ν′ ∆G0f, 298 , (6)
продукты исходные
реакции вещества
где ν и ν′ - стехиометрические коэффициенты в уравнении реакции;
∆G0f, 298 – стандартная энергия Гиббса образования вещества, кДж/моль.
Стандартная энергия Гиббса образования вещества (∆G0f, 298)– это изменение энергии Гиббса при реакции образования одного моля вещества из простых веществ при стандартных условиях. Значения ∆G0f,298 – это справочные данные, для простых веществ ∆G0f, 298 = 0 (см. табл. 2). Для расчета ∆G при температуре, отличающейся от стандартной (Т ≠ 298К), используется соотношение:
∆GТ = ∆H0298 – T×∆S0298 , (7)
где ∆H0298 – тепловой эффект химической реакции при стандартных условиях, энтальпийный фактор; ∆S0298 – изменение энтропии химической реакции при стандартных условиях; T∆S0298 – энтропийный фактор.
Знак и величина ∆G, а, следовательно, и возможность самопроизвольного протекания процесса при заданных температуре и давлении зависят от соотношения энтальпийного и энтропийного факторов.
Примеры решения задач
Пример 1. Рассчитайте тепловой эффект реакции образования оксида железа (III) из простых веществ при стандартных условиях и стандартную энтальпию образования оксида железа (III), используя следующие термохимические уравнения:
2 Fe(т) + O2 (г) = 2FeO(т) , ∆H01 = - 527,4 кДж (а)
4FeO(т) + O2(г) = 2Fe2O3(т) , ∆H02 = -587,9 кДж (б)
Р е ш е н и е. 1) Записываем термохимическое уравнение образования оксида железа (III) из простых веществ:
4 Fe (т) + 3O2(г) = 2Fe2O3(т) , ∆H03 = ? , (в)
где ∆H03 – тепловой эффект этой реакции.
2) Для расчета ∆H03 необходимо провести такую комбинацию уравнений (а) и (б), которая позволит получить уравнение реакции (в). На основании закона Гесса с термохимическими уравнениями можно оперировать также, как с алгебраическими. Для получения искомого результата следует уравнение (а) умножить на 2, а затем суммировать с уравнением (б): 4Fe + 2O2 + 4FeO + O2 = 4FeO + 2Fe2O3
4Fe + 3O2 = 2 Fe2O3
3) Тепловые эффекты реакции являются составной частью термохимических уравнений, поэтому с ними проведем аналогичные преобразования:
2∙∆H01 + ∆H02 = ∆H03
4) Рассчитываем ∆H03 – тепловой эффект реакции (в):
∆H03 = 2×(–527,4) + (–587,9) = –1054,8 – 587,9 = – 1642,7 кДж.
5) Определяем стандартную энтальпию образования Fe2O3 (∆H0f, 298).
Согласно уравнению (в) в результате реакции образуются 2 моль Fe2O3, поэтому
∆H0f, 298 (Fe2O3) = ∆H03 /2 = – 1642,7 / 2 = – 821,35 кДж/моль.
Правильность расчета проверяем, сравнивая полученное значение со справочными данными табл. 2.
Пример 2. Определите возможность самопроизвольного протекания реакции восстановления оксида хрома (III) углеродом при 298К и 1500К.
Р е ш е н и е. 1) Записываем уравнение этой реакции с указанием агрегатного состояния реагирующих веществ: Cr2O3 (т) +3C(т) = 2Cr(т) + 3CO(г)
2) Согласно условию задачи необходимо ответить на вопрос: будет ли данная реакция протекать в прямом направлении? Критерием направленности химической реакции является изменение энергии Гиббса, а условием самопроизвольного протекания реакции в прямом направлении является соотношение ∆G < 0. Поэтому для решения задачи необходимо определить величину ∆G.
3) Определяем, будет ли данная реакция осуществляться при Т=298К, отвечающей стандартным условиям. Рассчитываем ∆G по уравнению (6), которое для данной реакции имеет вид:
∆G0298 = (2×∆G0f, 298Cr + 3×∆G0f, 298 CO) – (∆G0f, 298 Cr2O3 + 3×∆G0f, 298C)
Для расчета используем значения ∆G0f, 298 приведенные в табл.2
Так как ∆G0f, 298 простых веществ Cr и С равны нулю, то уравнение упрощается:
∆G0298 = 3 моль×(-137,3 кДж/моль) – 1 моль×(-1046,8 кДж/моль)=
= -411,9 кДж + 1046,8 кДж = 634,9 кДж.
Вывод: ∆G0298 > 0, поэтому в стандартных условиях невозможно самопроизвольное протекание процесса в прямом направлении, т.е. при 298К невозможно восстановить Cr2O3 до Cr.
4) Выясняем, возможна ли данная реакция при 1500К. В условиях, отличающихся от стандартных, величина ∆G0Т рассчитывается по уравнению (7):
∆GТ = ∆H0298 – T×∆S0298. Рассчитаем тепловой эффект химической реакции при стандартных условиях, используя уравнение (3) и значения ×∆H0f, 298 из табл.2.
∆H0298 = (2×∆H0f, 298 Cr + 3×∆H0f, 298 CO) – (∆H0f, 298 Cr2O3 + 3∙∆H0f, 298 С).
Но ∆H0f, 298 Cr = 0 и ∆H0f, 298 С = 0, поэтому имеем
∆H0298 = 3∙∆H0f, 298 CO – ∆H0f, 298 Cr2O3,
∆H0298 = 3 моль×(–110,5 кДж/моль) – 1 моль∙(–1141,0 кДж/моль) =
= −331,5 кДж + 1141,0 кДж = 809,5 кДж , ∆H0298 > 0, значит реакция эндотермическая.
Определим изменение энтропии реакции при стандартных условиях. Для расчета используем уравнение (4) и значения S0 298 из табл.2.
∆S0298 = (2×S0 298 Cr + 3×S0 298 CO) – (S0 298 Cr2O3 + 3×S0 298 С),
∆S0298 = (2 моль×23,8 Дж/моль∙К + 3 моль×197,4 Дж/моль∙К) – (1 моль
×81,1 Дж/моль∙К + 3 моль×5,7 Дж/моль∙К) = 639,8 – 98,2 = 541,6 Дж/К.
∆S0298 > 0, т. е. реакция сопровождается увеличением энтропии.
Рассчитаем энергию Гиббса химической реакции при Т = 1500К, т.е. величину ∆G1500: ∆G1500 = ∆H0298 –1500×∆S0298 ,
∆G1500 = 809,5 кДж – 1500К×541,6 Дж/К = 809,5 кДж – 1500×541,6 Дж.
Как видно, члены этого уравнения имеют разную размерность, поэтому приводим их к одной размерности 1 Дж = 1∙10-3 кДж и тогда имеем
∆G1500 = 809,5 – 1500×541,6/1000 = 809,5 – 812,4 = –2,9 кДж.
Вывод: ∆G1500 < 0, значит при 1500К данная реакция протекает самопроизвольно, и при этих условиях можно получить металлический хром.
Таблица 2
Термодинамические величины некоторых веществ в стандартных условиях:
∆H0f, 298 кДж/моль, S0 298 Дж/моль∙К, ∆G0f, 298 кДж/моль.
| Вещество | ∆H0f 298 | S0 298 | ∆G0f, 298 | Вещество | ∆H0f, 298 | S0 298 | ∆G0f, 298 |
| Al (т) | +23,3 | HCl(г) | -92,3 | +187,6 | -95,3 | ||
| Al2O3(т) | -1677,0 | +50,9 | -1576,4 | H2S(г) | -20,2 | +205,6 | -33,0 |
| Al2(SO4)3(т) | -3434,0 | +239,2 | -3091,9 | H2Se(г) | +86,0 | +221,0 | +71,0 |
| C(т) | +5,7 | H2Te(г) | +154,0 | +234,0 | +138,0 | ||
| CO(г) | -110,5 | +197,4 | -137,3 | Mg(т) | +32,0 | ||
| CO2(г) | -393,0 | +214,0 | -394,0 | MgO(т) | -601,2 | +26,9 | -569,6 |
| Cl2(г) | +223,0 | MgCO3(т) | -1096 | +65,7 | -1029 | ||
| CaO(т) | -635,1 | +29,7 | -604,2 | MgCl2(т) | -645,0 | +90,0 | -595,0 |
| Ca(OH)2(т) | -966,2 | +83,4 | -896,8 | N2(г) | +191,5 | ||
| CaCO3(т) | -1206,0 | +92,3 | -1128,8 | NH3(г) | -46,2 | +192,5 | -16,6 |
| Cr(т) | +23,8 | NO(г) | +90,4 | +210,6 | +86,7 | ||
| Cr2O3(т) | -1141,0 | +81,1 | -1046,8 | NO2(г) | +33,9 | +240,5 | +51,8 |
| Cu(т) | +33,0 | NH4Сl(т) | -315,4 | +94,5 | -343,6 | ||
| CuO(т) | -156,0 | +43,0 | -127,0 | O2(г) | +205,0 | ||
| Fe(т) | +27,2 | SO2(г) | -296,9 | +248,1 | -300,4 | ||
| Fe2O3(т) | -821,3 | +90,0 | -741,0 | SO3(г) | -395,2 | +256,2 | -370,4 |
| H2(г) | +130,6 | S(т) | +31,9 | ||||
| H2O(г) | -241,8 | +188,7 | -228,8 | Ti(т) | +31,0 | ||
| H2O(ж) | -285,8 | +70,0 | -237,5 | TiCl4(г) | -759,0 | +353,1 | -714,0 |
1.6. Химическая кинетика и химическое равновесие
Химическая кинетика –раздел химии, изучающий скорость и механизм химических реакций. Различают гомогенные и гетерогенные химические реакции.
Гомогенные реакции протекают в объеме одной фазы – в жидком (водном) или газовом растворе. Например, 2СО(г) + О2(г) = 2СО2(г) (8)
Гетерогенные реакции протекают на границе раздела фаз: г – ж, г – т,
т – т и т.д. Например, 2С(т) + О2(г) = 2СО(г) (9)
Скорость химической реакции (υ) – это изменение количества вещества одного из реагентов за единицу времени в единице реакционного пространства. Она зависит от природы реагирующих веществ, температуры (Т), давления (Р), концентрации (С) реагирующих веществ и других факторов. Зависимость υ от С выражается законом действующих масс: При постоянной температуре скорость химической реакции прямо пропорциональна произведению концентраций реагирующих веществ, взятых в степенях, равных стехиометрическим коэффициентам в уравнении реакции.
Например, для гомогенной реакции (8) υ = k∙С2СО ×СО2 , где k – константа скорости химической реакции, которая зависит от природы реагирующих веществ, температуры, присутствия катализатора, но не зависит от концентрации реагирующих веществ; С – молярные концентрации веществ (моль / л). Для гетерогенной реакции (9) υ = k×СО2 , так как концентрации твердых веществ постоянны и приняты равными единице, т.е. СС = 1.
Зависимость скорости химической реакции от температуры выражает правило Вант-Гоффа: при повышении температуры на каждые 10º скорость химической реакции увеличивается примерно в 2 – 4 раза. Математическое выражение закона Вант-Гоффа:

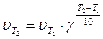 , (10)
, (10)
где υТ1 и υТ2 – скорости реакции при температурах Т1 и Т2; γ - температурный коэффициент скорости химической реакции. Он показывает, во сколько раз увеличивается скорость реакции при повышении температуры на 10º.
По полноте протекания химических процессов различают необратимые и обратимые химические реакции. Необратимые реакции протекают только в одном направлении и завершаются полным превращением исходных веществ в продукты реакции. Обратимые реакции при одной и той же температуре протекают как в прямом, так и в обратном направлении и завершаются установлением в системе химического равновесия. Они не идут до конца, в системе всегда остаются исходные вещества:
N2(г) + 3H2 (г) ⇄ 2NH3(г) (11)
Химическое равновесие – такое состояние химического взаимодействия, при котором скорости прямой и обратной реакций равны между собой, т.е. 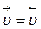 .
.
После наступления состояния равновесия концентрации реагирующих веществ при данных условиях остаются неизменными и называются равновесными концентрациями, обозначаются в квадратных скобках [ ]. Количественной характеристикой химического равновесия является константа химического равновесия К – величина, определяемая соотношением равновесных концентраций продуктов реакции и исходных веществ. Если в соотношение для константы равновесия входят равновесные концентрации, то ее обозначают символом Кс, а если используются парциальные давления газов (Рi) , то – символом Кр. Например, для реакции (11):
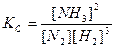 ,
, 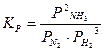
Состояние химического равновесия устанавливается и сохраняется лишь при определенных условиях (температуре, давлении и концентрации реагирующих веществ). При изменении хотя бы одного из этих условий, т.е. при каком-либо внешнем воздействии, равновесие в системе нарушается, и система переходит в новое состояние равновесия. Этот переход называется смещением химического равновесия.
Влияние внешних воздействий (изменение Т, Р или С) на состояние химического равновесия можно предсказать, пользуясь принципом Ле Шателье-Брауна:если на систему, находящуюся в равновесии, оказать внешнее воздействие, то равновесие смещается в том направлении, которое ослабляет эффект внешнего воздействия, т.е на внешнее воздействие система отвечает противодействием. Так увеличение концентрации какого-либо вещества вызовет противодействие системы – стремление уменьшить концентрацию этого вещества, что возможно путем смещения равновесия в направлении, при котором концентрация этого вещества будет уменьшаться.
Повышение Робщ или Рi; приводит к смещению равновесия в сторону протекания той реакции, которая вызывает уменьшение Робщ и Рi и наоборот, понижение Робщ или Pj смещает равновесие в направлении той реакции, которая приводит к увеличению этих параметров.
Повышение температуры вызывает смещение равновесия в направлении протекания той реакции, которая сопровождается поглощением теплоты, т.е. эндотермической (∆Н > 0). Понижение температуры будет вызывать смещение равновесия в сторону экзотермической реакции, сопровождающееся выделением теплоты (∆Н < 0).
Примеры решения задач
Пример 1. Как изменится скорость реакции 2NО(г) + О2(г) ⇄ 2NO2(г), если
одновременно концентрацию NО увеличить в 2 раза, а концентрацию О2 уменьшить в 8 раз?
Р е ш е н и е. 1) Зависимость скорости химической реакции от концентрации реагирующих веществ выражается законом действующих масс, поэтому записываем математическое выражение этого закона для данной реакции в начальный момент времени: 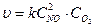
Согласно условию концентрацию NO увеличили в 2 раза, т.е. С'NO=2СNO, а концентрацию О2 уменьшили в 8 раз, т.е. С'o2 = Сo2 /8.
2) Записываем выражение для скорости реакции в конечный момент времени: υ' = k × (С' NO)2 × С'o2 или 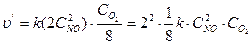
3)  Определяем, как изменяется скорость реакции. Для этого рассматриваем отношение
Определяем, как изменяется скорость реакции. Для этого рассматриваем отношение 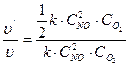 = 1/2
= 1/2
Ответ: при одновременном увеличении концентрации NО в 2 раза и уменьшении концентрации О2 в 8 раз скорость реакции уменьшается в 2 раза.
Пример 2. Определите, во сколько раз изменятся скорости прямой и обратной реакций в системе 2SO2 (г) + О2 (г) ⇄ 2SО3 (г), если объем газовой смеси уменьшить в 3 раза. Каково направление смещения равновесия в этой системе?
Р е ш е н и е. 1) Записываем выражения для скоростей прямой и обратной реакций, используя закон действующих масс: 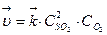 ,
, 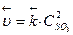
2) Рассматриваем, что происходит в реакционной системе при уменьшении ее объема. Уменьшение объема гомогенной системы в 3 раза приводит к увеличению концентрации каждого из реагирующих веществ также в 3 раза, т.е. математически это записываем в виде: С'so2 = 3С so2 , С'о2 = 3Сo2 и С'so3 = 3С so3.
3) Записываем выражение для скоростей прямой и обратной реакций после изменения объема системы:

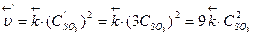
4) Определяем, во сколько раз изменяются скорости прямой и обратной реакций: 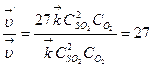 ;
; 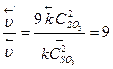
Таким образом, при уменьшении объема газовой смеси в 3 раза скорость прямой реакции увеличится в 27 раз, а скорость обратной реакции – в 9 раз.
5) Устанавливаем направление смещения равновесия в этой системе. В связи с тем, что скорость прямой реакции увеличилась в 27 раз, а обратной – только в 9 раз, равновесие сместится в направлении протекания прямой реакции, т.е. в сторону образования SO3.
Пример 3. Рассчитайте температурный коэффициент скорости химической реакции, если известно, что константа скорости этой реакции при 140°С равна 5,5 × 10-4, а при 185°С – 9,2 × 10-3.
Дано : Т1 =140° С, k1 =5,5 × 10 -4 ; Т2= 185°С, k2 = 9,2∙× 10-3. Найти γ.
Р е ш е н и е. 1) Зависимость скорости химической реакции от температуры описывается правилом Вант-Гоффа в форме: 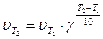
Но для проведения расчетов это уравнение необходимо прологарифмировать, т.е. 

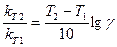
2) Рассчитываем температурный коэффициент скорости этой реакции.
а) вычисляем температуру по абсолютной шкале:
T1 = 140 + 273 = 413 К, Т2 = 185 + 273 = 458 К;
б) рассчитаем численное значение γ:
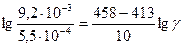 , lg 16,7 = 4,5 lgγ
, lg 16,7 = 4,5 lgγ
отсюда 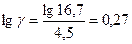 , т.е. lg γ = 0,27, и тогда γ = 1,87.
, т.е. lg γ = 0,27, и тогда γ = 1,87.
Ответ: температурный коэффициент этой реакции равен 1,87.
Пример 4. При синтезе аммиака N2 + ЗН2⇄ 2NНз равновесие установилось  при следующих концентрациях реагирующих веществ (моль/л) [N2 ] = 4; [H2] = 2 и [NH3] = 6. Рассчитайте константу равновесия и исходные концентрации Н2 и N2 .
при следующих концентрациях реагирующих веществ (моль/л) [N2 ] = 4; [H2] = 2 и [NH3] = 6. Рассчитайте константу равновесия и исходные концентрации Н2 и N2 .
Дано: [Н2]=2 моль/л, [N2] = 4 моль/л, [NH3] = 6 моль/л. Найти Кс, Сисх(Н2), Cиcx(N2).
Р е ш е н и е. 1) Записываем выражение для константы равновесия в этой системе и рассчитываем ее значение : 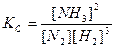 ;
; 


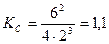
2) Определяем исходные концентрации Н2 и N2.
Для обратимых реакций ни одно из реагирующих веществ не расходуется полностью. Поэтому исходная концентрация вещества А складывается из равновесной концентрации этого вещества [А] и концентрации этого вещества, которая была израсходована на реакцию к моменту установления равновесия (условно обозначим ее X (А) . Таким образом, выражение для исходной концентрации вещества А может быть представлено в виде: Сисх(А) = [А] + Х(А).
а) Для определения Сисх(N2) и Сисх(Н2) обращаемся к уравнению реакции, согласно которому на образование 2 моль NH3 требуется 1 моль N2 и 3 моль Н2. Но поскольку равновесная концентрация NH3 равна 6 моль/л, то при этом было израсходовано 6/2 = 3 моль N2 и 3×(6 / 2) = 9 моль Н2.
б) Рассчитаем Сисх(N2) и Сисх(Н2):
Сисх(Н2) = [Н2] + Х(Н2) = 2 + 9 = 11 моль/л,
Cисх(N2) = [N2] + X(N2) = 4 + 3 = 7 моль/л.
Ответ: константа равновесия реакции равна 1,1. Исходные концентрации Н2 и N2 составляют 11 моль/л и 7 моль/л соответственно.
Пример 5. Установите направление смещения равновесия в системе
2Н2О(г)+ 2О2(г) ⇄ 2Н2О2 (г), ∆ Н = – 483,7 кДж
при понижении температуры и уменьшении общего давления.
Р е ш е н и е. Влияние внешнего воздействия на состояние химического равновесия в системах, в которых протекают обратимые реакции, оценивается с помощью принципа Ле Шателье-Брауна.
1) Рассматриваем влияние температуры на состояние равновесия в данной системе. Термохимическое уравнение реакции показывает, что ∆Н < 0, следовательно, прямая реакция экзотермическая. При понижении температуры согласно принципу Ле Шателье-Брауна система будет стремиться ослабить внешнее воздействие (т.е. повысить Т), а это возможно за счет реакции, протекающей с выделением теплоты, т.е. экзотермической реакции. Следовательно, понижение температуры приведет к смещению равновесия в направлении протекания прямой реакции.
2) Оцениваем влияние изменения давления на состояние равновесия в данной системе. Из уравнения реакции видно, что прямая реакция сопровождается уменьшением объема системы 2V (Н2О) + 2V (О2) ≠ 2V (Н2О2), т.е. ∆V ≠ 0. Поэтому общее давление (Робщ) будет влиять на состояние равновесия в данной системе. Уменьшение Робщ согласно принципу Ле Шателье-Брауна вызовет противодействие системы (увеличение Робщ) за счет смещения равновесия в сторону протекания реакции, сопровождающейся увеличением Робщ, т.е. в сторону обратной реакции. Действительно, обратная реакция приводит к увеличению числа моль газообразных веществ в системе, а это значит, что при протекании обратной реакции Робщ в системе увеличивается.