Спектры щелочных элементов.
Щелочные металлы одновалентны и их сравнительно легко ионизировать. Если атом щелочного металла имеет всего z электронов, то можно утверждать, что z-1 электронов образуют структуру атома благородного атома, а последний электрон связан с этими электронами и ядром весьма слабо. Таким образом, первые z-1 электронов и ядро образуют остов с зарядом +e, в эффективном поле которого движется электрон, называемый валентным.
Таким образом, щелочные атомы являются водородоподобными атомами, однако не полностью. Дело в том, что внешний электрон несколько деформирует оболочку первых z-1 электронов и несколько искажает их поле. Поэтому потенциальную энергию валентного электрона можно представить в виде 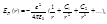 где
где 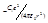 ,
,  - поправки, учитывающие отличие поля атомов щелочных металлов от поля атома водорода. Можно показать, что энергия зависит не только от квантового числа n, но и от орбитального квантового числа l.
- поправки, учитывающие отличие поля атомов щелочных металлов от поля атома водорода. Можно показать, что энергия зависит не только от квантового числа n, но и от орбитального квантового числа l.
Зависимость энергии от орбитального квантового числа составляет принципиальное отличие уровней энергии атомов щелочных металлов от уровней энергии атома водорода. Схему уровней энергии атомов щелочных металлов нельзя представить в функции лишь одного главного квантового числа: уровни энергии, соответствующие одному и тому же квантовому числу, но с различными орбитальными числами, не совпадают друг с другом.
Излучение происходит в результате перехода оптического электрона с одного энергетического уровня на другой. Однако не все переходы возможны. Главное квантовое число может изменяться на любое значение, а орбитальное квантовое число – лишь на единицу.
Это означает, что возможны переходы лишь между соседними по l уровнями, т. е. Между s- и p-состояниями, между p- и d- состояниями и т. д.
 |
Наибольшее число атомов в соответствии с распределением Больцмана находится в низшем энергетическом состоянии.
Поскольку при переходах главное квантовое число n может изменяться на любое значение, допустимы переходы в состояние 2s из любых p-состояние. Получающаяся в результате этих переходов серии линии называется главной. Возможны побочные серии. Серия называется диффузной потому, что ее линии несколько размыты, не очень резки.