Изотермический процесс
При изотермическом процессе выполняется условие: dT=0 или T=const.
Таким образом следует, что это возможно, если 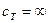 .
.
На основании этого можно определить n для изотермического процесса:
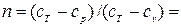
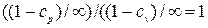
Следовательно, уравнение кривой, выражающей изотермический процесс в системе координат p,v имеет вид:
p v = const или T = const , (4.24)
Связь между параметрами газа для изотермического процесса:
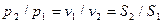 , (4.25)
, (4.25)
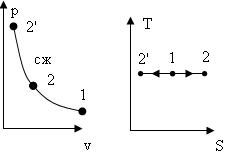
Таким образом, в изотермическом процессе отношение абсолютных давлений обратнопропорционально отношению удельных объемов (рис.4.3):
Как видим, на p,v – диаграмме, изотерма явл. равнобокой гиперболой, для которой оси координат асимптоты.
Работа изменения объема в изотермическом процессе:
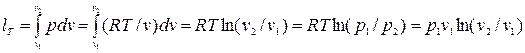 , и т.д. (4.26)
, и т.д. (4.26)
Изменение внутренней энергии изотермического процесса.
т.к. T=const, то dT=0, поэтому: 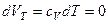 , (4.27)
, (4.27)
Количество теплоты, сообщаемое газу в изотермическом процессе.
Поскольку в изотермическом процессе dU=0, то из 1-го закона ТТД следует, что:
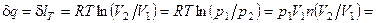
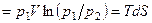 , (4.28)
, (4.28)
т.е. вся теплота изотермического процесса преобразуется
в работу процесса, а внутренняя энергия газа не претер-
певает изменения.
Изменение энтальпии изотермического процесс
Т.к. T=const, то dT=0, поэтому: 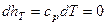 , (4.29)
, (4.29)
Изменение энтропии изотермического процесса.
Рис. 4.3 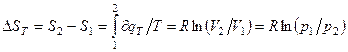 , (4.30)
, (4.30)
Если изотермический процесс протекает в потоке газа, то располагаемая работаможет бытьопределена следующим образом:
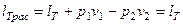 , т.к.
, т.к. 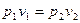 , (4.31)
, (4.31)