Адиабатный процесс
При адиабатном процессе теплообмен рабочего тела с окружающей средой отсутствует, т.е. рабочее тело предполагается изолированным от окружающей среды идеальной тепловой изоляцией.
Эти условия выражаются соотношением q=0, а следовательно и ∂q=0.
Из уравнения: 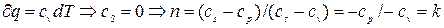 , (4.32)
, (4.32)
Следовательно, уравнение адиабаты имеет вид: рvk=const
где k – показатель адиабаты, который может быть выражен и при помощи уравнения Майера: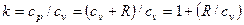 , (4.33)
, (4.33)
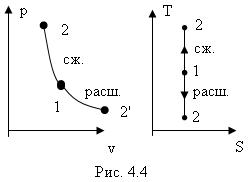
На рис. 4.4 приведен адиабатный процесс. Согласно классической кинематической теории, теплоемкость газа не зависит от температуры, поэтому можно считать, что величина k также не зависит от температуры и определяется числом степеней свободы молекулы.
Для одноатомного газа: k=1,66; Для двухатомного: k=1,41; Для трехатомного : k=1,33.
Связь между параметрами состояния в адиабатном процессе:
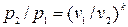 ;
; 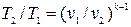 ;
; 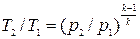 , (4.34)
, (4.34)
 Работа расширения объема рабочего тела в адиабатном процессе.
Работа расширения объема рабочего тела в адиабатном процессе.
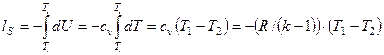 (4.35)
(4.35)
т.к. 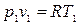 ,
, 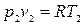 то можно записать:
то можно записать:
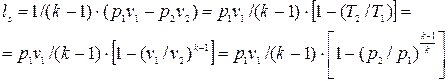 ,(4.36)
,(4.36)
Теплота адиабатного процесса: 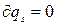
Изменение внутренней энергии адиабатного процесса, как следует из 1-го закона ТТД dus=-∂ls. Следовательно, изменение внутренней энергии газа можно расчитать по (4.36).
Изменение энтальпии адиабатного процесса.
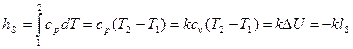 , (4.37)
, (4.37)
или при переменной теплоемкости: 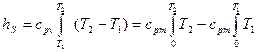 , (4.38)
, (4.38)
Изменение энтропии адиабатного процесса dS=0
Располагаемая работа адиабатного процесса в потоке газа определяется:
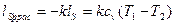 , Дж/кг (4.39)
, Дж/кг (4.39)