Задачи для самостоятельного решения.
1. Газ массой 16 г при давлении 1 МПа и температуре 112 0С занимает объем 1,6 л. Определите, какой это газ.
2. Найдите массу 20 моль серной кислоты (H2SO4).
3. В закрытом сосуде находится газ под давлением 500 кПа. Какое давление установится в этом сосуде, если после открытия крана 4/5 массы газа выйдет наружу, а температура газа не изменится?
4. С определенной массой идеального газа проводят следующие процессы: 1)изобарное нагревание; 2) изотермическое расширение. Изобразите графики процессов в координатных осях (Р,V).
5. В сосуде вместимостью 1 л находится кислород массой 1 г. Определите концентрацию молекул кислорода в сосуде.
6. Определите температуру азота, имеющего массу 2 г, занимающего объем 830 см3 при давлении 0,2 МПа.
7. Распределение молекул по скоростям в пучке, выходящем из небольшого отверстия в сосуде описывается функцией
F = Av3exp(-mv2/ 2kT), где Т- температура газа внутри сосуда. Найдите наиболее вероятные значения: 1) скорости молекул в пучке; сравните полученную величину с наиболее вероятной скоростью молекул в самом сосуде; 2) кинетической энергии
молекул в пучке.
8. В очень высоком вертикальном цилиндрическом сосуде находится углекислый газ при некоторой температуре Т. Считая поле силы тяжести однородным, найдите как изменится давление газа на дно сосуда, если температуру гага увеличить в 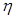 раз.
раз.
9. Некоторое количество водорода находится при температуре 200 К и давлении 400 Па. Газ нагревают до температуры 104К, при которой молекулы водорода полностью распадаются на атомы. Определите давление газа , если его объем и давление не изменились.
10. В колбе находится двухатомный газ. Под действием ультрафиолетового излучения распалось на атомы 12% молекул. При этом в колбе установилось давление 93 кПа. Найдите давление газа в недиссоциированном состоянии.
ЗАНЯТИЕ 7 Основы термодинамики