Пропанон растворяет жир
Следующим важным представителем группы растворителей является пропанон (ацетон).
При сухой перегонке древесины мы получили кальциевую соль уксусной кислоты - "серый древесноуксусный порошок". Тот, кто не проводил этого опыта, легко может приготовить указанную соль путем нейтрализации разбавленного раствора уксусной кислоты (столового уксуса) карбонатом или гидроксидом кальция.
Для получения ацетона поместим несколько граммов древесноуксусного порошка в пробирку из тугоплавкого стекла. Пробирку закроем резиновой пробкой, в отверстие которой вставлена изогнутая стеклянная трубка. Эту трубку охладим с помощью свинцового змеевика. Приемником может служить пробирка, погруженная в ледяную воду. Из-за огнеопасности продукта отводная трубка должна быть не слишком короткой, чтобы расстояние между пламенем и приемником было как можно больше. Кроме того, учтем, что опыт можно проводить только в вытяжном шкафу или на открытом воздухе.
Сильно нагреем пробирку с порошком горелкой Бунзена. Выделяются пары, и в приемнике конденсируется подвижная жидкость, которая в зависимости от степени чистоты исходной соли имеет окраску от желтой до коричневатой. Она состоит, главным образом из ацетона, применяемого в качестве растворителя жиров:
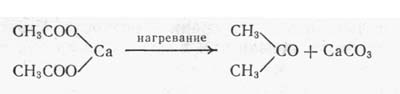
В превосходных свойствах этого растворителя легко убедиться, растворяя небольшие количества жира, воска, лака и других органических веществ. Многие пластмассы тоже растворяются в ацетоне или по крайней мере набухают в нем. Попробуйте обработать им кусочек целлулоида, полистирола или другой пластмассы. Что и говорить - отличный растворитель, к тому же, в отличие от тетрахлорметана, он не вызывает коррозии. Зато очень легко воспламеняется. Чтобы убедиться и в этом, нальем чуть-чуть в чашку и подожжем, осторожно приближая источник огня.
В чистом состоянии ацетон (пропанон) - бесцветная жидкость, кипящая уже при 56,2 °С и имеющая своеобразный, не лишенный приятности запах. Раньше его получали большей частью путем сухой перегонки серого древесноуксусного порошка, а в наши дни производят различными методами, в том числе из уксусной кислоты при пропускании ее паров над катализатором, окислением изопропилового спирта и брожением крахмала под влиянием соответствующих бактерий. В последние годы ацетон получают одновременно с фенолом окольным путем - через стадию образования кумола - из газов нефтехимического производства.
По своему химическому строению ацетон - простейший представитель алканонов (кетонов), родственных алканалям (альдегидам). В то время, как алканали, например метаналь или этаналь, содержат группу С=O на конце молекулы, у алканонов такая группа находится у "внутреннего", т. е. не у крайнего в цепи атома углерода. Алканоны проявляют ненасыщенность в меньшей степени, чем алканали, и поэтому не обнаруживаются с помощью качественных реакций, характерных для алканалей. (Проверить!)
И, наконец, эфир
В заключение рассмотрим эфир, который, помимо его применения в медицине для наркоза, является прекрасным растворителем для жиров и многих других веществ.
Строго говоря, существуют различные простые эфиры, которые так же, как алканали или алканоны, образуют класс соединений со сходными свойствами. Обычный эфир строго должен называться диэтиловым эфиром. Он образуется из двух молекул этанола путем отщепления воды, обычно с помощью концентрированной серной кислоты:
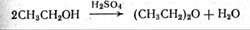
Получим малое количество эфира. Для этого в пробирку нальем около 2 мл денатурата и 1,5 мл концентрированной серной кислоты. Подберем к пробирке пробку с двумя отверстиями. В одно из них вставим маленькую капельную воронку или просто маленькую воронку с удлиненной трубкой, выход из которой вначале закроем с помощью кусочка резинового шланга и зажима. Используя второе отверстие в пробке, присоединим к пробирке устройство для охлаждения паров - такое же, как и при получении этаналя. Приемник надо непременно охлаждать водой со льдом, потому что эфир кипит уже при 34,6 °С! Ввиду его необычайно легкой воспламеняемости, холодильник должен быть как можно длиннее (не меньше 80 см), чтобы между источником огня и приемником было достаточное расстояние. По этой же причине проведем опыт вдали от горючих предметов, на открытом воздухе или в вытяжном шкафу. Нальем в воронку еще около 5 мл денатурата и осторожно нагреем пробирку на асбестированной сетке горелкой Бунзена приблизительно до 140 °С (Температура не должна превышать 145 0С, так как при более высокой (около 170 0С) образуется этен. Даже при работе с малым количеством эфира всегда следует учитывать опасность пожара. Поэтому рекомендуем заменить горелку закрытой электрической плиткой и между источником тепла и приемником установить защитный экран. При использовании капельной воронки надо тщательно смазать и проверить кран. В качестве приемника лучше всего взять плотно присоединенную к холодильнику пробирку с боковым отводом, на который можно надеть резиновый шланг для увеличения расстояния между выходящими парами эфира и источником тепла. Приемник лучше охлаждать смесью льда с солью – Прим. перев). В приемнике конденсируется очень летучий дистиллят, и в случае недостаточного охлаждения мы почувствуем характерный запах эфира. Осторожно приоткрывая зажим, будем постепенно, малыми порциями добавлять спирт. В конце реакции серная кислота все больше разбавляется образующейся водой, в результате чего образование эфира прекращается и перегоняется уже спирт.
При тщательном выполнении опыта мы получим около 4 мл очень подвижной, прозрачной жидкости, которая состоит в основном из эфира. Если несколько капель его нанести на палец, то почувствуешь сильный холод. Дело в том, что эфир быстро испаряется, а теплота испарения отнимается от окружающей его среды.
На химических предприятиях и в больницах при работе с эфиром случались очень сильные взрывы. При длительном соприкосновении с кислородом воздуха и под влиянием солнечного света в эфире образуются легко взрывающиеся перекиси. Поэтому ни в коем случае не будем хранить большее количество эфира. Оно не понадобится нам ни в одном из опытов, рекомендуемых в этой книге. Эфир будет нужен нам только в смеси с двумя частями спирта как растворитель для коллодия. Поэтому остаток эфира сразу разбавим двойным количеством спирта и будем хранить только в виде этой безопасной смеси в надежно закрытой бутылочке из темно-коричневого стекла.
Продолжительное вдыхание паров эфира вызывает потерю сознания, что впервые использовали в 1846 г. Джексон и Мортон для наркоза (Для этой цели эфир во время хирургической операции впервые применил Лонг (США) в 1842 г, но этот эксперимент не был опубликован. – Прим. перев.). Тщательно очищенный эфир и сейчас применяется с этой целью. Однако можно надеяться, что читатели этой книги заслуживают доверия и, конечно, не будут проводить опасных, безответственных и категорически недопустимых собственных опытов, связанных с наркозом.
Завершая этот раздел, посвященный растворителям, следует подчеркнуть, что в следующих частях книги мы еще познакомимся с другими важными растворителями, например, с бензолом и сложными эфирами, прекрасно растворяющими лаки и пластмассы.