КОНСТРУКЦИИ ЭЛЕКТРОЛИЗЕРОВ.
В литературе имеется мало публикаций о конструкциях современных электролизеров
Известно, что используются в основном монополярные ящичные электролизеры с платино-титановыми анодами и графитовыми катодами. При применении электролизеров без диафрагмы выделяющийся на катоде водород загрязняется хлором и кислородом в количествах, превышающих взрывобезопасные пределы. В этом случае газы в электролизере следует разбавлять инертными газами.
При использовании электролизеров с диафрагмой их конструкция усложняется, а напряжение на электролизере возрастает. Однако вследствие разделения анодного и катодного пространств получаемые водород и хлор достаточно чистые и могут быть использованы; облегчаются создание безопасных условий работы и защита окружающей среды от вредных газовых выбросов.
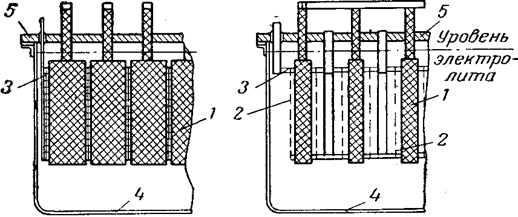
Рис. 8 Хлоратный электролизер Ангела:
1 — графитовые аноды; 2 — катоды; 3 — катодная рама;
4 — корпус электролизера; 5 — крышка.
Сообщается о применении для получения хлорной кислоты электролизеров фильтр-прессного типа с биполярным включением электродов. Рамы электролизера, изготовленные из поливинилхлорида, снабжены диафрагмой из сетки, выполненной из полимерных материалов. Аноды покрыты платиновой фольгой, катоды — серебряные. Электролизер на нагрузку 5 кА работал при плотности тока 2,5 кА/м и напряжении на ячейке 4,4 В; выход по току составил около 60%.
Предложено также получать хлорную кислоту анодным окислением водных растворов хлоратов в трехкамерном электролизере (рис. 9)с двумя ионообменными мембранами. При применении платиновых или платино-титановых анодов в анодном пространстве можно получить достаточно чистую 2 н. кислоту, а в катодном пространстве — раствор щелочи. При этом в качестве катода можно использовать обычную сталь.
Хотя хлорная кислота, полученная электрохимическим окислением растворов НС1 или С12 в НС104, используется для производства различных перхлоратов, часто с успехом применяется также и обратный процесс — получение хлорной кислоты из перхлоратов щелочных или щелочноземельных металлов. В этом случае исходным сырьем обычно служит перхлорат натрия, получаемый электрохимическим окислением хлората натрия. Иногда перхлорат
 |
натрия переводят в перхлораты калия, бария или других металлов обменным разложением.
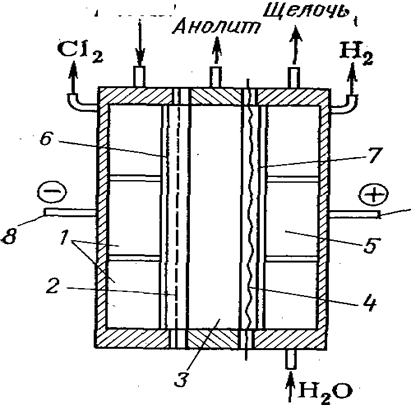
Рис.8. Трехкамерный электролизер:
/ — анодная камера; 2 — пористая диафрагма, 3 — центральная камера; 4 — катионообменная мембрана; 5 — катодная камера; 6 — катод; анод; 8, 9 — соответственно катодная и анодная шины.
Один из первых промышленных методов получения хлорной кислоты был основан на реакции между перхлоратом калия и серной кислотой
КС1O4 + H2S04 = НС104 + KHS04 (3)
Хлорную кислоту отгоняли дистилляцией в вакууме. При этом в случае применения достаточно концентрированной серной кислоты получали хлорную кислоту высокой концентрации, близкую к безводной. Реализация этого процесса в промышленности связана со сложностью аппаратурного оформления, ограниченностью материалов, пригодных для работы в среде хлорной и серной кислот, и необходимостью проведения отгонки хлорной кислоты в вакууме. Поэтому применение процесса целесообразно только для получения безводной хлорной кислоты. Для получения водных растворов хлорной кислоты предложено взаимодействие перхлората калия с кремнефтористоводородной кислотой в водном растворе
КС104 + HsiF6 = НС104 + KsiF6 (4)
При этом помимо растворов хлорной кислоты получают осадок плохо растворимого кремнефторида калия. После фильтрования осадка разбавленные растворы хлорной кислоты можно подвергать концентрированию и затем возгонке в виде азеотропной кислоты концентрацией около 72%. Однако получаемые осадки кремнефторида калия плохо фильтруются, что затрудняет практическое использование этого метода.
Для получения безводной хлорной кислоты, помимо указанного взаимодействия солей хлорной кислоты с сильными неорганическими кислотами, применяют перегонку в вакууме смеси технической, примерно 70%-ной хлорной кислоты с трех—четырехкратным по объему количеством дымящейся серной кислоты.
Предложен непрерывный процесс получения безводной хлорной кислоты обезвоживанием азеотропа олеумом с вакуумной отгонкой. Схема такой установки показана на рис. 10. На рисунке изображена лабораторная установка, однако по такому же принципу может быть создана и более крупная установка. В самом аппарате всегда находится небольшое количество подвергаемой обработке смеси кислот, что уменьшает опасность, связанную с возможными взрывами. При смешении кислот требуется охлаждение смесителя во избежание перегрева и возможного термического разложения хлорной кислоты.
|
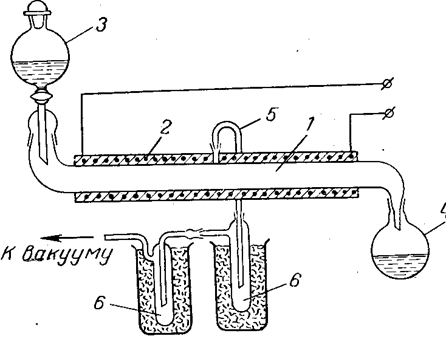
Рис. 10. Схема установки для получения безводной хлорной кислоты:
1 — труба из кварцевого стекла или пирекса;
2 — электрообогрев; з — капельная воронка;
4 — приемник отработанной смеси кислот;
5 — трубка для отвода паров хлорной кислоты;
6 — приемник-конденсатор безводной хлорной кислоты.