Способы выражения концентраций в титриметрическом анализе
В титриметрическом анализе используют следующие основные способы выражения концентраций растворов.
Молярная концентрация с(А) —- количество растворенного вещества А в молях, содержащееся в одном литре раствора:
 , моль/л
, моль/л
где m(А) — масса растворенного вещества А, г
М(А.) — молярная масса растворенного вещества А, г/моль.
Молярная концентрация эквивалента с(1/Z А), или нормальность (старое название),— количество растворенного вещества А в молях, соответствующее эквиваленту А, содержащееся в одном литре раствора:
 , моль/л
, моль/л
где 1/Z — фактор эквивалентности; рассчитывается для каждого вещества на основании стехиометрии реакции;
M(1/ZА) — молярная масса эквивалента растворенного вещества А, г/моль.
Титр T(А) растворенного вещества А — это масса растворенного вещества А в граммах, содержащаяся в одном миллилитре раствора:
 , г/мл
, г/мл
где объем раствора V измеряется в мл.
Титр раствора по определяемому веществу X, или титриметрический фактор пересчета t(Т/Х), — масса титруемого вещества, взаимодействующая с одним миллилитром титранта Т:
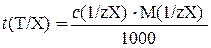 , г/мл
, г/мл
Поправочный коэффициент К — число, выражающее отношение действительной (практической) концентрации c(1/zA) вещества А в растворе к его заданной (теоретической) концентрации с(1/zА)теор:
К = c(1/zA)пр/c(1/zA)теор
Лабораторная работа № 1
Определение содержания Na2CO3 и NaHCO3