Решение.
Напишем уравнение реакции:+ KOH - HCOOK + H2O.
рН в точке эквивалентности определяется гидролизом соли.
HCOO- + H2O - HCOOH + OH-, рН>7.



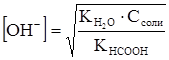



В точке эквивалентности объем титранта (КОН) равен:
 мл
мл
 моль/л
моль/л
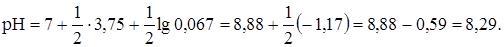
Точка начала скачка соответствует рН нейтрализации на 99,9%, т.е. раствор кислоты недотитрован на 0,1%.
Если 10 мл составляют 100%
х - 99,9%
х = 9,99 мл.
Было кислоты 0,1∙20 = 2 ммоль-экв
Добавлено щелочи 0,2∙9,99 = 1,998 ммоль-экв
Осталось кислоты 2-1,998 = 0,002 ммоль-экв
Образовалось соли 1,998 ммоль-экв
В данной точке титрования раствор представляет собой буферную систему: слабая кислота и соль этой кислоты.
Расчет рН проводим, исходя из константы кислотности.

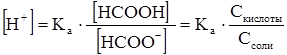

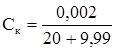
 ,
,
так как объемы сокращаются, то вместо концентрации можно подставлять количество вещества эквивалентов кислоты и соли.
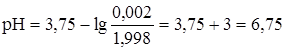 .
.
Концентрацию кислоты и соли можно заменить прямо процентом оттировки.
 .
.
В точке конца скачка раствор перетитрован на 0,1%, т.е. добавлено 10,01 мл 0,2 н. КОН:


 ;
; 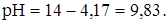
Таким образом, при титровании муравьиной кислоты раствором гидроксида калия рН в точке эквивалентности равен 8,29, область скачка лежит в интервалах рН от 6,75 до 9,83. Индикатор - фенолфталеин (рТинд. = 9).
При проведении количественных расчетов в методе кислотно-основного титрования используется закон эквивалентов. Особое внимание следует обратить на используемые индикаторы, с тем чтобы правильно определить фактор эквивалентности реагирующих веществ.