Теоретические сведения. - Лабораторная Работа, раздел Химия, По курсу "Химия" для студентов нехимических специальностей Понятие «Химическое Равновесие» Применимо Только К Обратимым Реакциям....
Понятие «химическое равновесие» применимо только к обратимым реакциям. Химическим равновесием называют такое состояние реагирующей системы, при котором скорость прямой реакции равна скорости обратной реакции
равна скорости обратной реакции 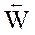 . Равенство
. Равенство  является кинетическим условием химического равновесия.
является кинетическим условием химического равновесия.
Химическое равновесие характеризуется постоянством величин энергии Гиббса системы GT. Равенство ΔGT = 0 является термодинамическим условием химического равновесия.
Химическое равновесие характеризуется постоянным для данных условий соотношением равновесных концентраций всех веществ, участвующих во взаимодействии.
Величина, равная отношению произведения равновесных концентраций продуктов реакции к произведению равновесных концентраций исходных веществ, взятых в степенях, равных их стехиометрическим коэффициентам, называется константой равновесия. Для обратимой реакции
Н2(г) + I2(г)↔2HI(г)
константа равновесия имеет вид
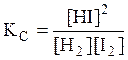 или
или 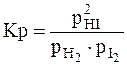 ,
,
где КС, КР – константы равновесия в случае отношения молярных концентраций и парциальных давлений соответственно; [HI], [H2], [I2] – равновесные молярные концентрации; ,
,  - парциальные давления.
- парциальные давления.
Константа равновесия зависит от природы реагентов, температуры и не зависит от исходной концентрации веществ в сиcтеме. Показывает на сколько скорость прямой реакции больше скорости обратной; характеризует глубину протекания процесса.
Константа равновесия связана со стандартной энергией Гиббса данной реакции (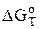 ) следующим соотношением
) следующим соотношением
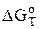 = -RTlnKС
= -RTlnKС
где R — универсальная газовая постоянная [8,31 Дж/(моль.К)]; Т — абсолютная температура, К; КС — константа равновесия.
Если КС>1 (ΔG<0), то в равновесной системе преобладают продукты реакции, а если КС<1 (ΔG>0), то в равновесной системе преобладают исходные вещества.
Химическое равновесие остается неизменным до тех пор, пока постоянны параметры (p,T,CM), при которых оно установилось. При изменении условий равновесие нарушается. Через некоторое время в системе вновь наступает равновесие, характеризующееся новым равенством скоростей и новыми равновесными концентрациями всех веществ.
В общем случае, направление смещения равновесия определяется принципом Ле Шателье: если на систему, находящуюся в равновесии, оказать внешнее воздействие, то равновесие сместится в сторону, противодействующую этому воздействию.
1. При увеличении концентрации реагирующих веществ, равновесие сместится в сторону продуктов реакции, а при уменьшении концентрации исходных веществ – в сторону их образования.
2. При увеличении общего давления в системе равновесие смещается в сторону меньшего числа моль газообразных веществ, а при уменьшении – в сторону большего числа моль газообразных веществ.
3. Увеличение температуры в системе смещает равновесие в сторону эндотермической реакции, а уменьшение – в сторону экзотермической реакции.
Все темы данного раздела:
Тверь. Типография ТГТУ
Ó Тверской государственный
технический университет, 2002
ВВЕДЕНИЕ
Лабораторные работы являются
Общие правила работы в лаборатории
Выполнение лабораторных работ связано с использованием разнообразного оборудования, химических реактивов, химической посуды, которые при неумелом обращении способны нанести травмы и отравления.
Реактивы и правила обращения с реактивами
1. По степени чистоты реактивы делятся на технические (техн.), чистые (ч.), чистые для анализа (ч.д.а.), химически чистые (х.ч.).
2. Необходимые для работы реактивы выставл
Меры предосторожности при работе в лаборатории
1. К проведению опыта следует приступать после внимательного ознакомления с его содержанием и уяснения техники его выполнения.
2. Опыты с ядовитыми и неприятно пахнущими в
Оказание первой помощи
1. При попадании на кожу концентрированных кислотследует тотчас же смыть ее большим количеством воды из крана, а затем обработать пораженный участок 2% -м раствором
Уравнение Бойля-Мариотта и Гей-Люссака
;
где V – объем газа, измеренный при реальных условиях, т.е. при атмосферном давлении Р и температуре Т; V
Молярную массу газа можно вычислить, пользуясь уравнением Клапейрона - Менделеева
, или ,
где Р – давление,
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ.
Оборудование: эвдиометр, штатив, колба, соединительные трубки, кристаллизатор, термометр, барометр, соляная кислота (HCl 1:2), таблетка цинка.
РАСЧЕТ МОЛЯРНОЙ МАССЫ ЭКВИВАЛЕНТА ЦИНКА.
1. Приводим объем выделившегося водорода к нормальным условиям (V он.у.) по уравнению Бойля-Мариотта и Гей-Люссака
Опыт №1. Приготовление раствора заданной концентрации.
Задание: из сухой соли и дистиллированной воды приготовить, согласно варианту (см.табл.) раствор заданной концентрации. Рассчитать массу сухой соли и объем воды, необходимые для приготовлени
Опыт №2.
Задание: Из раствора, полученного в опыте №1 и дистиллированной воды приготовить раствор заданной концентрации (см.таблицу), используя правило «креста». Рассчитать объем раствора и объем вод
Теоретические сведения
Химический процесс, фазовые превращения сопровождаются энергетическими изменениями. Законы взаимного превращения различных видов энергии, а также состояние химического равновесия и
Результаты опыта
Время τ, мин
0,5
1,0
1,5
2,0
2,5
3,0
3,5
4,0
4
Закон действующих масс может быть записан
, (1)
где W- скорость химической реакции; k – константа скорости; С
Закон действующих масс имеет вид
где W- скорость химической реакции; k – константа скорости; С
Опыт №4. Влияние температуры на скорость химической реакции в гомогенной системе.
Для выполнения опыта используется термостат – стакан с крышкой, в котором имеются три отверстия для термометра и двух пробирок.
Выполнение работы
Опыт 1. Влияние изменения концентрации веществ на химическое равновесие.
Задание: изучить влияние изменения концентрации веществ на химическое равновесие в системе
FeCl3 + 3KSCN <==>Fe(SCN)3 + 3KCl красн
ОПРЕДЕЛЕНИЕ МОЛЕКУЛЯРНОЙ МАССЫ РАСТВОРЕННОГО ВЕЩЕСТВА МЕТОДОМ КРИОСКОПИИ.
(Глинка Н.Л.,2000, 7.1-7.2, Коровин Н.В.,2000, §8.1 )
Цель работы: определить методом криоскопии молекулярную мас
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Исходный раствор "А": 20%, =0.97 г/см3
Заданные растворы: С1
КОЛЛОИДНЫЕ РАСТВОРЫ
(Глинка Н.Л., 2000, глава 10, Коровин Н.В., 2000, §6.3, §8.7)
Цель работы:знакомство с методами получения коллоидных растворов и их свойствами.
Опыт №4. Определение порога коагуляции золя гидроксида железа.
Выполнение работы:
1. Подготовить 3 серии пробирок по 4 пробирки в каждой.
2. Налить в 4 пробирки соответствующие количе
Теоретические сведения.
Электролитами называют вещества, диссоциирующие в растворах или расплавах на ионы. Растворы и расплавы электролитов проводят электрический ток. Распад молекул на ионы называют электролитической дис
Все электролиты делят на сильные и слабые.
Сильные электролиты
Это вещества, которые при растворении в воде практически полностью распадаются на ионы. Как правило, к сильным электролитам относятся вещества с
В зависимости от pH раствора
Название
Окраска индикатора в среде
Кислая
[H+] > [OH-]
рН < 7
Н
PO43- + HOH → HPO42- + OH- pH>7 – среда щелочная
Если основание и кислота, образующие соль, являются не только слабыми электролитами, но и малорастворимы или неустойчивы и разлагаются с образованием летучих продуктов, то в этом случае гидролиз со
Опыт №1. Определение рН водных растворов электролитов.
Цель работы: определение водородного показателя среды методами визуального колориметрирования и рН-метрии.
№ п/п
Б) Получение амфотерного гидроксида и исследование его свойств.
Ход работы: получить в двух пробирках осадок гидроксида металла взаимодействием растворимой соли со щелочью: поместить по 5 капель соли в каждую пробирку и добавить по 1-2 капли (стро
Опыт №3. Гидролиз солей.
Цель работы: опытным путем изучить реакцию гидролиза солей и смещение равновесия гидролиза.
а) Реакция cреды в растворах различных со
Б) Влияние температуры на равновесие гидролиза соли.
Цель опыта: Экспериментально установить влияние температуры на равновесие в растворе гидролизующейся соли.
Ход работы: В пробирку напо
Смещение равновесия гидролиза при изменении температуры
Ионно-молекулярное уравнение гидролиза СН3 СОО Na : СН3 СОО- + НОН <== > CH3COOH + OH-
Изме
Порядок выполнения работы
1. Заполнить бюретку раствором Трилона Б с концентрацией 0.025 моль-экв/л.
2. Взять пипеткой пробу воды 50 мл и поместить в коническую колбу. Добавить в воду 1 мл аммиачного буферного раст
Лабораторная работа №10
ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ РЕАКЦИИ (ОВР)
(Глинка Н.Л.,2000, 9.1-9.3, Коровин Н.В., 2000, §9.1 )
Цель работы: опытным путем и
Теоретические сведения.
Степень окисления - это условный заряд атома в молекуле, вычисленный в предположении, что молекула состоит из ионов и в целом электронейтральна.
Наиболее электроотр
Опыт 1. Окислительные свойства перманганата калия в зависимости от реакции среды.
Ход работы: В три пробирки налейте по 5 капель раствора перманганата калия. В одну из них прибавьте 2 капли 2н раствора серной кислоты, во вторую - 2 капли концентрированного раствора щелочи
Опыт №2. Химические свойства металлов. Взаимодействие металлов с концентрированными и разбавленными кислотами.
Кислота
Активные металлы H2 Неактивные металлы
Li Al
HCl(к), (р)
Теоретические сведения
Под электрохимическими процессами понимаются процессы, сопровождающиеся превращением химической энергии в электрическую и электрической энергии в химическую.
Электрохимические процессы отн
Лабораторная работа №12
КОРРОЗИЯ МЕТАЛЛОВ
(Глинка Н.Л., 2000, 38.5, Коровин Н.В., 2000, глава 10.)
Цель работы: опытным пу
Опыт 1.Качественная реакция на ион Fe2+.
При коррозии металлического железа его атомы теряют электроны и превращаются в ионы двухвалентного железа Fe2+. Присутствие в системе с корродирующим железом ионов Fe2+ опреде
Опыт 2. Коррозия оцинкованного (Fe-Zn) и луженого (Fe-Sn) железа в кислой среде.
Выполнение работы. В две пробирки налейте на ½ их объема дистиллированной воды, добавьте в каждую по 3 капли 2н раствора серной кислоты и по 2 капли К3[Fe(CN)6
Опыт 3. Зависимость скорости коррозии железа от рН среды.
Выполнение работы В пять пробирок налейте на ½ их объема следующих растворов: в первую - хлорида натрия (рН 7); во вторую - хлорида натрия и две капли 2н раствора NaOH (pH 12);
Зависимость скорости коррозии железа от рН среды.
№ п/п
Состав раствора
рН
Последовательность окрашивания
Вид деполяриризации
Ион среды: активатор или
Теоретические сведения.
Электролиз — это окислительно-восстановительный процесс, протекающий на электродах при прохождении постоянного электрического тока через раствор или расплав электролитов.
Законы электролиза.
Количественные соотношения при электролизе между выделившимся веществом и прошедшим через электролит электричеством выражаются двумя законами Фарадея.
I закон Фарадея.
Опыт №1. Электролиз раствора CuSO4 с угольным и медным анодами.
Выполнение работы.Налить в электролизер 0,5 н. раствор CuSO4, опустить в него графитовые электроды и пропустить через раствор электрический ток. Через несколько минут пр
Опыт №2. Электролиз раствора KI с графитовым анодом.
В электролизер наливают раствор KI, в оба колена добавляют по 2-3 капли фенолфталеина и опускают графитовые электроды, которые подсоединяют к выпрямителю. Опишите свои наблюдения. Как окрашен раств
Опыт №3. Электролиз раствора Na2SO4 с графитовым анодом.
В U- образный сосуд наливают раствор Na2SO4 и добавляют по 2-3 капли раствора лакмуса в оба колена электролизера. Затем опускают электроды и подсоединяют к выпрямителю. Опишит
СВИНЦОВЫЙ АККУМУЛЯТОР
(Глинка Н.Л.,2000, 38.4, Коровин Н.В., 2000, §9.8)
Цель работы:изучение работы свинцового аккумулятора.
Теоретические сведения.
Устройства, в которых электрическая энергия превращается в химическую, а химическая – снова в электрическую, называют аккумуляторами.
Готовый к употреблению свинцовый аккумулятор состоит
Pb, PbO2, PbSO4 │H2SO4 │ PbSO4, PbO2, Pb
Для зарядки (или заряда) аккумулятор подключают к внешнему источнику тока (плюсом к плюсу и минусом к минусу).
Зарядка:
Рb + РbO2 + 2Н2SO4= 2PbSO4 + 2Н2O
Электроны, отдаваемые атомами металлического свинца при окислении, принимаются атомами свинца РbО2 при восстановлении; электроны передаются от одного электрода к другому по внешней цепи
Опыт 1. Изучение качественного состава водной вытяжки портландцемента.
Насыпьте в пробирку небольшую порцию порошка цемента (0,5 – 1 см. Высотой), прилейте дистиллированной воды до половины объема и хорошо перемешайте стеклянной палочкой. Дайте образовавшейся суспензи
Опыт 2. Проведение частичного растворения и разрушения портландцемента с помощью кислоты.
В пробирку насыпать около 1 см3 порошка портландцемента и прилить 2-3 капли концентрированной соляной кислоты. Смесь осторожно (в вытяжном шкафу) перемешать стеклянной палочкой и наблюда
Опыт 3. Качественная реакция на ион Al3+.
Взять полоску фильтровальной бумаги, нанести 2 капли исследуемого раствора, подержать 2-3 минуты над открытой склянкой с концентрированным раствором аммиака (NH3·H2O). Эта реа
 равна скорости обратной реакции
равна скорости обратной реакции 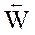 . Равенство
. Равенство  является кинетическим условием химического равновесия.
является кинетическим условием химического равновесия.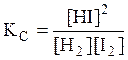 или
или 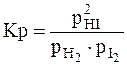 ,
, ,
,  - парциальные давления.
- парциальные давления.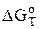 ) следующим соотношением
) следующим соотношением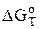 = -RTlnKС
= -RTlnKС






Новости и инфо для студентов