Дослід 2. Вплив температури на швидкість реакції
Мета: обчислити відносні швидкості реакцій та середнє значення температурного коефіцієнту γ. У висновку провести паралель з правилом Вант-Гоффа.
Обладнання та реактиви: штатив із пробірками, секундомір, розчин з молярною концентрацією натрій тіосульфату 0,25 моль/л, розчин з молярною концентрацією сульфатної кислоти 0,25 моль/л.
Хід роботи.У три пробірки, які позначені маркером, налийте по 3 мл розчину сульфатної кислоти, а в три інші – по 3 мл розчину натрій тіосульфату. Помістіть всі пробірки в склянку з водою. Виміряйте температуру води в склянці і злийте вміст першої пари пробірок (кислоту з тіосульфатом). Відзначте час від моменту зливання до помутніння розчину. Склянку з іншими пробірками нагрійте на 100С і злийте вміст другої пари пробірок. Аналогічні дії проведіть з третьою парою пробірок при температурі, яка вища за кімнатну на 200С. Результати зведіть у таблицю. Обчисліть середнє значення температурного коефіцієнту γ та проведіть паралель з правилом Вант-Гоффа.
Таблиця 2.3
| Температура Т, 0С | Час перебігу реакції, t, с | Відносна швидкість реакції, 1/t | γ; 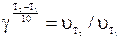
|
| Ткімнатна | |||
| Ткімнатна + 10 | |||
| Ткімнатна + 20 |
______________________________________________________________________________________________________________________________________________