Визначення метала за молярною масою його еквівалента
Мета роботи: визначити молярну масу еквівалента невідомого металу
Згадайте основні класи хімічних сполук:
| Основні оксиди(склад) | Кислотні оксиди(склад) | Основи(склад) | Кислоти(склад) | Солі(склад) |
 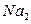 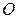
|  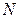 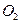
|  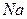 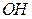
|  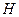 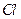
|  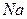 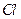
|
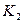 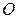
| 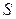 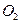
| 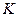 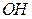
| 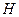 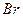
| 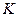 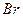
|
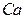 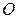
| 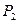 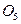
| 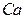 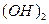
| 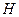 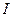
| 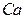 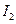
|
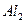 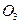 (амф.) (амф.)
| 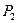 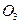
| 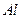 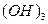
| 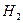 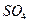
| 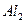 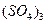
|
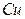 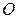
| 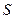 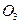
| 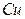 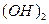
| 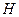 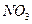
| 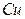 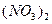
|
| Елемент метал Оксиген | Елемент неметал Оксиген | Елемент метал гідроксил | кислотний Гідроген залишок | Елемент кислотний метал залишок |
Дайте відповіді на запитання(домашня підготовка):
| № | Запитання | Ваші відповіді |
| 1. | Назвіть характеристичну групу кислот. | |
| 2. | Назвіть характеристичну групу основ. | |
| 3. | До якого класу належить 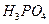 ? Дайте назву. ? Дайте назву.
| |
| 4. | До якого класу належить 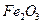 ? Дайте назву. ? Дайте назву.
| |
| 5. | До якого класу належить 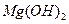 ? Дайте назву. ? Дайте назву.
| |
| 6. | До якого класу належить 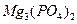 ? Дайте назву. ? Дайте назву.
|
Щоб виконати роботу, Ви повинні знати:
- Універсальний газовий закон:
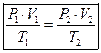
- Формулу розрахунку молярної маси еквівалента елемента:
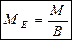 Запам’ятай!
Запам’ятай! 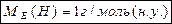
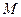 - молярна маса елемента (дивись в періодичній системі Д.І.Менделєєва)
- молярна маса елемента (дивись в періодичній системі Д.І.Менделєєва) 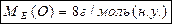
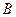 - валентність елемента.
- валентність елемента.
Наприклад: 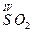 , валентність Сульфуру дорівнює IV;
, валентність Сульфуру дорівнює IV; 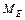 (
(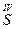 ) = M(S)/B = 32/4 = 8 г/моль;
) = M(S)/B = 32/4 = 8 г/моль;
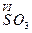 , валентність Сульфуру дорівнює VI;
, валентність Сульфуру дорівнює VI; 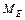 (
(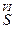 ) = M(S)/B = 32/6 = 5,3 г/моль.
) = M(S)/B = 32/6 = 5,3 г/моль.
- Способи розрахунку молярної маси еквівалента кислоти
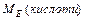 :
:
Спосіб а) 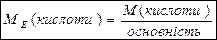 Основність кислоти– це кількість катіонів Гідрогену в кислоті,
Основність кислоти– це кількість катіонів Гідрогену в кислоті,
які витіснились металом. Наприклад: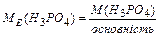 :
: 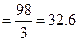 г/моль
г/моль
Спосіб б): 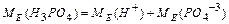 =1+
=1+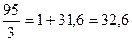 г/моль
г/моль
- Способи розрахунку молярної маси еквівалента основ
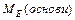 :
:
Спосіб а):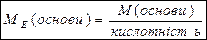 Кислотність основи –це кількість
Кислотність основи –це кількість 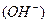 груп у молекулі основи, що вступили в
груп у молекулі основи, що вступили в
реакцію.Наприклад: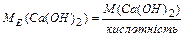
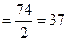 г/моль
г/моль
Спосіб б):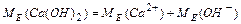 =
=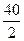 +17=37 г/моль
+17=37 г/моль
- Способи розрахунку молярної маси еквівалента оксиду
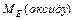 :
: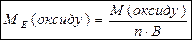
Спосіб а): 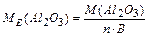 ; n – кількість атомів елемента в молекулі; В – його валентність.
; n – кількість атомів елемента в молекулі; В – його валентність.
Наприклад: 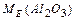 =
= 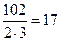 г/моль
г/моль
Спосіб б): 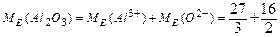 =17 г/моль
=17 г/моль
6. Способи розрахунку молярної маси еквівалента солі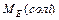 :
: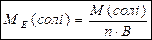
Спосіб а): 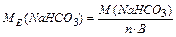 ; n – кількість атомів металу в молекулі; В – його валентність.
; n – кількість атомів металу в молекулі; В – його валентність.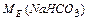
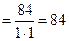 г/моль
г/моль
Спосіб б): 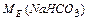 =
=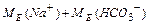 =23+61=84 г/моль
=23+61=84 г/моль
7. Еквівалентний об’єм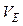 – це об’єм одного еквівалента газоподібної речовини за нормальних умов(н.у.)
– це об’єм одного еквівалента газоподібної речовини за нормальних умов(н.у.)
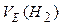 =11,2 л/моль;
=11,2 л/моль; 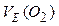 =5,6 л/моль
=5,6 л/моль
8. Закон еквівалентів (закон співвідношення молярних мас еквівалентів реагуючих сполук А і В):