Маси реагуючих речовин пропорційні молярним масам їх еквівлентів.
Закон еквівалентів виражений через маси: 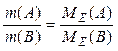
Задача:
Обчисліть молярну масу еквівалента металу в оксиді, який містить 52% металу. Назвіть цей метал і складіть формулу
оксиду,враховуючи, що валентність металу дорівнює VI.
Хід рішення задачі:
1.Знаходимо відсоток Оксигену в оксиді: 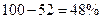 , або 48г Оксигену у 100г оксиду.
, або 48г Оксигену у 100г оксиду.
2.За законом еквівалентних співвідношень обчислюємо молярну масу еквівалента металу:
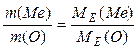
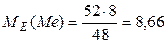 г/моль
г/моль
3.За формулою (1) визначаємо молярну масу металу:
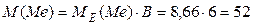 г/моль
г/моль
Висновок: Цей VI-ти валентний метал -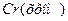 .Його оксид
.Його оксид 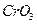 .
.
8.2 Закон еквівалентів, у разі присутності в реакції газоподібної сполуки (В)
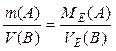 ;
;
Запам’ятай!
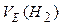 =11,2 л/моль (н.у.) =11,2 л/моль (н.у.)
| 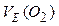 =5,6 л/моль (н.у.) =5,6 л/моль (н.у.)
|
Задача :
На відновлення 7,09 г оксиду металу потрібно 2,24 л водню (н.у.). Обчисліть молярну масу еквівалента металу та його оксиду.
Розв’язання задачі: Записуємо формулу закону еквівалентів і обчислимо молярну масу еквівалента оксиду:
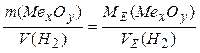
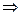
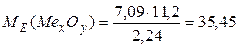 г/моль
г/моль
Визначаємо молярну масу еквівалента металу:
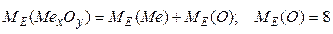 г/моль:
г/моль:
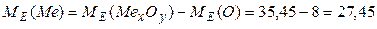 г/моль
г/моль
8.3 Закон еквівалентів у випадку, коли і А, і В – газоподібні речовини
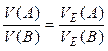
Хід рішення за цією формулою подібний двом попереднім.
Література [дивись с. 6]:
[1] с. 3-10; [2] с. 11-17; [3] с. 18-21; [4] с. 11-14 [5] с. 8-11
Завдання для самостійної роботи:
| № | Запитання | Ваші відповіді |
| 1. | Запишіть математичний вираз універсального газового закону | |
| 2. | Розрахуйте молярну масу еквівалента 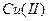
| |
| 3. | Розрахуйте молярну масу еквівалента 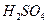
| |
| 4. | Розрахуйте молярну масу еквівалента 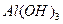
| |
| 5. | Розрахуйте молярну масу еквівалента 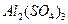
| |
| 6. | Розрахуйте молярну масу еквівалента 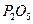
|
Самостійно вирішити задачі № 1, 6, 10, 18 [5. с. 10-11]
Виконайте експеримент та заповніть лабораторний журнал:
Дотримуйтесь правил техніки безпеки! (стор5)
| № | Зміст роботи | Рівняння реакцій, спостереження, розрахунки |
· В одне коліно дворогої пробірки покладіть наважку метала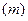 . У друге—налийте 2-3мл . У друге—налийте 2-3мл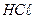 (1:1,5)
· Приєднайте дворогу пробірку до приладу. Перевірте прилад на герметичність.
· Запишіть (1:1,5)
· Приєднайте дворогу пробірку до приладу. Перевірте прилад на герметичність.
· Запишіть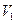 —рівень води у бюретці. Проведіть реакцію.
· Пересуваючи воронку, зрівняйте рівень води в бюретці та воронці.
· Запишіть кінцевий рівень води в бюретці —рівень води у бюретці. Проведіть реакцію.
· Пересуваючи воронку, зрівняйте рівень води в бюретці та воронці.
· Запишіть кінцевий рівень води в бюретці 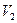 .
· Визначте температуру в лабораторії.
· Визначте атмосферний тиск. .
· Визначте температуру в лабораторії.
· Визначте атмосферний тиск.
| 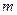 (маса наважки металу) = (маса наважки металу) =
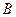 (валентність металу) = (валентність металу) =
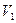 (вихідний рівень води в бюретці) = (вихідний рівень води в бюретці) =
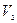 (кінцевий рівень води в бюретці) = (кінцевий рівень води в бюретці) =
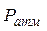 (атмосферний тиск) = (атмосферний тиск) =
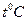 (температура) = (температура) =
| |
| Розрахуйте об’єм водню. | 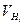 = =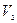 - -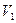 ……………мл ……………мл
| |
| Перерахуйте температуру за шкалою Кельвіна | 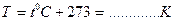
| |
| Знайдіть величину тиску водяної пари (див. таблицю 1, c.13) | 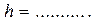 мм рт. ст. мм рт. ст.
| |
| Розрахуйте тиск водню | 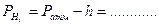 мм рт. ст. мм рт. ст.
| |
Перерахуйте об’єм водню 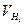 на нормальні умови (Р=760 мм рт. ст.;Т=273К), на нормальні умови (Р=760 мм рт. ст.;Т=273К),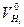
| 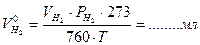
| |
Обчисліть молярну масу еквівалента досліджуваного металу
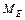 (Ме) за законом еквівалентів (Ме) за законом еквівалентів
| 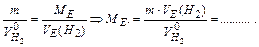
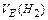 =11,2 л/моль=11200мл/моль =11,2 л/моль=11200мл/моль
| |
Розрахуйте експериментальну молярну масу металу М експ(Ме). через знайдену молярну масу еквівалента 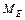
| 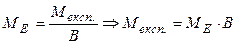
| |
Користуючись періодичною системою Д.І. Менделєєва, визначте теоретичну молярну масу металу Мтеор(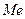 )за його валентністю. )за його валентністю.
| В=………. , М=…….. Цей метал — ……….. | |
Визначте відносну похибку досліду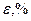
| 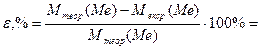
| |
| Напишіть рівняння реакції металу з кислотою |
Таблиця 1. ТИСК НАСИЧЕНОЇ ВОДЯНОЇ ПАРИ
| t°С | h, мм. рт. ст. | t°С | h, мм. рт. ст. |
| 12,8 | 18,7 | ||
| 14,5 | 21,1 | ||
| 16,5 | 23,8 |
 Висновки і місце для домашніх задач:
Висновки і місце для домашніх задач:
Оцінка___________ Дата____________ Підпис викладача____________