Результаты измерений
| Масса бюкса, г | Масса бюкса с СuSО4, г | Навеска СuSО4, г | Vводы, см3 | Т1 (до реакции), К | Т2 (после реакции), К | ДТ, К | ДНоп (опыт- ное) | ДНт (теоре- ти- ческое) |
Расчеттеплового эффекта:
1.Рассчитать, сколько теплоты (ДН, Дж) выделяется при растворении взятой навески СuSО4:
ДН = (mж ·Сж + mст ·Сст) · ДТ , (Дж),
где mж и mст – масса жидкости в стакане и масса самого стакана, кг; Сж и Сст – удельные теплоемкости стекла и жидкости (Сст = 0,75·103 Дж/кг· К, Своды = 4,18·103 Дж/кг· К), mж = Vводы·с (с=1г/см3).
2. Рассчитать тепловой эффект реакции нейтрализации (ДНоп, кДж):
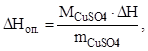
где М СuSО4 - молярная масса соли.
3. Определить относительную ошибку опыта. Гидратация безводной соли и растворение пятиводной соли (кристаллогидрата в воде) выражается уравнениями:
СuSО4 + 5 Н2О = СuSО4 · 5 Н2О, ДН = -74,4 кДж,
СuSО4 · 5 Н2О + аq = СuSО4 · аq, ДН = +11,0 кДж,
ДНт (СuSО4 · 5 Н2О) = -63,4 кДж,
 .
.
Опыт №3. Установление количественного значения теплового эффекта реакции нейтрализации
Отмерить цилиндром 50 см3 0,5М раствора соляной кислоты и перелить в стакан, который затем поместить в калориметр. Закрыть плотно крышкой с отверстием. Опустить термометр и замерить температуру раствора соляной кислоты. Отмерить цилиндром 50 см3 0,5М раствора гидроксида натрия, вылить в раствор соляной кислоты. Быстро перемешать и отметить температуру раствора с точностью до 0,1 єС.
Результаты свести в таблицу 3.2.