рефераты конспекты курсовые дипломные лекции шпоры
- Раздел Химия
- /
- Для лекарственных веществ химической структуры
Реферат Курсовая Конспект
Для лекарственных веществ химической структуры
Для лекарственных веществ химической структуры - раздел Химия, Фармацевтическая химия ...
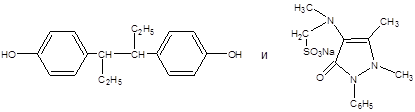
общей реакцией является образование:
1) азокрасителя
2) перйодида
3) ауринового красителя
4) бромпроизводного
5) гидроксамата железа (III)
26. Гидразидом по строению является:
1) изониазид
2) этазол
3) букарбан
4) фурадонин
5) анестезин
27. Образование плава сине-фиолетового цвета с выделением аммиака характерно для:
1) барбитала
2) бутадиона
3) стрептоцида
4) норсульфазола
5) новокаина
28. Метод йодометрии используется для количественного определения:
1) ментола
2) никотинамида
3) кислоты глютаминовой
4) фенобарбитала
5) анальгина
29. Кофеин образует осадок с раствором йода в присутствии:
1) натрия гидроксида
2) спирта
3) кислоты хлористоводородной
4) аммиака
5) натрия ацетата
30. Общим продуктом гидролитического расщепления парацетамола и сульфацил-натрия в кислой среде является:
1) оксид углерода
2) азот
3) диоксид серы
4) формальдегид
5) кислота уксусная
31. Отсутствие примеси восстанавливающих веществ в воде очищенной устанавливают по:
1) появлению синей окраски от прибавления раствора дифениламина
2) сохранению окраски раствора калия перманганата в среде кислоты серной
3) сохранению окраски раствора калия перманганата в среде кислоты хлористоводородной
4) обесцвечиванию раствора калия перманганата в среде кислоты серной
5) обесцвечиванию раствора калия перманганата в среде кислоты хлористоводородной
32. ФС регламентирует с помощью соответствующего эталонного раствора содержание в воде очищенной ионов:
1) хлорида
2) сульфата
3) кальция
4) аммония
5) тяжелых металлов
33. ФС рекомендует открывать примесь нитратов и нитритов в воде очищенной по:
1) обесцвечиванию раствора калия перманганата
2) реакции с концентрированной кислотой серной
3) обесцвечиванию раствора калия перманганата в сернокислой среде
4) реакции с раствором дифениламина
5) реакции с раствором дифениламина в среде концентрированной кислоты серной
34. Ион, который может быть одновременно обнаружен при проведении испытаний на хлорид-ионы в воде очищенной:
1) бромид
2) фосфат
3) сульфид
4) карбонат
5) гидрокарбонат
35. Общий метод количественного определения раствора пероксида водорода, натрия нитрита, железа (II) сульфата, железа восстановленного:
1) ацидиметрия
2) алкалиметрия
3) рефрактометрия
4) комплексонометрия
5) перманганатометрия
36. Примесь трех ионов (бария, кальция, бромата) в лекарственном средстве "натрия бромид" можно обнаружить одним реактивом:
1) кислотой серной
2) раствором аммиака
3) раствором аммония оксалата
4) раствором натрия гидроксида
5) кислотой хлористоводородной
37. Стабилизатор для раствора пероксида водорода согласно ГФ XI:
1) натрия бензоат
2) кислота бензойная
3) натрия гидрокарбонат
4) раствор натрия гидроксида
5) кислота хлористоводородная
38. Отличить раствор гидрокарбоната натрия от карбоната натрия можно по:
1) индикатору лакмусу
2) индикатору фенолфталеину
3) индикатору метиловому красному
4) реакции с кислотой уксусной
5) реакции с минеральной кислотой
39. При определении примеси хлорид-ионов в натрия тиосульфате необходимо предварительно провести реакцию с:
1) аммиаком
2) натрием гидроксидом
3) кислотой азотной
4) кислотой уксусной
5) кислотой хлористоводородной
40. Лекарственное вещество, растворимое и в кислотах, и в щелочах:
1) цинка оксид
2) магния оксид
3) лития карбонат
4) висмута нитрат основной
5) бария сульфат
41. Реакция, протекающая при взаимодействии ксантинола никотината с калия дихроматом в сернокислой среде:
1) дегидратации
2) комплексообразования
3) окислительно-восстановительная
4) гидролиза
5) этерификации
42. Стабилизатор инъекционного раствора кислоты аскорбиновой по НД:
1) натрия гидрокарбонат и натрия хлорид
2) натрия хлорид и натрия метабисульфит
3) натрия гидроксид и натрия метабисульфит
4) натрия гидрокарбонат и натрия метабисульфит
5) натрия карбонат
43. При взаимодействии ментола с раствором ванилина в концентрированной серной кислоте происходит:
1) полимеризация
2) окисление спиртовой группы
3) окисление всей гидрированной системы
4) конденсация в α-положении к спиртовому гидроксилу с последующим окислением
5) конденсация в α-положении к спиртовому гидроксилу
44. Общим в строении камфоры и преднизолона является наличие:
1) кетогруппы
2) гидроксильных групп
3) α-кетольной группировки
4) ядра циклопентанпергидрофенантрена
5) системы сопряженных двойных связей
45. Общая функциональная группа нитроглицерина, анестезина, валидола:
1) аминогруппа
2) нитрогруппа
3) метильная
4) гидроксильная
5) сложно-эфирная
46. Образует осадок при добавлении бромной воды:
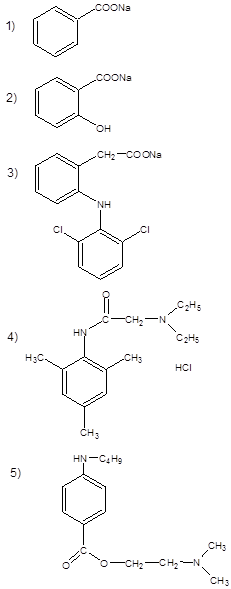
47. Лактоном по строению является:
1) кислота ацетилсалициловая
2) камфора
3) кислота аскорбиновая
4) изониазид
5) фенобарбитал
48. Метод ацетилирования используется для количественного определения:
1) кислоты бензойной
2) кислоты глютаминовой
3) никотинамида
4) ментола
5) глюкозы
49. Процентное содержание кофеина в кофеин-бензоате натрия должно быть:
1) 14-18
2) 18-22
3) 38-40
4) 58-62
5) 80-85
50. К общеалкалоидным реактивам не относится:
1) танин
2) реактив Марки
3) кислота пикриновая
4) реактив Драгендорфа
5) реактив Бушарда
51. Метод нитритометрии применяется для количественного определения:
1) барбитала
2) оксафенамида
3) левомицетина
4) теобромина
5) кислоты никотиновой
52. Специфической реакцией, применяемой для определения подлинности резорцина и фталазола, является:
1) взаимодействие с железа (III) хлоридом
2) образование флюоресцеина
3) бромирование
4) взаимодействие с меди сульфатом
5) азосочетание с солью диазония
53. Эффектом реакции взаимодействия кальция лактата с калия перманганатом в среде разведенной серной кислоты является:
1) красно- фиолетовое окрашивание
2) осадок красно- коричневого цвета
3) запах формальдегида
4) запах ацетальдегида
5) запах кислоты уксусной
54. Реакции кислотного гидролиза используют при идентификации:
1) дибазола
2) барбитала
3) метенамина (гексаметилентерамина)
4) теобромина
5) кислоты аскорбиновой
55. Общими реагентами для кодеина и морфина гидрохлорида являются все перечисленные ниже, кроме:
1) железа (III) хлорида
2) концентрированной кислоты серной
3) кислоты пикриновой
4) реактива Марки
5) концентрированной кислоты азотной
56. Красно-оранжевый осадок с реактивом Фелинга образует:
1) барбитал
2) кортизона ацетат
3) теобромин
4) стрептоцид
5) кислота никотиновая
57. В виде трео- и эритростереоизомеров может существовать:
1) леводопа
2) папаверина гидрохлорид
3) левомицетин
4) кодеин
5) морфина гидрохлорид
58. Белым кристаллическим порошком является:
1) хинина сульфат
2) хинозол
3) кислота фолиевая
4) рибофлавин
5) рутин
59. Кислота хлористоводородная как стабилизатор входит в состав инъекционного раствора:
1) эуфиллина
2) кальция хлорида
3) кофеин-бензоата натрия
4) анальгина
5) атропина сульфата
60. Реагент, при добавлении которого (в определённом количестве) к водному раствору эуфиллина образуется белый осадок:
1) натрия гидроксид
2) разведённая кислота хлористоводородная
3) спирт
4) натрия карбонат
5) раствор аммиака
61. Кислотный гидролиз применяется для количественного определения:
1) бутадиона
2) гексаметилентетрамина
3) глюкозы
4) стрептоцида
5) натрия салицилата
62. Метод количественного определения кофеина в препарате «кофеин-бензоат натрия»:
1) ацидиметрия
2) йодометрия
3) алкалиметрия
4) броматометрия
5) кислотно-основное титрование в неводной среде
63. Азокраситель можно получить для:
1) барбитала
2) нитроксолина
3) аминазина
4) кофеина
5) ментола
64. Термической стерилизации не подвергают инъекционный раствор:
1) новокаина
2) адреналина гидрохлорида
3) глюкозы
4) кислоты никотиновой
5) пиридоксина гидрохлорида
65. Количественное определение фурацилина йодометрическим методом основано на его способности к:
1) комплексообразованию
2) восстановлению
3) окислению
4) реакции электрофильного замещения
5) реакции конденсации
66. Растворитель, рекомендуемый ФС при количественном определении фенобарбитала методом кислотно-основного титрования в неводных средах:
1) ацетон
2) диметилформамид
3) ангидрид уксусный
4) ртути (II) ацетат
5) метиловый спирт
67. Циклическим уреидом по строению является:
1) рутин
2) фтивазид
3) норсульфазол
4) барбитал
5) бутадион
68. Метод количественного определения стрептоцида в мази при внутриаптечном контроле:
1) алкалиметрия
2) броматометрия
3) ацидиметрия
4) аргентометрия
5) нитритометрия
69. Стабилизатор раствора натрия тиосульфата для инъекций:
1) натрия метабисульфит
2) кислота хлористоводородная
3) натрия гидроксид
4) натрия гидрокарбонат
5) натрия хлорид
70. Окрашенное соединение с раствором йода образует:
1) бензонал
2) кислота никотиновая
3) адреналина гидротартрат
4) ментол
5) кислота аскорбиновая
71. Реагент, позволяющий дифференцировать теобромин и теофиллин:
1) железа (III) хлорид
2) меди сульфат
3) натрия гидроксид
4) кислота хлористоводородная
5) кобальта хлорид
72. Стабилизатор раствора адреналина гидрохлорида для инъекций:
1) раствор кислоты хлористоводородной, хлорбутанолгидрат
2) хлорбутанолгидрат, раствор кислоты хлористоводородной, натрия метабисульфит
3) натрия метабисульфит, хлорбутанолгидрат, раствор натрия гидрокарбоната
4) натрия тиосульфат
5) кислота аскорбиновая, натрия хлорид
73. Термической стерилизации не подвергается:
1) глюкоза
2) гексаметилентетрамин
3) кислота аскорбиновая
4) натрия тиосульфат
5) новокаин
74. Окрашенный хелатный комплекс с раствором меди сульфата образует:
1) кислота бензойная
2) эуфиллин
3) кислота аскорбиновая
4) кофеин
5) анальгин
75. Групповым реагентом для производных 5-нитрофурана является:
1) раствор йода
2) концентрированная кислота серная
3) раствор аммиака
4) концентрированная кислота азотная
5) раствор натрия гидроксида
76. Реагент, позволяющий дифференцировать производные 5-нитрофурана по НД:
1) раствор йода
2) железа (III) хлорид
3) нитрат серебра
4) концентрированная кислота серная
5) спиртовой раствор калия гидроксида в диметилформамиде
77. Общим методом количественного определения кислоты аскорбиновой и изониазида является:
1) ацидиметрия
2) алкалиметрия
3) йодометрия
4) аргентометрия
5) нитритометрия
78. Дважды сложным эфиром по строению является:
1) новокаин
2) кокаина гидрохлорид
3) анестезин
4) ретинола ацетат
5) неодикумарин
79. Тип реакции взаимодействия указанного лекарственного вещества с 1% раствором натрия нитрита в кислой среде:
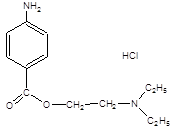
1) окисление
2) осаждение
3) диазотирование
4) солеобразование
5) электрофильное замещение
80. Тип реакции взаимодействия указанного лекарственного вещества с 1% раствором натрия нитрита в кислой среде:
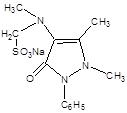
1) окисление
2) осаждение
3) диазотирование
4) солеобразование
5) электрофильное замещение
81. Тип реакции взаимодействия указанного лекарственного вещества с 1% раствором натрия нитрита в кислой среде:
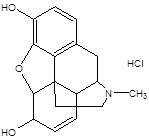
1) окисление
2) осаждение
3) нитрозирование
4) солеобразование
5) диазотирование
82. Реакции, происходящие при взаимодействии изониазида с катионами меди (II) в различных условиях:
1) комплексообразования
2) окисления
3) восстановления
4) гидролитического расщепления
5) все вышеперечисленные
83. Для лечения подагры используют:
1) кофеин
2) аллопуринол
3) ксантинола никотинат
4) рибоксин
5) дипрофиллин
84. Специфическая примесь в кислоте ацетилсалициловой:
1) фенол
2) п-аминофенол
3) салициловая кислота
4) п-аминосалициловая кислота
5) п-аминобензойная кислота
85. Лекарственное средство, по составу являющееся солью:
1) ретинола ацетат
2) анестезин
3) теобромин
4) токоферола ацетат
5) дибазол
86. Примесь метанола в спирте этиловом по ГФ определяют с:
1) концентрированной кислотой серной
2) реактивом Марки
3) концентрированной кислотой серной и ванилином
4) концентрированной кислотой серной и кислотой хромотроповой
5) реактивом Фелинга
87. Растворитель, применяемый при количественном определении фталазола методом кислотно-основного титрования в неводной среде:
1) хлороформ
2) диметилформамид
3) ацетон
4) ангидрид уксусный
5) кислота муравьиная
88. Применение метода цериметрии для количественной оценки токоферола ацетата основано на его способности к:
1) восстановлению
2) солеобразованию
3) окислению
4) комплексообразованию
5) электрофильному замещению
89. Молярная масса эквивалента резорцина при броматометрическом титровании равна:
1) 1/2 М.м резорцина
2) 1/3 М.м резорцина
3) 1/4 М.м резорцина
4) 1/6 М.м резорцина
5) 1/8 М.м резорцина
90. В основе количественного определения анальгина йодометрическим методом лежит реакция:
1) комплексообразования
2) электрофильного замещения
3) окисления S+4 до S+6 после гидролиза
4) окисления формальдегида
5) окисления пиразолонового цикла
91. Реакция, которая правильно отражает процесс броматометрического определения салициловой кислоты:
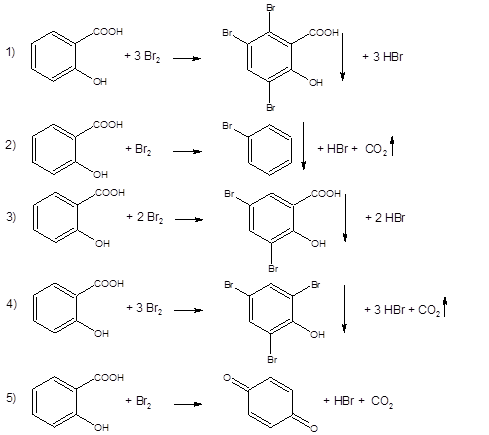
92. В процессе хранения глазных капель сульфацила-натрия под действием света и кислорода воздуха может происходить:
1) появление осадка
2) пожелтение раствора
3) сдвиг рН в кислую сторону
4) сдвиг рН в щелочную сторону
5) изменение удельного вращения
93. При количественном определении органически связанного йода методом сжигания в колбе с кислородом в качестве поглощающего раствора используют:
1) кислоту хлористоводородную
2) натрия тиосульфат
3) натрия гидрокарбонат
4) кислоту серную
5) натрия гидроксид
94. При окислении ментола образуется:
1) альдегид
2) фенол
3) карбоновая кислота
4) хинон
5) кетон
95. Химическое название неодикумарина:
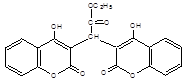
1) 3-α-фенил-β-пропионилэтил-4-оксикумарин
2) этиловый эфир ди-(4-оксикумаринил-3)-уксусной кислоты
3) ди-(4-оксикумаринил-3)-уксусная кислота
4) 3-(α-пара-нитрофенил-β-пропионил-этил)-4-оксикумарин
5) 4-оксикумарин
96. Лекарственное вещество, которому соответствует химическое название 1,2-дифенил-4-бутилпиразолидиндион-3,5:
1) анальгин
2) бутадион
3) диэтиламид никотиновой кислоты
4) фенобарбитал
5) кофеин
97. Лекарственное вещество, имеющее слабый запах ванилина:
1) пропифеназон
2) кислота никотиновая
3) папаверина гидрохлорид
4) фтивазид
5) изониазид
98. Производное пурина, обладающее слабым аммиачным запахом:
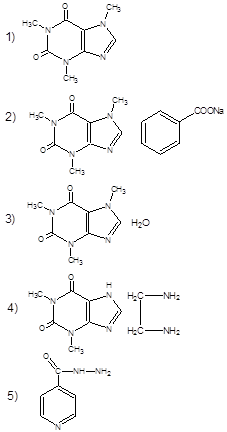
99. Лекарственное вещество, водный раствор которого имеет зеленовато-жёлтую окраску с зелёной флюоресценцией:
1) этилморфина гидрохлорид
2) рибофлавин
3) нозепам
4) аминазин
5) хинозол
100. Реактив, позволяющий отличить фтивазид от изониазида:
1) 2,4-динитрохлорбензол
2) кислота фосфорномолибденовая
3) бромродановый реактив
4) кислота хлористоводородная (при нагревании)
5) пикриновая кислота
101. Сложным эфиром по химическому строению является:
1) атропина сульфат
2) морфина гидрохлорид
3) фтивазид
4) фурацилин
5) стрептоцид
102. Соединение, при взаимодействии которого с раствором натрия гидроксида появляется темно-красное окрашивание:
1) бутадион
2) кислота глютаминовая
3) фурадонин
4) резорцин
5) фенобарбитал
103. Общая реакция для кислоты ацетилсалициловой, новокаина и валидола:
1) с раствором хлорамина
2) с бромной водой
3) гидроксамовая реакция
4) образование азокрасителя
5) с раствором хлорида железа (III)
104. Осаждение основания из водного раствора атропина сульфата проводят:
1) натрия карбонатом
2) раствором аммиака
3) натрия гидроксидом
4) кислотой хлористоводородной
5) натрия ацетатом
105. Фрагмент реакции этерификации для получения препаратов местноанестезирующего действия:

106. Образование при кислотном гидролизе химического соединения со специфическим запахом характерно для:
1) изониазида
2) кофеина
3) фенобарбитала
4) фтивазида
5) никотинамида
107. Общим реагентом при определении подлинности норсульфазола и бутадиона является:
1) меди сульфат
2) калия йодид
3) раствор йода
4) концентрированная кислота серная
5) раствор аммиака
108. В состав инъекционного раствора кислоты никотиновой входит:
1) натрия гидрокарбонат
2) натрия хлорид
3) кислота хлористоводородная
4) натрия гидроксид
5) натрия метабисульфит
109. Реакция, лежащая в основе получения сульфаниламидных препаратов:
1) сульфохлорирование
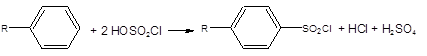
2) нитрование
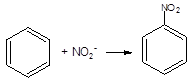
3) галогенирование
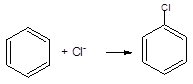
4) карбоксилирование фенолята натрия
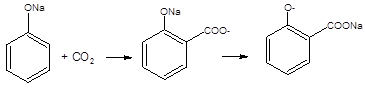
5) сульфирование бензола
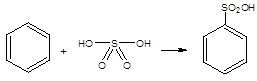
110. Реакция, используемая для идентификации сложных эфиров:

111. Азокраситель не образуют лекарственные вещества – производные:
1) сульфаниламидов
2) п-аминобензойной кислоты
3) бензойной кислоты
4) о-аминобензойной кислоты
5) п-аминофенола
112. Фармакопейным методом количественного определения кислоты аскорбиновой является:
1) йодатометрия
2) йодометрия
3) цериметрия
4) алкалиметрия
5) йодхлорметрия
113. Реакция среды, необходимая для повышения воспроизводимости результатов при количественном определении препаратов – производных первичных ароматических аминов:
1) щелочная
2) нейтральная
3) кислая
4) сильно щелочная
5) сильно кислая
114. Метод количественного анализа, в котором применяются адсорбционные индикаторы:
1) кислотно-основное титрование в водных средах
2) титрование в неводных средах
3) броматометрия (прямая и обратная)
4) аргентометрия
5) комплексонометрия
115. При оценке качества раствора натрия тиосульфата для инъекций ФС регламентирует определение:
1) хлоридов
2) сульфатов
3) щёлочности
4) сульфитов
5) кислотности
116. Лекарственное средство, для которого необходимо определение присутствия спирта этилового при количественном анализе методом нейтрализации лекарственного средства:
1) гексаметилентетрамин
2) кислота глютаминовая
3) натрия салицилат
4) атропина сульфат
5) кислота ацетилсалициловая
117. Разделение вещества в тонком слое сорбента можно отнести к следующему типу хроматографии:
1) ионообменная
2) осадочная
3) адсорбционная
4) ионообменная
5) гель-фильтрация
118. Отличие УФ-спектрофотометрии от фотоэлектроколориметрии заключается в:
1) зависимости светопоглощения от толщины раствора
2) способах расчета концентрации вещества
3) используемой области оптического спектра
4) зависимости светопоглощения от концентрации вещества в растворе
5) подчинении основному закону светопоглощения
119. Химические процессы, происходящие при неправильном хранении лекарственных препаратов, содержащих в молекуле фенольный гидроксил:
1) окисление
2) восстановление
3) гидролиз
4) конденсация
5) полимеризация
120. Основной фактор воздействия на лекарственное вещество при изучении сроков годности методом ускоренного старения:
1) свет
2) температура
3) влажность воздуха
4) упаковка
5) углекислота воздуха
121. Кальция хлорид по физическим свойствам – это:
1) белый мелкий лёгкий порошок без запаха
2) бесцветные призматические выветривающиеся кристаллы
3) бесцветные кристаллы без запаха, горько-солёного вкуса, очень гигроскопичные, расплываются на воздухе
4) белый или белый с желтоватым оттенком аморфный порошок
5) блестящие игольчатые кристаллы
122. Не растворим в воде:
1) натрия хлорида
2) натрия тетраборат
3) цинка оксид
4) натрия йодид
5) натрия тиосульфат
123. Кислотные свойства аскорбиновой кислоты обусловлены:
1) лактонным кольцом
2) карбоксильной группой
3) енольным гидроксилом
4) спиртовым гидроксилом
5) фенольным гидроксилом
124. Метод анализа, который используется для количественного определения натрия тетрабората по НД:
1) косвенная нейтрализация
2) ацидиметрия в водной среде
3) алкалиметрия
4) ацидиметрия в водно-глицериновой среде
5) аргентометрия
125. Для подтверждения подлинности формальдегида, глюкозы и аскорбиновой кислоты по их восстановительным свойствам используют:
1) реактив Фелинга
2) кислоту пикриновую
3) реактив Драгендорфа
4) кислоту салициловую
5) железа (III) хлорид
126. Кислоту аскорбиновую хранят в хорошо укупоренной таре, предохраняя от действия света, так как при хранении она подвергается процессу:
1) восстановления
2) гидролиза
3) полимеризации
4) окисления
5) конденсации
127. По химической структуре сульфацил-натрий является:
1) 2-(п-аминобензолсульфамидо)-3-метоксипиразином
2) п-аминобензолсульфонил-ацетамидом-натрия
3) 2-п-аминобензолсульфамидо-тиазолом
4) N-(п-метилбензолсульфонил)-N-бутилмочевиной
5) N-(п-хлорбензолсульфонил)-N-пропилмочевиной
128. По химической структуре метилдопа является:
1) изопропилнорадреналином
2) 3-гидрокси-α-метил-l-тирозином
3) l-1-амино-β-(3-оксифенил)-пропионовой кислотой
4) 4-хлор-N-(2-фурилметил)-5-сульфамоилантраниловой кислотой
5) l-1-(3,4-дигидроксифенил)-2-метиламиноэтанолом
129. Препарат, в котором по НД определяют содержание активного хлора:
1) хинозол
2) глибенкламид
3) дихлотиазид
4) хлорамин Б
5) хлорхинальдол
130. Производным андростана является:
1) кортизона ацетат
2) прегнин
3) тестостерона пропионат
4) этинилэстрадиол
5) дексаметазон
131. Стероидный препарат, растворимый в воде:
1) строфантин К
2) метилтестостерон
3) дигитоксин
4) преднизолон
5) прогестерон
132. По реакции образования гидроксамата железа можно идентифицировать:
1) преднизолон
2) дексаметазон
3) тестостерона пропионат
4) метандростенолон
5) прегнин
133. Метод, применяемый для определения посторонних примесей в препарате «кортизона ацетат»:
1) УФ-спектрофотометрия
2) гравиметрия
3) фотоколориметрия
4) тонкослойная хроматография
5) поляриметрия
134. Лекарственное средство, не проявляющее амфотерных свойств:
1) теобромин
2) стрептоцид
3) изониазид
4) фенобарбитал
5) теофиллин
135. Структурная формула гексамидина:
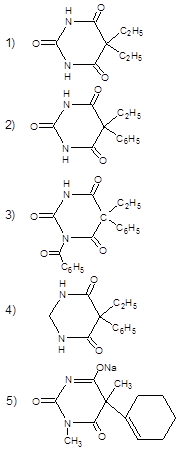
136. Структурная формула кокарбоксилазы:
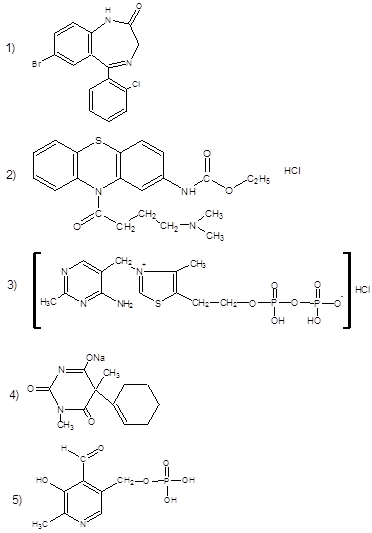
137. Гетероциклы хинолин и хинуклидин содержатся в химической структуре:
1) кодеина
2) хинина дигидрохлорида
3) резерпина
4) этилморфина гидрохлорида
5) хинозола
138. Химическое название рибофлавина:
1) 6,7-диметил-9-(D-1-рибитил)-изоаллоксазин
2) 6-хлор-7-сульфамин-3,4-дигидро-1,2,4-бензотиадиазин-1,1-диоксид
3) 6-метил-9-(D-1-рибитил)-изоаллоксазин
4) диметилаллоксазин
5) 1,2-дифенил-4-бутилпиразолидиндион-3,5
139. Лекарственное вещество, представляющее собой слабо-желтую маслянистую жидкость с характерным запахом:
1) изониазид
2) кислота никотиновая
3) пиридоксина гидрохлорид
4) диэтиламид никотиновой кислоты
5) никотинамид
140. Антибиотик-аминогликозид, содержащий в молекуле альдегидную группу:
1) амикацина сульфат
2) гентамицина сульфат
3) канамица сульфат
4) стрептомицина сульфат
5) неомицина сульфат
141. Фактор эквивалентности натрия тетрабората при титровании кислотой хлористоводородной равен:
1) 1/2
2) 1/4
3) 1
4) 2
5) 4
142. Фактор эквивалентности метенамина (гексаметилентетрамина) в методе кислотного гидролиза равен:
1) 1/2
2) 1/3
3) 1/4
4) 1
5) 2
143. Индикатор в аргентометрии по методу Мора:
1) эриохром черный Т
2) фенолфталеин
3) флюоресцеин
4) калия хромат
5) калия дихромат
144. Процесс, лежащий в основе разделения веществ в адсорбционном варианте тонкослойной хроматографии:
1) ионного обмена
2) кристаллизации
3) фильтрации
4) сорбции-десорбции
5) осаждения
145. Функциональная группа п-аминосалициловой кислоты, взаимодействующая с титрантом при алкалиметрическом титровании:
1) фенольный гидроксил
2) аминогруппа
3) карбоксильная группа
4) бензольное кольцо
5) фенольный гидроксил и карбоксильная группа
146. Испытание на пирогенность не проводится для:
1) канамицина сульфата
2) стрептомицина сульфата
3) феноксиметилпенициллина
4) бензилпенициллина натриевой соли
5) карбенициллина динатриевой соли
147. Реакцию с орцином дает:
1) цефалексин
2) канамицина моносульфат
3) феноксиметилпенициллин
4) цефалотина натриевая соль
5) бензилпенициллина калиевая соль
148. Метод количественного анализа лекарственных препаратов, имеющих в молекуле первичную ароматическую аминогруппу:
1) ацидиметрия
2) нитритометрия
3) аргентометрия
4) комплексонометрия
5) алкалиметрия
149. При количественном анализе лекарственного вещества в таблетках на анализ берут:
1) одну таблетку
2) массу из 10 растертых таблеток
3) массу растертых таблеток (не менее 20)
4) массу одной растертой таблетки
5) массу из 5 растертых таблеток
150. Препарат из группы терпенов, растворимый в воде:
1) ментол
2) камфара
3) терпингидрат
4) кислота сульфокамфорная
5) валидол
151. Окрашенный хелатный комплекс с раствором меди сульфата образует:
1) кислота аскорбиновая
2) изониазид
3) ментол
4) кофеин
5) анальгин
152. Кислотный гидролиз используется для определения подлинности:
1) кофеина
2) барбитала
3) кислоты ацетилсалициловой
4) теобромина
5) кислоты аскорбиновой
153. Реакция кислотного гидролиза используется для идентификации:
1) хинозола
2) барбитала
3) феназепама
4) ментола
5) кислоты аскорбиновой
154. Уравнение окислительного распада пероксида водорода:
1) Н2О2 + 2Н+ + 2е = 2Н2О
2) Н2О2 – 2е = О2 + 2Н+↑
3) Н2О2 + 2Н+ = 2Н2О
4) Н2О2 + 2Н+- 2е = 2Н2О
5) Н2О2 + 2е = О2 + 2Н+↑
155. Процентное содержание хлористого водорода в препарате «Аcidum hydrocloricum dilutum»:
1) 8,2 – 8,4
2) 24,8 – 25,2
3) 35,0 – 36,0
4) 38,0 – 42,0
5) 99,5 – 100,0
156. Аргентометрия (метод Фаянса) проводится в среде:
1) аммиачного буферного раствора
2) хлористоводородной кислоты
3) щелочной
4) нейтральной
5) уксуснокислой
157. Реакция, обусловленная наличием альдегидной группы в хлоралгидрате:
1) щелочного гидролиза
2) «серебряного зеркала»
3) конденсации с салициловой кислотой
4) «гидроксамовой пробы»
5) окисления с перманганатом калия в кислой среде
158. Общим методом количественного определения кальция глюконата и кальция лактата является:
1) аргентометрия
2) комплексонометрия
3) перманганатометрия
4) поляриметрия
5) ацидиметрия
159. Общегрупповой реакцией на лекарственные препараты группы аминокислот является:
1) реакция образования индофенолового красителя
2) реакция образования азокрасителя
3) реакция образования ауринового красителя
4) нингидриновая реакция
5) гидроксамовая реакция
160. Общей функциональной группой камфоры, бромкамфоры и сульфокамфокаина является:
1) сульфогруппа
2) кето-группа
3) органически связанный галоген
4) система сопряженных двойных связей
5) вторичный спиртовой гидроксил
161. Наличие свободного фенольного гидроксила в молекуле парацетамола доказывается реакцией с:
1) натрия нитритом
2) хлористоводородной кислотой разведенной
3) хлоридом железа (III)
4) нитратом серебра
5) перманганатом калия
162. Функциональная группа, обуславливающая солеобразование новокаина с хлористоводородной кислотой:
1) первичная ароматическая аминогруппа
2) ароматическая нитрогруппа
3) амидная группа
4) сложно-эфирная группа
5) алифатическая аминогруппа
163. В основе количественного определения эфедрина гидрохлорида методом кислотно-основного титрования в среде неводного растворителя лежит его способность:
1) окисляться
2) проявлять слабые основные свойства
3) проявлять слабые кислотные свойства
4) восстанавливаться
5) осаждаться
164. Для обнаружения йода в трийодтиронине проводят:
1) реакцию с нитратом серебра
2) нагревание препарата
3) реакцию с хлорамином в кислой среде
4) реакцию с нитритом натрия в кислой среде
5) реакцию с перманганатом калия в кислой среде
165. К реактивам, доказывающим кислотные свойства сульфаниламидных препаратов, относятся:
1) FeCl3, CuSO4, NaNO2, реактив Фелинга
2) AgNO3, FeCl3, NaOH
3) NaNO2, CoCl2, AgNO3, реактив Несслера
4) NaNO2, CoCl2
5) AgNO3, FeCl3, реактив Марки
166. Препарат, не растворимый в воде:
1) хлорамин Б
2) гексаметилентетрамин
3) цинка оксид
4) цинка сульфат
5) кислота аскорбиновая
167. Метод йодометрии в соответствующих условиях применим для количественного определения:
1) серебра нитрата
2) меди сульфата
3) железа восстановленного
4) цинка оксида
5) серебра нитрата
168. Примесь солей аммония и параформа в гексаметилентетрамине открывают по методике НД реакцией с:
1) раствором йода
2) раствором натрия гидроксида
3) реактивом Фелинга
4) реактивом Несслера
5) реактивом Марки
169. Индикатор в алкалиметрии кислоты глютаминовой по методике ФС:
1) фенолфталеин
2) тимоловый синий
3) бромтимоловый синий
4) бромкрезоловый пурпурный
5) нейтральный красный
170. Левомицетин применяется в виде сложного эфира кислоты:
1) уксусной
2) хлористоводородной
3) янтарной
4) серной
5) лимонной
171. Фармакопейный метод количественного определения кислоты глютаминовой:
1) йодометрия
2) алкалиметрия
3) аргентометрия
4) перманганатометрия
5) комплексонометрия
172. Общим методом количественного определения висмута нитрата основного, цинка сульфата, кальция хлорида является:
1) ацидиметрия
2) алкалиметрия
3) рефрактометрия
4) комплексонометрия
5) перманганатометрия
173. К реактивам, выявляющим способность лекарственных веществ к комплексообразованию, относят:
1) AgNO3, FeCl3, реактив Драгендорфа
2) FeCl3, реактив Фелинга, Cо(NO3)2
3) реактив Фелинга, раствор йода, AgNO3
4) реактив Несслера, FeCl3
5) реактив Марки, раствор йода, AgNO3
174. Специфическая примесь в новокаине:
1) фенол
2) п-аминофенол
3) салициловая кислота
4) п-аминосалициловая кислота
5) п-аминобензойная кислота
175. Изменяет внешний вид при прокаливании:
1) натрия хлорид
2) цинка оксид
3) магния сульфат
4) натрия гидрокарбонат
5) натрия хлорид
176. Растворимость парацетамола в растворе натрия гидроксида обусловлена:
1) имидной группой
2) енольным гидроксилом
3) фенольным гидроксилом
4) спиртовым гидроксилом
5) карбоксильной группой
177. Примесь посторонних аминокислот в препарате «Ацетилцистеин» открывают с применением метода:
1) спектрофотометрии в УФ-области
2) тонкослойной хроматографии
3) характерных химических реакций
4) ВЭЖХ
5) ГЖХ
178. Потемнение аммиачного раствора нитрата серебра при пропускании через него кислорода свидетельствует о наличии в кислороде примеси:
1) диоксида углерода
2) озона
3) оксида углерода
4) оксида азота
5) диоксида азота
179. Индикатором в фармакопейном методе количественного определения серебра нитрата является:
1) калия хромат
2) эозинат натрия
3) бромфеноловый синий
4) флуоресцеин
5) железо-аммониевые квасцы
180. Функциональная группа, имеющаяся в структуре терпингидрата:
1) спиртовой гидроксил
2) кето-группа
3) сложно-эфирная группа
4) альдегидная группа
5) фенольный гидроксил
181. Взаимодействие норадреналина с хлоридом железа (III) обусловлено:
1) восстановительными свойствами фенольных гидроксилов
2) наличием сложно-эфирной группы
3) основными свойства аминогруппы
4) кислотными свойствами фенольных гидроксилов
5) кислотными свойствами спиртового гидроксила
182. Реактив, используемый для определения примеси солей тяжелых металлов в серебра нитрате:
1) разведенная серная кислота
2) раствора едкого натра
3) раствор бария хлорида
4) раствор аммиака
5) реактив Несслера
183. Точка эквивалентности в количественном определении натрия п-аминосалицилата методом нитритометрии определяется:
1) внутренним индикатором
2) потенциометрически
3) внешним индикатором
4) фотоэлектроколориметрически
5) спектрофотометрически
184. Препарат, растворимый в воде:
1) кислота ацетилсалициловая
2) кальция хлорид
3) цинка оксид
4) кислота бензойная
5) магния оксид
185. Препарат, для которого реакция «серебряного зеркала» положительна:
1) натрия хлорид
2) кислота борная
3) метионин
4) формальдегид
5) цистеин
186. Препарат, водный раствор которого имеет щелочную реакцию среды по фенолфталеину:
1) натрия тетраборат
2) кислота аскорбиновая
3) калия йодид
4) железа сульфат
5) натрия бромид
187. Расчет титра по определяемому веществу проводится по формуле:
1) Т = Э ∙ К
2) Т = Э ∙ Ститранта
0,1
3) Т = М.м ∙ Ститранта
4) Т = М.м ∙ С0
5) Т = Э ∙ Ститранта
188. Лекарственное средство, являющееся кристаллогидратом:
1) кислота борная
2) цинка сульфат
3) калия бромид
4) кислота глютаминовая
5) натрия салицилат
189. Препарат, спиртовой раствор которого при поджигании горит пламенем с зеленой каймой:
1) хлоралгидрат
2) кислота борная
3) натрия хлорид
4) калия йодид
5) кислота ацетилсалициловая
190. Препарат, дающий положительную реакцию «нингидриновой пробы»:
1) кислота аскорбиновая
2) серебра нитрат
3) гексаметилентетрамин
4) метионин
5) кислота ацетилсалициловая
191. При неправильном хранении субстанции натрия цитрата происходит:
1) окисление
2) восстановление
3) выветривание
4) поглощение диоксида углерода
5) поглощение влаги
192. Реакция, лежащая в основе количественного определения хлоралгидрата методом обратной алкалиметрии:
1) нейтрализации
2) разложения
3) окисления
4) солеобразования
5) восстановления
193. Лекарственное средство, соответствующее описанию «белый кристаллический порошок без запаха, кислого вкуса»:
1) натрия бромид
2) кальция хлорид
3) кислота аскорбиновая
4) кальция лактат
5) левомицетина стеарат
194. Препарат, при добавлении к раствору которого нитрата серебра образуется белый творожистый осадок, легко исчезающий от добавления раствора аммиака:
1) дикаин
2) калия бромид
3) бромкамфора
4) анестезин
5) калия йодид
195. Препарат, имеющий характерный запах:
1) натрия п-аминосалицилат
2) кислота ацетилсалициловая
3) новокаин
4) тимол
5) глибекламид
196. Реакция на первичную ароматическую аминогруппу (по методике ОФС) положительна для препарата:
1) парацетамол
2) норсульфазол
3) левомицетин
4) дийодтирозин
5) ацетилцистеин
197. Препарат, для которого положительна реакция образования азокрасителя после кислотного гидролиза:
1) фталазол
2) дийодтирозин
3) бутамид
4) кислота аскорбиновая
5) кислота глютаминовая
198. Препарат, при количественном определении которого растворителем является этанол:
1) резорцин
2) кислота салициловая
3) парацетамол
4) натрия бензоат
5) фенол
199. Препарат, нитритометрическое титрование которого проводят при температуре от 0-5оС:
1) парацетамол
2) натрия п-аминосалицилат
3) новокаин
4) анестезин
5) сульфаметаксозон
200. Препарат, имеющий характерный запах:
1) кислота бензойная
2) фенол
3) анестезин
4) норсульфазол
5) натрия салицилат
201. Препарат, при пиролизе которого образуется плав бурого цвета, ощущается запах сероводорода:
1) норсульфазол
2) букарбан
3) натрия салицилат
4) фуросемид
5) сульфацил-натрий
202. Внутренним индикатором в нитритометрии является:
1) фенолфталеин
2) метиловый оранжевый
3) нейтральный красный
4) тимолфталеин
5) бромфеноловый синий
203. Препарат, имеющий характерный запах:
1) левомицетин
2) кислота салициловая
3) парацетамол
4) ментол
5) стрептоцид
204. Соединение, которое при взаимодействии с раствором натрия гидроксида образует хлороформ, а с аммиачным раствором серебра – осадок черного цвета:
1) метенамин (гексаметилентетрамин)
2) формальдегид
3) калия ацетат
4) натрия цитрат
5) хлоралгидрат
205. Нитритометрия применяется для количественного определения:
1) натрия бензоат
2) эфедрина гидрохлорид
3) дийодтирозин
4) адреналина гидротартрат
5) дикаин
206. Минимальная процентная концентрация, рекомендуемая для анализа раствора методом рефрактометрии:
1) не более 1-3
2) не менее 1-3
3) не менее 3-5
4) не более 3-5
5) более 10
207. Оптическая плотность однопроцентного раствора при толщине слоя 1 см называется:
1) удельным вращением
2) молярным показателем поглощения
3) удельным показателем поглощения
4) калибровочным графиком
5) спектром поглощения
208. Индикатор в методе йодометрии:
1) фенолфталеин
2) крахмал
3) калия хромат
4) эозинат натрия
5) метиловый оранжевый
209. Цвет, в который бром окрашивает хлороформный слой:
1) синий
2) жёлто-бурый
3) фиолетовый
4) розовый
5) красный
210. Реакцию с цинкуранилацетатом в уксуснокислой среде выполняют при определении подлинности:
1) калия хлорида
2) магния сульфата
3) кальция хлорида
4) натрия тетрабората
5) бария сульфата
211. Окислитель, применяемый при выполнении окислительно-восстановительной реакции на йодид-ион по методике ГФ ХI:
1) бария хлорид
2) хлорид железа (III)
3) калия перманганат в кислой среде
4) хлорамин в кислой среде
5) перекись водорода в кислой среде
212. Реактив на карбонат-ион:
1) оксалат аммония
2) нитрат серебра
3) хлорид железа (III)
4) хлористоводородная кислота
5) уксусная кислота
213. Лекарственное вещество, при идентификации которого наблюдается розовое пятно на куркумовой бумаге, переходящее в грязно-зеленое от прибавления раствора аммиака:
1) кислота глютаминовая
2) кислота хлористоводородная
3) кислота бензойная
4) кислота борная
5) кислота аскорбиновая
214. Фактор эквивалентности тимола при броматометрическом титровании равен:
1) 1/2
2) 1/4
3) 1
4) 2
5) 4
215. Фактор эквивалентности фенола при броматометрическом титровании равен:
1) 1/2
2) 1/4
3) 1/5
4) 1/6
5) 1
216. Реакцию на ион магния с натрия гидрофосфатом проводят в присутствии:
1) аммония гидроксида и аммония хлорида
2) разведенной уксусной кислоты
3) натрия ацетата
4) аммония гидроксида
5) аммония хлорида
217. Лекарственное средство, которое может быть использовано в качестве реактива при идентификации фенолов кислой среде:
1) раствор пероксида водорода
2) раствор формальдегида
3) кальция глюконат
4) резорцин
5) кислота салициловая
218. Реакция, лежащая в основе обратного ацидиметрического титрования гексаметилентетрамина:
1) разложения
2) нейтрализации
3) окисления
4) восстановление
5) конденсация
219. Общей фармакопейной реакцией на первичную ароматическую аминогруппу является:
1) «гидроксамовая проба»
2) реакция образование азокрасителя
3) «нингидриновая проба»
4) «мурексидная проба»
5) «талейохинная проба»
220. Активность изомеров адреналина:
1) равная физиологическая активность
2) d-изомер более активен
3) l-изомер более активен
4) трео-изомер более активен
5) эритро-изомер более активен
221. Растворителем при титровании адреналина гидротартрата в неводной среде является:
1) диметилформамид
2) диоксан
3) муравьиная кислота
4) пиридин
5) уксусная кислота безводная
222. Наиболее рациональный метод количественного определения левомицетина сукцината:
1) поляриметрия
2) спектрофотометрия
3) рефрактометрия
4) фотоколориметрия
5) газовая хроматография
223. Порошок, имеющий оранжевое окрашивание:
1) фталазол
2) фурацилин
3) левомицетин
4) салазопиридазин
5) сульфадиметоксин
224. Возможный метод количественного определения бутамида:
1) комплексономерия
2) нитритометрия
3) броматометрия
4) ацидиметрия
5) алкалиметрия
225. Препарат, в процессе хранения которого возможна потеря кристаллизационной воды:
1) висмута нитрат основной
2) борная кислота
3) магния сульфат
4) магния оксид
5) цинка оксид
226. Вид индикаторов, используемых при трилонометрическом титровании:
1) адсорбционные
2) кислотно-основные для водных сред
3) металлохромные
4) окислительно-восстановительные
5) кислотно-основные для неводных сред
227. В процессе хранения расплывается на воздухе и гидролизуется:
1) калия ацетат
2) кальция лактат
3) кислота аскорбиновая
4) кислота салициловая
5) эфедрина гидрохлорид
228. Не взаимодействует с хлоридом железа (III):
1) парацетамол
2) эфедрина гидрохлорид
3) изадрин
4) адреналина гидротартрат
5) резорцин
229. Не вступает в реакцию азосочетания без предварительного гидролиза:
1) новокаин
2) сульфацил-натрий
3) хинозол
4) феназепам
5) тиамин
230. При проведении нитритометрии необходимо соблюдать условие:
1) нагревание перед титрованием
2) среда разведенной серной кислоты
3) быстрое титрование
4) среда неводного растворителя
5) медленное титрование
231. Алкалиметрическое титрование борной кислоты ведут в среде:
1) диметилформамида
2) этанола
3) эфира
4) глицерина
5) безводной уксусной кислоты
232. Стабилизатором 37% раствора формальдегида является:
1) кислота уксусная
2) кислота муравьиная
3) этанол
4) метанол
5) хлоралгидрат
233. Общая специфическая примесь, определяемая в спирте этиловом и эфире медицинском:
1) восстанавливающие вещества
2) альдегиды
3) фурфурол
4) спирт метиловый
5) пероксиды
234. Эффект реакции глицерина с калия гидросульфатом:
1) образуется осадок белого цвета
2) выделяется бурый газ
3) образуется осадок желтого цвета
4) появляется неприятный раздражающий запах
5) появляется сине-фиолетовое окрашивание
235. Специфическая примесь в кислоте ацетилсалициловой:
1) салициловая кислота
2) п-аминофенол
3) фенол
4) бензойная кислота
5) резорцин
236. Более слабые кислотные свойства гидроксильной группы при С2 кислоты аскорбиновой обусловлены:
1) наличием лактонного кольца
2) образованием водородной связи с карбонилом при С1
3) наличием спиртовых гидроксилов
4) наличием ендиольной группировки
5) наличием остатка гулоновой кислоты
237. Для идентификации третичного атома азота в молекуле используют реактив:
1) нингидрин
2) реактив Фелинга
3) реактив Несслера
4) реактив Толленса
5) реактив Драгендорфа
238. В методике количественного определения натрия цитрата алкалиметрическому титрованию предшествует:
1) минерализация
2) препарат пропускают через ионообменную колонку
3) высушивание до постоянного веса
4) гидролиз
5) осаждение
239. Положительный эффект реакции образования берлинской лазури свидетельствует о наличии в препарате «калия йодид» примеси:
1) йодноватистой кислоты
2) нитратов
3) тиосульфатов
4) цианидов
5) йодоводородной кислоты
240. Не имеет характерного запаха:
1) метионин
2) камфора
3) терпингидрат
4) валидол
5) тиамина бромид
241. Левомицетин дает реакцию образования азокрасителя после:
1) гидролиза
2) восстановления
3) окисления
4) нагревания
5) разложения
242. Продуктами кислотного гидролиза парацетамола являются:
1) анилин и уксусная кислота
2) фенол и метиламин
3) п-аминофенол и этиламин
4) фенол и уксусная кислота
5) п-аминофенол и уксусная кислота
243. Наиболее сильные основные свойства проявляет:
1) формальдегид
2) метенамин (гексаметилентетрамин)
3) хлоралгидрат
4) кальция лактат
5) кальция глюконат
244. Препарат, при добавлении к раствору которого раствора едкого натра образуется белая муть с запахом хлороформа:
1) пантоцид
2) кальция глюконат
3) хлоралгидрат
4) хлорамин Б
5) кальция лактат
245. Расчет концентрации при прямом титровании проводится по формуле:
1) С% = V ∙ К ∙ Т ∙ 100%
а
2) С% = V ∙ К ∙ Т ∙ 100%
М.м.
3) С% = V ∙ К ∙ Т
а ∙ 100%
4) С% = ( V1 ∙К1 – V2 ∙К2 ) ∙ Т ∙ 100%
а
5) С% = V ∙ К ∙ 100%
а ∙ Т
246. Препарат, имеющий характерный запах сероводорода:
1) пантоцид
2) фтивазид
3) железа сульфат
4) анальгин
5) метионин
247. При действии окислителей кислота аскорбиновая окисляется до:
1) гулоновой кислоты
2) глутаровой кислоты
3) дегидроаскорбиновой кислоты
4) l-сорбозы
5) воды и углекислоты
248. Препарат, растворяющийся в воде при нагревании:
1) магния оксид
2) кислота аскорбиновая
3) кальция глюконат
4) бария сульфат
5) кислота ацетилсалициловая
249. Препарат, при нагревании раствора которого с серной кислотой разведенной ощущается запах формальдегида:
1) фталазол
2) гексаметилентетрамин
3) натрия гидрокарбонат
4) кислота ацетилсалициловая
5) хлорамин Б
250. Для создания оптимального значения pH, при котором проводится комплексонометрическое титрование кальция хлорида, используют:
1) азотную кислоту
2) ацетатный буфер
3) уксусную кислоту ледяную
4) аммиачный буфер
5) гидрокарбонатный буфер
251. Индикатор в ацидиметрическом титровании натрия тетрабората:
1) метиленовый синий
2) тропеолин 00
3) бромфеноловый синий
4) эриохром черный специальный
5) метиловый оранжевый
252. Препарат, дающий положительную реакцию с FeCl3 на фенольный гидроксил:
1) эфедрина гидрохлорид
2) левомицетин
3) натрия п-аминосалицилат
4) бутамид
5) фталазол
253. При титровании натрия салицилата по методике ФС эфир диэтиловый добавляют для:
1) извлечения выделяющегося основания
2) растворения препарата
3) подавления гидролиза
4) извлечения выделяющейся кислоты
5) создания оптимальной рН среды
254. Рефрактометрия – метод анализа, основанный на явлении:
1) отражения световых лучей на границе раздела двух различных оптических сред
2) адсорбции световых лучей на границе раздела двух различных оптических сред
3) поглощения световых лучей на границе раздела двух различных оптических сред
4) вращения плоскости поляризации прямолинейно поляризованного света
5) преломления световых лучей на границе раздела двух различных оптических сред
255. Формула расчёта концентрации вещества в растворе (метод рефрактометрии), при известном значении фактора показателя преломления раствора:
1) С% = nх - nо
F ∙ 100
2) С% = (nх - nо) ∙ 100
F
3) С% = nх - nо
F
4) С% = nх - nо
F ∙ l
5) С% = nх - nо
F∙1000
256. Поляриметрия – метод анализа основанный на свойстве оптически активных веществ:
1) преломлять плоскость поляризации прямолинейно поляризованного света
2) поглощать прямолинейно поляризованный свет
3) вращать плоскость поляризации прямолинейно поляризованного света
4) отражать прямолинейно поляризованный свет
5) рассеиват
– Конец работы –
Эта тема принадлежит разделу:
Фармацевтическая химия
по дисциплине Фармацевтическая химия... Вопрос Ответ Вопрос Ответ Вопрос Ответ...
Если Вам нужно дополнительный материал на эту тему, или Вы не нашли то, что искали, рекомендуем воспользоваться поиском по нашей базе работ: Для лекарственных веществ химической структуры
Что будем делать с полученным материалом:
Если этот материал оказался полезным ля Вас, Вы можете сохранить его на свою страничку в социальных сетях:
| Твитнуть |
Хотите получать на электронную почту самые свежие новости?







Новости и инфо для студентов