рефераты конспекты курсовые дипломные лекции шпоры
- Раздел Химия
- /
- Основные понятия и законы химии
Реферат Курсовая Конспект
Основные понятия и законы химии
Основные понятия и законы химии - раздел Химия, Министерство Образования И Науки ...
Министерство образования и науки
Российской Федерации
Федеральное государственное АВТОНОМНОЕобразовательное учреждение
высшего профессионального образования
Национальный исследовательский ядерный университет «МИФИ»
Волгодонский инженерно-технический институт – филиал НИЯУ МИФИ
Учебно-методическое пособие
К выполнению индивидуальных заданий и
Контрольных работ по общей химии
ВведениеОсновные понятия и законы химии
Относительная атомная масса (Аr)химического элемента показывает, во сколько раз средняя масса атома естественного изотопного состава элемента больше 1/12 массы изотопа углерода-12 (12С):
Аr = mатома: (1/12 m (12С)).
Относительная молекулярная масса (Мr)простого или сложного вещества показывает, во сколько раз средняя масса молекулы естественного изотопного состава элемента больше 1/12 массы изотопа углерода-12 (12С):
Мr = mмолекулы: (1/12 m (12С)).
Атомная единица массы (а.е.м.) = 1,66·10-27кг; Аr и Мr –безразмерные величины.
Количество вещества ν – физическая величина, равная количеству молей структурных элементов, составляющих систему. Определяется ν отношением числа структурных единиц N, содержащихся в системе, к постоянной Авогадро NА:
ν = N : NА.
Моль– это количество вещества системы, содержащей столько же структурных единиц, сколько содержится атомов в углероде 12С,взятогомассой 0,012 кг. Принято считать, что число структурных единиц в одном моле численно равно постоянной Авогадро NА = 6,02·1023 моль-1.
Молярная (мольная) масса М (Х) –масса единицы количества вещества Х, т.е. масса одного моля данного вещества (г/моль). Молярная масса М (Х) численно равна его относительной молекулярной массе (Мr).
Эквивалент – это некоторая реальная или условная частица вещества, которая может замещать, присоединять, высвобождать или быть каким-либо иным способом эквивалентна одному атому или одному иону водорода в кислотно-основных или ионообменных реакциях или одному электрону в окислительно-восстановительных реакциях.
Данное определение предложено Конгрессом ИЮПАК. Однако оно отличается громоздкостью, допускает использование в количественных соотношениях реально не существующих «условных» частиц и, к тому же, страдает неопределенностью: «эквивалент - частица …, которая эквивалентна…»(тавтология!).
Кроме того, при таком определении величина эквивалента вещества становится безразмерной и тождественной фактору эквивалентности.
Более конкретным и лишенным перечисленных недостатков является следующее определение: Эквивалент вещества (Э) – это количество вещества, приходящееся на единицу его валентного химического сродства.
Под валентным химическим сродством (W) понимается произведение валентности (модуля заряда для ионов, числа отданных или принятых электронов в окислительно-восстановительной реакции) частицы (В) на их количество в формуле вещества (n):
W = В· n [безразмерна].
Эталоном эквивалента вещества принят 1 моль атомарного водорода. Расчет эквивалента любого вещества производят по формуле
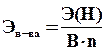 [моль].
[моль].
Безразмерная величина, показывающая, какая часть моля элемента или вещества Х эквивалентна 1 моль атомарного водорода, называется фактором эквивалентности fэ (Х):
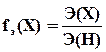 .
.
Масса одного эквивалента (эквивалентная масса) Мэ(Х), г/моль,определяется по формуле
Мэ(Х) = fэ (Х)·М(Х). (1.1)
Если в реакции участвуют газы, то могут быть найдены их эквивалентные объемы Vэ, л/моль, по формуле (при н.у.)
Vэ(Х) = fэ (Х)·22,4 .
Фактор эквивалентности химического элемента Х в его соединениях равен
где с.о. – степень окисления элемента Х в данном соединении. Пример 1.Найти величины факторов эквивалентности и эквивалентных масс для азота в следующих веществах: NН3, НNО3,…Фактор эквивалентности вещества Х, участвующего в окислительно-восстановительном процессе, равен
где Nе – количество электронов, которые теряет или присоединяет одна молекула вещества Х. Пример 2.Найти величину фактора эквивалентности, эквивалентные массу и объем… Решение.В данном химическом процессе степень окисления серы изменяется от –2 (Н2S) до +4 (SO2). Следовательно,…Фактор эквивалентности вещества Х, участвующего в ионообменном процессе, равен
где Ni и zi - соответственно число и заряд ионов, которыми обменивается молекула реагирующего вещества со своим партнером. Многоосновные кислоты НnА и многокислотные основания М(ОН)n имеют по n… Для солей фактор эквивалентности может быть найден по числу замещенных катионов или анионов.Следствия из закона Авогадро.
1. 1 моль любого газа при данных условиях занимает один и тот же объем – молярный объем.
2. При нормальных условиях 1 моль различных газов занимает объем 22,4 л.
Относительная плотность одного газа по другому.
Молярную массу газа можно определить по его плотности ρ[г/л] :
Мгаза= 22,4· ρ.
Плотности газов при одинаковых условиях относятся как их молярные массы:
 ,
,
где D – относительная плотность одного газа по другому.
Задачи к главе 1
Й уровень
6-10. Оксид n-валентного элемента содержит Х% этого элемента. Вычислите эквивалентные и мольные массы элемента и оксида. Какой элемент образует… 11-15. При превращении m1, г, хлорида металла в сульфат было затрачено m2, г,…Й уровень
16.КMnО4+КОН+К2SО3→К2МnО4+К2SО4+Н2О 17.KJО3+Н2SО4+Nа2SО3 →J2+К2SО4+Nа2SО4+Н2О 18.Al(OH)3 + H2SO4 →AlOHSO4 + H2OЙ уровень
36.При некоторой температуре плотность паров серы по воздуху равна 6,62. Из скольких атомов состоят молекулы серы? 37. При некоторой температуре плотность паров фосфора по воздуху равна 4,28.… 38.Плотность галогеноводорода по воздуху равна 4,41. Какова плотность этого газа по водороду?СОСТАВ И СТРОЕНИЕ АТОМА. ХИМИЧЕСКАЯ СВЯЗЬ.
Состав атома
Количество элементарных частиц (протонов р, электронов и нейтронов n) можно определить по формулам: ;(2.1) ,(2.2),Строение электронных оболочек
(2.3) Пример 2.Сколько протонов и нейтронов содержат ядра изотопа ? Написать электронную формулу рассматриваемого элемента,…Геометрические и энергетические характеристики атомов
Энергия ионизации Еi –это энергия, необходимая для отрыва наиболее слабо связанного электрона от атома, количественно выражается в кДж/моль или эВ.… Энергия сродства к электрону Еср –энергия, выделяющаяся при присоединении… Электроотрицательностью элемента (ЭО)называют меру относительной способности атомов оттягивать на себя электроны при…Химическая связь.
Важнейшими видами химической связи являются: ковалентная, ионная водородная, металлическая, межмолекулярная. При образовании ковалентной связи между атомами их электроны обобщаются и… Число общих электронных пар,соединяющих два атома,определяет кратность химической связи.Задачи к главе 2
Й уровень
46-50. Укажите в периодической системе элемент, валентные электроны которого имеют конфигурацию Z. Напишите полную электронную формулу этого… 51-55. Какие значения квантовых чисел n, l, m1, ms, имеют валентные электроны… 56-60. Составьте уравнение реакции ядерного обмена согласно схеме для изотопа элемента, содержащего Z протонов с…ХИМИЧЕСКАЯ ТЕРМОДИНАМИКА
Термодинамика – наука о превращениях энергии. Химическая термодинамика применяет законы термодинамики к свойствам и поведению веществ в химических… - внутренняя энергия U – полная энергия частиц, составляющих данное вещество;… - энтальпия системы Н – термодинамическая функция, характеризующая систему, находящуюся при постоянном давлении,…Термохимия
Количество энергии относят к такому числу молей вещества, которое указано в уравнении реакции, и называют его тепловым эффектом (теплотой) Q… Для реакций, протекающих при постоянном давлении и постоянной температуре,… Тепловой эффект реакции образования одного моля вещества из простых веществ называется теплотой образования DН данного…Химическое сродство
Т.к. энтропия является функцией состояния системы, то для вычислений изменения стандартной энтропии химической реакции DSх.р применяют следствие из… .Задачи к главе 3
Й уровень
Задачи Реакции A B C DЙ уровень
126-130. Вычислите, какое количество теплоты выделится при восстановлении оксида А металлом Б, если было получено m, г, восстановленного металла: … 131-135. Оцените при стандартных условиях возможность самопроизвольного… 136-140. Определите знаки при D Н° и D S° для реакции, протекающей при стандартных условиях в прямом направлении. Как…ХИМИЧЕСКАЯ КИНЕТИКА И РАВНОВЕСИЕ
Химическая кинетика
На скорость реакции существенное влияние оказывают концентрации реагирующих веществ, давление в системе (для газовых реакций), температура, природа… Зависимость скорости от концентрации реагирующих веществ описывается законом… Для гомогенной реакцииХимическое равновесие
Химическое равновесие имеет динамический характер. Скорость реакции (число частиц, образующихся в единицу времени в единице объема) в прямом… Для реакции, протекающей по уравнению: аА(г) + bВ(г) ↔ cC(г)+ dD(г)Решение.
2. Влияние общего давления в системе. Если в результате реакции изменяется число молей газообразных веществ, то изменение общего давления в системе… 3. Влияние температуры. С увеличением температуры равновесие смещается в… 2Н2 + О2 = 2Н2О (ΔΗ<0)Й уровень
161 – 165 Во сколько раз изменится скорость прямой гомогенной реакции, если концентрацию вещества А увеличить в X раз, а концентрацию вещества В… 166-170. Температурный коэффициент скорости некоторой реакции равен g. Во… 171-175. Равновесие в гомогенной газовой системе установилось в момент, когда прореагировало 50% вещества А. Вычислите…Й уровень
181.Определите энергию активации реакции, константа скорости которой… 182. Протекают две реакции. Энергия активации первой из них на 10 кДж меньше, чем у второй. Во сколько раз скорость…Задачи к главе 5
Й уровень
211-215. Какую массу вещества А необходимо растворить в воде, чтобы получить 3 л 0,5 М раствора? Какова массовая доля (%) и моляльность этого… 216-220.Какой объем (мл) x-молярного раствора Н3PО4 можно приготовить из V,…Й уровень
226-230. Смешали m1, г, X %-го по массе раствора Н2SО4 и m2, г, Y%-го по массе… 231-235. К V, мл, 8,28%-го раствора NaОН плотностью 1,09 г/мл прибавили m, г X %-го раствора NаОН. Вычислите массовую…Й уровень
241-245. В каком объеме воды нужно растворить m, г, кристаллогидрата А, чтобы…Свойства растворов неэлектролитов
Разбавленные растворы неэлектролитов обладают рядом свойств, количественное выражение которых зависит от числа находящихся в растворе частиц… Зависимость этих свойств от концентрации выражается уравнениями, являющимися… 1. Относительное понижение давления паров растворителя над раствором (D р) равно мольной доле растворенного…Задачи к главе 6
Й уровень
251-255. Вычислите молярную массу вещества, если раствор, содержащий m, г, этого вещества на каждый литр воды, замерзает при температуре t°? … 256-260. Вычислить осмотическое давление раствора, содержащего m, г, вещества…Й уровень
266-270. Вычислите температуру кипения X %-го водного раствора вещества А: Задачи … 271-275.Сколько грамм вещества А нужно растворить в V л воды, чтобы…Й уровень
281-285. В каком отношении должны находиться массы воды и спирта А, чтобы при их смешивании получить раствор, кристаллизующийся при температуре t? …СВОЙСТВА РАСТВОРОВ ЭЛЕКТРОЛИТОВ
Электролитическая диссоциация
Δtпл = i·Кк·Сm, , Росм=1000i·См·RT.Произведение растворимости
AmBn↔mAn++ nBm-, то выражение для ПР будет иметь вид ПРAmBn =[Аn+]m·[Вm-]n.ЗАДАЧИ К ГЛАВЕ 7
Й уровень
291-295. Вычислить ионную силу и активность ионов в растворе, содержащем А, моль/ дм3 Са(NO3)2 и В, моль/дм3 СаCl2 Задачи … 296-300. Концентрация малорастворимого вещества А в его насыщенном растворе равна с, моль/л. Вычислите произведение…Й уровень
302.При 100ºC давление пара раствора, содержащего 0,05 моля сульфата натрия в 450 г воды, равно 100,8 кПа. Определить кажущуюся степень… 303. В 1 дм3 0,01 М раствора уксусной кислоты содержится 6,26·1021 ее молекул… 304. Кажущаяся степень диссоциации хлорида калия в 0,1 н растворе равна 0,80. Чему равно осмотическое давление этого…Й уровень
312.В равных количествах воды растворено в одном случае 0,5 моль сахарозы С12Н22О11, а в другом 0,2 моля СаCl2. Температуры кристаллизации обоих… 313. Рассчитать концентрацию ионов СН3СОО- в растворе, 1 дм3 которого содержит… 314. Исходя из значений последовательных констант диссоциации ортофосфорной кислоты (К1 = 7,5 ·10-3; К2 = 6,3 ·10-8;…ИОННОЕ ПРОИЗВЕДЕНИЕ ВОДЫ. ВОДОРОДНЫЙ ПОКАЗАТЕЛЬ.
Н2О↔ Н+ + ОН- Константа диссоциации воды весьма мала и составляет при 25ºC:Задачи к главе 8
Й уровень
Й уровень
326-330. Определить [Н+] и [ОН-] в растворе, рН которого равен А:
| Задачи | |||||
| А |
Й уровень
332. Рассчитать рН 0,1н раствора уксусной кислоты, содержащего, кроме того, 0,1 моль/дм3СН3СООNa. Коэффициенты активности ионов считать равными… 333.Во сколько раз концентрация ионов водорода в крови (рН = 7,36) больше, чем… 334. Определить активность ионов водорода и значение раН+ в 2,5·10-3 М растворе НСl, содержащем, кроме того, 2,5·10-3…ИОНООБМЕННЫЕ РЕАКЦИИ. ГИДРОЛИЗ СОЛЕЙ
Пример 1.Записать в молекулярной и ионно-молекулярной формах уравнения реакций… Решение:Задачи к главе 9
Й уровень
341-345. Составьте уравнения гидролиза солей А и Б в молекулярной и…Й уровень
361-365. Укажите направление смещения равновесия гидролиза соли А при добавлении к раствору веществ Б, В и Г: Задачи … 366-370. Какое из веществ Б, В или Г следует добавить к раствору соли А, чтобы…Й уровень
Для каждого случая указать причину смещения равновесия в сторону прямой реакции. 376-380.Значение рН 0,1 М раствора соли А составляет В. Рассчитайте константу… 381-385. Вычислите рН водного раствора А с концентрацией с, моль/л, если степень диссоциации α = 0,8: …КОМПЛЕКСНЫЕ СОЕДИНЕНИЯ
1) центральное место занимает комплексообразователь – обычно положительно заряженный ион; 2) вокруг комплексообразователя расположены или координированы лиганды… 3) находится координационное число, показывающее, сколько лигандов удерживает комплексообразователь.ЗАДАЧИ К ГЛАВЕ 10
Й уровень
Й уровень
Й уровень
ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ РЕАКЦИИ
Окислительно-восстановительными называются реакции, которые сопровождаются изменением степени окисления атомов, входящих в состав реагирующих… - что степень окисления атома в молекуле простого вещества равна нулю; - степень окисления атома водорода во всех соединениях, кроме гидридов щелочных и щелочноземельных металлов равна…Задачи к главе 11
Й уровень
Задачи Элементы, соединения, реакции A – N; Б – N 2O5; B – NH3; Г – NO3-. Реакция KIO3 + H2SO4… 406-410. Определите степень окисления элемента А в частицах Б, В, Г. Используя электронно-ионный метод, расставьте…Й уровень
421-425. Определите количество электронов, отдаваемое или принимаемое элементом А в переходах А®Б, А®В, А ®Г, Б®В, Б ®Г, В®Г. Используя… 426-430. Составьте электронные уравнения окисления или восстановления элемента…Й уровень
436-440. Пользуясь таблицей стандартных электродных потенциалов (прил. 6) вычислите константы равновесия реакций. Используя электронно-ионный метод,…ЭЛЕКТРОХИМИЧЕСКИЕ ЯВЛЕНИЯ
Таким образом, электрохимия – это раздел химии, изучающий закономерности протекания химических реакций, сопровождающихся взаимопревращениями… Самопроизвольно электрохимические процессы протекают в гальванических… В любой электрохимической системе электрод, на котором протекает окислительный процесс, называется анодом. Катодом…Гальванический элемент
Элемент состоит из двух электродов (например, цинк и медь), опущенных в растворы собственных солей (или другого электролита) и соединенных… Растворы солей также приведены в электрический контакт полупроницаемой… При этом через проводник протекает электронный ток, а на электродах в растворе электролита протекают…Электролиз
Меn++ ne= Ме0 На аноде – окисление соответствующих анионов: Аnm—- me- = Аn0Задачи к главе 12
Й уровень
446-450. Вычислите потенциал отрицательного электрода в растворе, содержащем А, г, соли и Б, мл, воды: Задачи Схема… 451-455. Вычислите потенциал положительного электрода в растворе, содержащем… 456-460. Какая масса металла осаждается на катоде при электролизе раствора соли А силой тока I ампер в течение t мин?…Уровень
С1, моль/(кг воды), положительного электрода - С2, моль/(кг воды): Задачи Схема гальванического элемента … 476-480. Рассчитайте моляльную концентрацию потенциалопределяющих ионов… 481-485. Рассчитайте моляльную концентрацию потенциалопределяющих ионов положительного электрода указанного…Й уровень
Задачи Схема гальванического элемента (-) Сr/Сr2(SО4)3//Со(NO3)2/Со(+) … 506-510. Определите константу равновесия токообразующей реакции, протекающей в… 511-515. Через раствор А пропускают ток силой I ампер в течение t мин. Используя только закон Фарадея, определите…ПРИЛОЖЕНИЯ
Приложение 1
Таблица вариантов контрольных заданий
| Номер варианта | Номер уровня | Номера задач | ||||||||||||
| 00. | ||||||||||||||
Приложение 2
Относительная электроотрицательность элементов
Приложение 3
Термодинамические свойства простых веществ и соединений
Приложение 4
Произведения растворимости труднорастворимых веществ
Приложение 5
Термодинамические свойства ионов в водных растворах
Приложение 6
Стандартные электродные потенциалы в водных растворах
Приложение 7
Растворимость неорганических веществ в воде при комнатной температуре
Приложение 8
Названия некоторых кислот и их кислотных остатков
ОГЛАВЛЕНИЕ Введение 3 Общие методические указания 3– Конец работы –
Используемые теги: основные, понятия, законы, химии0.067
Если Вам нужно дополнительный материал на эту тему, или Вы не нашли то, что искали, рекомендуем воспользоваться поиском по нашей базе работ: Основные понятия и законы химии
Что будем делать с полученным материалом:
Если этот материал оказался полезным для Вас, Вы можете сохранить его на свою страничку в социальных сетях:
| Твитнуть |
Хотите получать на электронную почту самые свежие новости?







Новости и инфо для студентов