И элиминирования у насыщенного атома углерода
Реакции нуклеофильного замещения у sp3- гибридизованного атома углерода: гетеролитические реакции, обусловленные поляризацией s- связи углерод - гетероатом (галогенопроизводные, спирты).
Эти реакции протекают по механизму нуклеофильного замещения.
Для первичных и вторичных соединений предполагается механизм нуклеофильного замещения второго порядка (SN2), для третичных веществ – нуклеофильного замещения первого порядка (SN1).
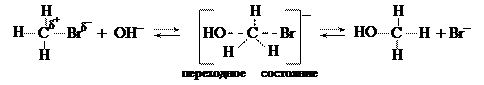 |
В случае первичных и вторичных алкилгалогенидов отрицательно заряженная гидроксильная группа атакует положительно заряженный атом углерода со стороны, противоположной отрицательно заряженному атому брома. При наличии достаточной энергии гидроксил приближается настолько, что между ним и атомом углерода начинает образовываться связь, а связь между атомами углерода и иода начинает разрываться. В этом переходном состоянии атом углерода и все три водородных атома находятся в одной плоскости (молекула «уплощена»). Затем анион иода выталкивается и образуется молекула метилового спирта. Такой процесс носит название реакции нуклеофильного замещения второго порядка (SN2): нуклеофильного потому, что атакующая частица заряжена отрицательно; второго порядка — т.к. скорость реакции зависит от концентрации и йодистого метила, и гидроксила. Если исходное соединение было оптическим активным, то в процессе реакции произойдёт обращение конфигурации: например, при гидролизе D-2-бромбутана образуется L-2-бутанол.
У третичных алкилгалогенидов подход отрицательно заряженной частицы затруднен имеющимися объемными заместителями, и процесс идет по другому механизму. Хотя и в очень малой степени, но все же происходит процесс диссоциации третичного бромистого бутила:
(CH3)3C – Br « (CH3)3C+ + Br- (очень медленно)
Образующийся третичный бутилкатион мгновенно реагирует с находящимися в растворе нуклеофильными частицами:
(CH3)3C+ + HO- ® (CH3)3C – OH (очень быстро)
В этом случае скорость реакции зависит только от процесса диссоциации и, следовательно, от концентрации в реакционной смеси третичного бромистого бутила и реакция в целом называется реакцией нуклеофильного замещения первого порядка - sn1. Если в реакцию вступает оптически активное соединение, то в результате образуется оптически неактивная рацемическая смесь.
Хорошо уходящие группы – это такие группы, протонированные формы которых соответствуют сильным кислотам, например: Hal–, H2O, ROH, NH3 (протонированные формы: галогеноводородные кислоты HHal, ионы: гидроксония Н3О+, алкилоксония ROH2+, аммония NH4+ — сильные кислоты).
Плохо уходящие группы – это такие группы, протонированные формы которых соответствуют слабым кислотам, например: OH–, NH2–, SH–, OR– и др. В этом случае для протекания реакций необходимо протонирование, т.е. кислотный катализ, что позволит перевести плохоуходящую группу в хорошоуходящую.
На последней (быстрой) стадии реакции замещения происходит конкуренция за карбкатион между двумя частицами: галогенид-ионом (если в качестве кислоты использовали галогеноводородную кислоту) и молекулой воды, выступающей в роли акцептора протона. В первом случае происходит нуклеофильное замещение (SN) гидроксила на галоген, а во втором — элиминирование (Е) — отщепление протона.