Тиск насиченої водяної пари
Температура, 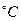
| Тиск , кПа | Температура, 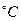
| Тиск , кПа |
| 1,597 | 2,189 | ||
| 1,705 | 2,337 | ||
| 1,817 | 2,486 | ||
| 1,935 | 2,642 | ||
| 2,062 | 2,841 |
Температура повітря в приміщенні дорівнює Т = 273 + t0С.
Використовуючи закону еквівалентів 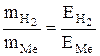 , визначити еквівалентну масу металу, враховуючи, що
, визначити еквівалентну масу металу, враховуючи, що 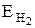 = 1 г/моль.
= 1 г/моль.
2.Через об’єм виділеного водню, приведений до нормальних умов.
Застосовуючи рівняння об’єднаного газового закону 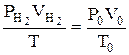 привести об’єм виділеного водню до нормальних умов (V0).
привести об’єм виділеного водню до нормальних умов (V0).
Знайти еквівалентну масу металу за формулою:
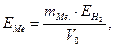
де 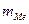 - наважка металу (г);
- наважка металу (г);
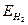 - еквівалентний об’єм водню (дорівнює 11200 мл/моль за н. у.).
- еквівалентний об’єм водню (дорівнює 11200 мл/моль за н. у.).
Обчислити середню еквівалентну масу металу.
Розрахувати атомну масу металу через співвідношення еквівалентної маси металу і валентності (В):
А = ЕМе∙В
Використовуючи періодичну таблицю елементів Д.І.Менделєєва, визначити назву металу. Зробити висновок.
Контрольні питання.
1. Визначити еквівалентні маси наступних речовин: N2O5;H3PO4; Ва(ОН)2; Ca3(PO4)2; FeCl3; MgHPO4; AlOH(NO3)2.
2. При розчиненні у кислоті 3,06 г металу виділилося 2,8 л водню за н.у. Визначити молярну масу еквіваленту металу.
3. Визначити атомну масу двовалентного металу, якщо для окиснення 8,34 г металу використано 0,680 л кисню (н.у.).
4. При нагріванні 0,92 г олова у кисні утворилось 1,17 г оксиду. Знайти валентність олова у цьому оксиді і записати його формулу.
5. Масова частка алюмінію у його хлориді складає 20,22%. Обчислити молярну масу еквіваленту алюмінію, валентність і скласти формулу хлориду.