рефераты конспекты курсовые дипломные лекции шпоры
- Раздел Биология
- /
- Пространственная (стереоизомерия)
Реферат Курсовая Конспект
Пространственная (стереоизомерия)
Пространственная (стереоизомерия) - раздел Биология, Биологически активные вещества растительного происхождения Пространственная Изомерия Обусловлена Различным Пространственным Расположение...
Пространственная изомерия обусловлена различным пространственным расположением атомов при одинаковом порядке их связывания.
Различают:
1) геометричекую (цис-, транс-изомерию)
Наиболее устойчивы транс-изомеры, поэтому в природе они наиболее распространены.
Цис-форма — 2 заместителя расположены по одну сторону плоскости двойной связи.
Транс-форма – 2 заместителя расположены по разные стороны плоскости двойной связи.
2) Оптическая изомерия
Для описания пространственных различий используют два важнейших понятия: конфигурация и конформация молекул.
Конфигурация –определенное пространственное расположение атомов в молекуле, без учета различий, возникающих вследствие вращения вокруг одинарных связей.
В основе пространственного строения лежит предположение Вант-Гоффа (1874 г) о тетраэдрической конфигурации атома углерода, которое впоследствии было полностью подтверждено. Если у атома углерода все четыре заместителя одинаковые, то пространственная модель - тетраэдр, валентный угол – 109,50. Если заместители разные, то угол несколько отличается от нормального. На плоскости обычно изображают атом углерода и две связи. Связь, направленную к наблюдателю показывают жирной чертой, от наблюдателя за плоскостью — пунктирной или заштрихованной линией.
Термин конформациябыл предложен в 1929 году Хеуорсом,
Конформации молекулы представляют собой различные ее геометрические формы, возникающие в результате вращения вокруг одинарных связей. Оперировать бесчисленным множеством конформаций практически невозможно, поэтому принимают во внимание молекулярные структуры, в которых последовательно осуществлен поворот вокруг простой связи на 600 , При полном обороте вокруг центральной связи возникает 6 конформаций.
7. Оптическая изомерия; хиральность молекул органических соединений. Энантиомеры и диастереомеры. Связь пространственного строения с физиологической активностью органических соединений.
Энантиомеры — пара стереоизомеров, представляющих собой зеркальные отражения друг друга, не совмещаемые в пространстве. Простейший пример такой молекулы — это атом углерода с четырьмя разными заместителями. К примеру, СHClBrF или аланин CH3CHNH2COOH (рис. 1). Наличие у такой молекулы двух разных конфигураций связано с тем, что у атома углерода, образующего четыре одинарные связи, эти связи направлены к вершинам тетраэдра.
|
Диастереомеры — стереоизомеры, не являющиеся зеркальными отражениями друг друга Диастереомерия возникает, когда соединение имеет несколько стереоцентров. Если два стереоизомера имеют противоположные конфигурации всех соответствующих стереоцентров, то они являются энантиомерами. Однако, если конфигурация различается лишь у некоторых (а не у всех) стереоцентров, то такие стереизомеры являются диастереомерами. Если диастереомеры отличаются конфигурацией лишь одного стереоцентра, то они называются эпимерами.

Атом углерода с четырьмя разными заместителями называется хиральным атомом (от греческого heiros «ладонь» — тот же корень, что и в слове «хиромантия»). Чем больше хиральных атомов в молекуле, тем больше у вещества может быть оптических изомеров. Интересно, что возможны органические вещества, которые имеют оптические изомеры, хотя в них формально нет ни одного хирального атома — центра изомерии.
Биологическая активность зависит от оптического строения. Некоторые ферменты могут взаимодействовать только с одним изомером одного вещества (абсолютная специфичность) либо с определенным изомером веществ гомологического ряда (стереоспецифичность)
8. Типы реакций в биоорганической химии: SR, SE, SN, AE, AN, E. Примеры
В настоящее время приняты три типа классификаций химических реакций.
1. По направлению реакции.
Этот тип делится на две большие группы. К первой группе относят реакции, протекающие без изменения структуры углеродного скелета (порядок соединения атомов углерода в молекуле продукта реакции аналогичен порядку соединения атомов углерода в исходном веществе). Ко
второй группе относят реакции, протекающие с изменением структуры углеродного скелета (порядок соединения атомов углерода в продукте реакции отличается от порядка соединения атомов углерода в исходном веществе). Первую группу реакций (I) составляют реакции замещения (S), присоединения (А), элиминирования или отщепления (Е), некоторые реакции перегруппировки и изомеризации. Вторую группу реакций (II) составляют реакции удлинения углеродной цепи, укорочения углеродной цепи, некоторые реакции изомеризации и перегруппировки, циклизации, раскрытия цикла, сжатия и расширения цикла и некоторые другие.
2. По характеру атакующих частиц – реагентов (по типу разрыва связей).
Бывают гомолитическими (или радикальными) и гетеролитическими (или полярными), которые рассмотрим ниже.
В реакциях принято различать атакуемое вещество – субстрат и атакующее вещество (или частицу) – реагент. В зависимости от характера реагента различают реакции нуклеофильные, радикальные и электрофильные. Часто эту классификацию сочетают с классификацией по направлению реакции, что обычно и используют в органической химии. Тогда говорят о реакциях радикального присоединения (AR), электрофильного присоединения (AE), нуклеофильного присоединения (AN), радикального замещения (SR), нуклеофильного замещения (SN), электрофильного замещения (SE), где A,S,E – тип реакции, а индексы R,N,E – тип атакующей частицы (реагента)

3. По молекулярности реакции.
«Молекулярность» реакции указывает на число молекул, в которых происходит изменение ковалентных связей в стадии, определяющей (лимитирующей) суммарную скорость реакции – самой медленной стадии реакции. Если в стадии, лимитирующей скорость реакции, участвует одна молекула, то реакцию считают мономолекулярной, если две – то бимолекулярной. Полимолекулярные реакции встречаются очень редко.
– Конец работы –
Эта тема принадлежит разделу:
Биологически активные вещества растительного происхождения
Биоорганическая химия наука которая изучает связь между строением органических веществ и их биологическими функциями Как самостоятельная наука... Методы Основной арсенал составляют методы органической химии для решения... Объекты изучения...
Если Вам нужно дополнительный материал на эту тему, или Вы не нашли то, что искали, рекомендуем воспользоваться поиском по нашей базе работ: Пространственная (стереоизомерия)
Что будем делать с полученным материалом:
Если этот материал оказался полезным ля Вас, Вы можете сохранить его на свою страничку в социальных сетях:
| Твитнуть |
Хотите получать на электронную почту самые свежие новости?


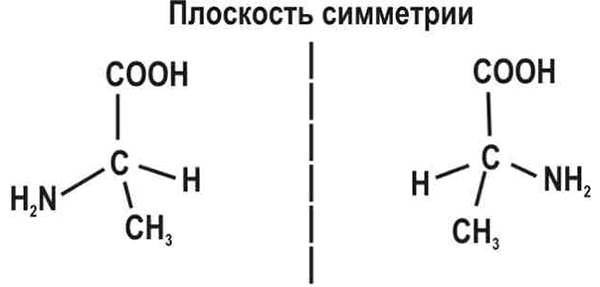 Рис. 1. Аминокислота аланин CH3CHNH2COOH. Две молекулы, состоящие из атома углерода с четырьмя разными заместителями, — оптические изомеры. Живые существа используют только левовращающие изомеры аминокислот (на рисунке справа)
Рис. 1. Аминокислота аланин CH3CHNH2COOH. Две молекулы, состоящие из атома углерода с четырьмя разными заместителями, — оптические изомеры. Живые существа используют только левовращающие изомеры аминокислот (на рисунке справа)





Новости и инфо для студентов