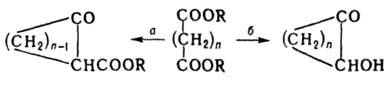Карбонильные соединения в биоорганической химии. Строение, химические свойства, медикобиологическое значение альдегидов и кетонов.
Карбонильные соединения содержат карбонильную группу С=О. Один из наиб. распространенных типов неорг. и орг. в-в. К ним относятся, напр., СО, СО2, карбонаты, мочевина. Однако под карбонильными соединениями в узком смысле понимают лишь альдегиды и кетоны, а также (в меньшей степени) карбоновые кислоты и их производные. Карбонильные соединения высоко реакционноспособны. Группа С=О способна восстанавливаться до спиртовой или метиленовой группы. Из-за наличия частичного положит. заряда на атоме С карбонильные соединения присоединяют разл. нуклеофилы, напр., амины, металлоорг. соед., вступают в р-ции электроф. замещения в ароматич. кольце. Р-ции с нуклеофилами часто сопровождаются дальнейшим отщеплением воды с образованием производных карбонильных соединений, напр., гидразонов, шиффовых оснований. Если группа С=О связана с гетероатомом, несущим неподеленную пару электронов, напр., в карбоновых к-тах и их производных, то р-ции по этой группе с нуклеофилами могут затрудняться, а с электрофилами (к-тами) облегчаться. Благодаря подвижности атомов Н у соседнего с карбонильной группой атома С (a-С-атома) карбонильные соединения сравнительно легко, в особенности при катализе к-тами или основаниями, переходят в енольную форму Енолизация или образованиеенолят-аниона первая стадия мн. важных р-ций карбонильных соединений, где они выступают в качестве С-нуклеофильных реагентов. К таким р-циям относятся галогенирование по a-С-атому, альдольная и кретоновая конденсации, присоединение к активир. кратным связям (реакция Михаэля ) и др.
У альдегидов карбонильный углерод соединен с атомом Н и органической группой R (общая формула RHC=O)
Применение альдегидов в медицине.
Формальдегид (формалин).Применяют как дезинфицирующее и дезодорирующее средство для мытья рук, обмывания кожи при повышенной потливости (0,5-1 %), для дезинфекции инструментов (0,5 %), для спринцеваний (1:2000 - 1:3000). Входит в состав лизоформа.
Формидрон - жидкость, содержащая раствора формальдегида 10 частей, спирта этилового 95 % 40 частей, воды 50 частей, одеколона 0,5 частей. Применяют для протирания кожи при повышенной потливости.
Мазь формальдегидная. Применяют при повышенной потливости, втирают в подмышечняю впадины один раз в сутки, в межпальцевые складки.
Лизоформ мыльный раствор формальдегида. Состав: формалина 40 частей, мыла калийного 40 частей, спирта 20 частей. Оказывает дезинфицирующее и дезодорирующее действие. Применяют для спринцевания в гинекологической практике, для дезинфекции рук (1-3 % растворы).
Уротропин (гексаметилентетрамин), бесцветные кристаллы без запаха, легко растворимы в воде. Водные растворы имеют щелочную реакцию. Применяют главным образом при инфекционных процессах мочевыводящих путей (циститах, пиелитах)
Кетоны — органические соединения общей формулы R—CO—R (где R — углеводородные радикалы, например СН3—, СН3 — СН2— и т. д.). Низшие кетоны — жидкости с характерным запахом, например ацетон (СН3)2CO, высшие — твердые вещества, например камфора. К классу кетонов относятся также стероидные гормоны (эстрон, кортизон и др.), многие из которых применяются в медицине в разных целях.
12. Карбоновые кислоты в биоорганической химии. Строение, химические свойства. Функциональные производные карбоновых кислот: ангидриды, амиды, сложные эфиры. Реакции декарбоксилирования.
Карбо́новые кисло́ты — класс органических соединений, молекулы которых содержат одну или несколько функциональных карбоксильных групп -COOH. Кислые свойства объясняются тем, что данная группа может сравнительно легко отщеплять протон. За редкими исключениями карбоновые кислоты являются слабыми. Например, у уксусной кислоты CH3COOH константа кислотности равна 1,75·10−5. Ди- и трикарбоновые кислоты более сильные, чем монокарбоновые
В зависимости от радикала, связанного с карбоксилом, различают следующие группы карбоновых кислот:
· ароматические
· алифатические (в том числе предельные и непредельные)
· алициклические
· гетероциклические.
По числу карбоксильных групп кислоты могут быть одно-, двух- и многоосновными. При введении в молекулы кислоты других функциональных групп (например, -ОН, =CO, -NH2 и др.) образуются окси-, кето-, аминокислоты и другие классы соединений. Эти соединения вступают в те же реакции, что и карбоновые кислоты, плюс ко всему протекают реакции и по замещенной группе.
Наиболее важные химические свойства, характерные для большинства карбоновых кислот:
1. Карбоновые кислоты при реакции с металлами, их оксидами или их осно́вными гидроксидами дают соли соответствующих металлов:
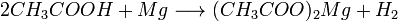
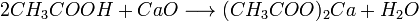
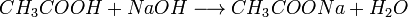
2. Карбоновые кислоты могут вытеснять более слабую кислоту из её соли, например:
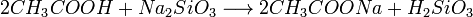

3. Карбоновые кислоты в присутствии кислого катализатора реагируют со спиртами, образуя сложные эфиры (реакция этерификации):
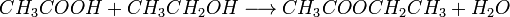
4. При нагревании аммонийных солей карбоновых кислот образуются их амиды:
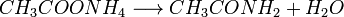
5. Под действием 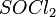 карбоновые кислоты превращаются в соответствующие хлорангидриды:
карбоновые кислоты превращаются в соответствующие хлорангидриды:
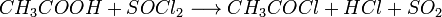
13. Строение и свойства дикарбоновых кислот.
Дикарбоновыекислоты, орг. соед., содержащие две карбоксильные группы СООН. Называют их аналогично карбоновым кислотам; многие дикарбоновые кислоты имеют тривиальные назв., которые, как правило, и используются (см. табл.). Дикарбоновые кислоты- кристаллич. в-ва. Т-ры плавления алифатич. дикарбоновых кислот с четным числом атомов С значительно выше, а р-римость в воде меньше, чем соответствующие показатели соседних нечетных гомологов. Первая константа диссоциации дикарбоновых кислот выше, чем соответствующих монокарбоновых к-т, что особенно заметно у низших гомологов.
Дикарбоновые кислоты проявляют все св-ва карбоновых к-т, образуя как моно-, так и дипроизводные. Взаимное влияние и взаимод. двух карбоксильных групп вызывает ряд р-ций, характерных только для дикарбоновых кислот. При нагр. низшие алифатич. дикарбоновые кислоты (щавелевая, малоновая) легко декарбоксилируются; к-ты, содержащие 2-3 атома С между карбоксилами, при нагр. или при действии дегидратирующих агентов образуют циклич. ангидриды, а высшие дикарбоновые кислоты - полимерные ангидриды. Образование циклич. продуктов характерно и для производных дикарбоновых кислот, напр., эфиров, дающих эфиры циклич. b-кетокислот (а)и восстанавливающихся в циклич. ацилоины (б):