Неорганические вещества клетки
Вода – один из самых основных компонентов живой клетки, составляет в среднем 70-80% массы клетки. В клетке вода находится в свободной (95%) и связанной (5%) формах. Помимо того, что она входит в их состав, для многих организмов это еще и среда обитания.
Роль воды в клетке определяется ее уникальными химическими и физическими свойствами, связанными главным образом с малыми размерами молекул, с полярностью ее молекул и с их способностью образовывать друг с другом водородные связи. Вода как компонент биологических систем выполняет следующие важнейшие функции:
1. Вода - универсальный растворитель для полярных веществ, например солей, сахаров, спиртов, кислот и др. Вещества, хорошо растворимые в воде, называются гидрофильными.
2. Молекулы воды участвуют во многих химических реакциях, например при гидролизе полимеров.
3. В процессе фотосинтеза вода является донором электронов, источником ионов водорода и свободного кислорода.
4. Неполярные вещества вода не растворяет и не смешивается с ними, поскольку не может образовывать с ними водородные связи. Нерастворимые в воде вещества называются гидрофобными.
5. Вода обладает высокой удельной теплоемкостью. Для разрыва водородных связей, удерживающих молекулы воды, требуется поглотить большое количество энергии. Это свойство обеспечивает поддержание теплового баланса организма при значительных перепадах температуры в окружающей среде.
6. Вода отличается высокой теплопроводностью, что позволяет организму поддерживать одинаковую температуру во всем его объеме.
7. Вода характеризуется высокой теплотой парообразования, т. е. способностью молекул уносить с собой значительное количество тепла при одновременном охлаждении организма. Благодаря этому свойству воды, проявляющемуся при потоотделении у млекопитающих, тепловой одышке у крокодилов и других животных, транспирации у растений, предотвращается их перегрев.
8. Для воды характерно исключительно высокое поверхностное натяжение. Это свойство имеет большое значение для передвижения растворов по тканям (кровообращение, восходящий и нисходящий токи в растениях). Многим мелким организмам поверхностное натяжение позволяет удерживаться на воде или скользить по ее поверхности.
9. Вода обеспечивает передвижение веществ в клетке и организме, поглощение веществ и выведение продуктов метаболизма.
10. У растений вода определяет тургор клеток, а у некоторых животных выполняет опорные функции, являясь гидростатическим скелетом (круглые и кольчатые черви, иглокожие).
11. Вода - составная часть смазывающих жидкостей (синовиальной - в суставах позвоночных, плевральной - в плевральной полости, перикардиальной - в околосердечной сумке) и слизей (облегчают передвижение веществ по кишечнику, создают влажную среду на слизистых оболочках дыхательных путей). Она входит в состав слюны, желчи, слез и др.
Свойства, функции и значение воды
| Свойства и функции воды | Значение воды |
| Полярность молекулы | Универсальный растворитель, среда для протекания химических реакций |
| Большая теплоемкость | Поддержание теплового равновесия клетки и организма |
| Высокая теплопроводность | Равномерное распределение теплоты между клетками и тканями организма |
| Несжимаемость | Создает тургорное давление |
| Подвижность молекул | Обеспечивает осмос |
| Источник ионов водорода | Синтез АТФ в митохондриях и пластидах |
| Донор электронов | Фотолиз воды при фотосинтезе |
Минеральные соли. Молекулы солей в водном растворе распадаются на катионы и анионы. Наибольшее значение имеют катионы (К+, Na+, Са2+, Mg2+, NH4+) и анионы (Сl- , Н2Р04 -, НР042- , НС03 -, NO3 2-, SO4 2- ) .Некоторые ионы участвуют в активации ферментов, создании осмотического давления в клетке, в процессах мышечного сокращения, свертывании крови и др. Ряд катионов и анионов необходим для синтеза важных органических веществ (например, фосфолипидов, АТФ, нуклеотидов, гемоглобина, хлорофилла и др.), а также аминокислот, являясь источниками атомов азота и серы. Соляная кислота входит в состав желудочного сока. Соли кальция и фосфора присутствуют в костной ткани животных и человека.
Органические вещества. Основой всех органических соединений является углерод (С), который образует связи с другими атомами и их группами. В результате образуются сложные химические соединения, разные по строению и функциям, - макромолекулы (от греч. macros – большой).
Макромолекулы состоят из повторяющихся низкомолекулярных соединений, - мономеров (от греч. monos – один).
Полимер (от греч. poly – много) – макромолекула, образованная мономерами.
В молекулах полимеров мономеры могут быть одинаковые или разные. В зависимости от того, какие мономеры входят в состав полимеров, полимеры делятся на следующие группы:
Полимеры
 |
Регулярные Нерегулярные
-А-А-А-А-A-A- - А-В-А-С- В-А-А-D- C- A-
-A-S-D-A-S-D-A-S-D-
Полимеры, входящие в состав живых организмов, называются биополимеры, свойства которых зависят от строения их молекул, числа и разнообразия мономеров. Биополимеры универсальны, так как построены по единому плану у всех живых организмов. Разнообразие свойств биополимеров обусловлено различным сочетанием мономеров, образующих различные варианты. Свойства биополимеров проявляются только в живой клетке.
Углеводы, или сахариды, - органические соединения, в состав которых входят углерод, водород и кислород. Название «углеводы» они получили из-за своего химического состава: общая формула большинства из них Сn(H2O)n.
Состав и строение углеводов
| Состав | Строение |
| Химические элементы: углерод, водород, кислород (C, H, O). | Общая формула: Cn (H2 O)n, где n – не меньше трех. |
Моносахариды – простые сахара, имеющие общую формулу (СН2О)n , где n=3-9. Среди моносахаридов различают триозы (3С), тетраозы (4С), пентозы (5С) – рибоза, дезоксирибоза, гексозы (6С) – глюкоза, галактоза. Моносахариды хорошо растворяются в воде, они сладкие на вкус. Фруктоза входит в состав меда, находится в плодах, зеленых частях растений. Глюкоза находится в плодах, крови, лимфе, является основным источником энергии, входит в состав дисахаридов и полисахаридов.
Дисахариды – вещества, образованные в результате конденсации двух молекул моносахаридов с потерей одной молекулы воды. У растений - это сахароза (С12Н22О11) и мальтоза, у животных – лактоза. Сахароза – основная транспортная форма углеводов в растениях. Лактоза образуется в молочной железе и присутствует в молоке.
глюкоза + глюкоза = мальтоза;
глюкоза + галактоза = лактоза;
глюкоза + фруктоза = саxароза.
По своим свойствам дисахариды близки к моносахаридам. Они хорошо растворяются в воде и имеют сладкий вкус.
Полисахариды – это высокомолекулярные углеводы, образованные путем соединения большого числа молекул моносахаридов, У растений – крахмал, целлюлоза (клетчатка), формула (С6Н10О5)n ; у животных – гликоген, хитин. Целлюлоза – основной опорный компонент клеточной стенки у растений. Крахмал – основной резервный углевод растений. Гликоген – резервный полисахарид животных (накапливается в печени и мышцах. Хитин входит в состав покровов членистоногих, обеспечивает прочность покровных структур грибов.
Место синтеза в клетке: на мембранах гладкой эндоплазматической сети.
Локализация в клетке и организме: клеточная стенка, клеточные включения, клеточный сок растений, покровы членистоногих.
Функции углеводов:
1) Энергетическая. Углеводы – это основной источник энергии для организмов. В процессе окисления 1 г углеводов освобождается 17,6 кДж.
2) Структурная. Клеточные стенки растений построены из целлюлозы. Покровы тела членистоногих, клеточные стенки грибов состоят из хитина. Углеводы входят в состав органоидов, молекул ДНК и РНК.
3) Запасающая. Эту функцию выполняют у растений крахмал, у животных гликоген. Они обладают способностью накапливаться в клетках и расходоваться по мере возникновения потребности в энергии.
4) Защитная. Железы выделяют секреты, которые содержат углеводы. Секреты защищают стенки полых органов (желудок, кишечник) от механических повреждений, проникновения болезнетворных бактерий.
Липиды - это жироподобные вещества, большинство из которых состоит из жирных кислот и трехатомного спирта; это сложные эфиры высших жирных кислот и трехатомного спирта глицерина.
Жиры – наиболее простые и широко распространенные липиды. Жидкие жиры называются маслами. У животных масла встречаются в молоке, но чаще встречаются у растений в семенах, плодах.
Состав и строение липидов
| Состав | Строение |
| Химические элементы: углерод, водород, кислород (C, H, O). | Это сложные соединения трехатомного спирта глицерина и высокомолекулярных жирных кислот. |
Место синтеза в клетке: на мембранах гладкой эндоплазматической сети.
Локализация в клетке и организме: клеточная мембрана, клеточные включения, подкожная жировая клетчатка и сальники.
Функции липидов:
1) Энергетическая. Липиды – «энергетическое депо». При окислении 1 г липидов до СО2 и Н2О освобождается 38,9 кДж, что в два раза больше по сравнению с углеводами и белками.
2) Структурная. Липиды принимают участие в построении мембран клеток и образовании важных биологических соединений, например, гормонов, витаминов.
3) Запасающая. В растениях чаще накапливаются масла, а не жиры. Семена сои и подсолнечника богаты маслами.
4) Защитная и теплоизоляционная. Жиры плохо проводят тепло. Они откладываются под кожей животных, у некоторых достигают такие скопления толщины до 1 м, например, у китов. Жировой слой защищает животных от переохлаждения. Жировая ткань выполняет функцию терморегулятора. У китов, кроме того, он играет еще и другую роль — способствует плавучести. Благодаря низкой теплопроводности слой подкожного жира помогает сохранить тепло, что позволяет, например, многим животным обитать в условиях холодного климата.
5) Смазывающая и водоотталкивающая. Воск покрывает кожу, шерсть, перья, делает их более эластичными и предохраняет от влаги. Восковой налет имеют листья и плоды многих растений. Такой слой защищает листья во время сильных дождей от намокания.
6) Регуляторная. Многие биологически активные вещества (половые гормоны - тестостерон у
мужчин и прогестерон у женщин), витамины (A, D, E) являются соединениями липидной
природы.
7) Источник метаболической воды. Одним из продуктов окисления жира является вода, которая
очень важна для некоторых обитателей животного мира пустынь, например, для верблюдов.
Жир, который запасают эти животные в горбах, является источником воды. Окисление 100 г
жира дает примерно 105 г воды. Необходимую для жизнедеятельности воду медведи, сурки и
другие животные, впадающие в спячку, получают в результате окисления жира.
8) В миелиновых оболочках аксонов нервных клеток липиды являются изоляторами при проведении нервных импульсов.
9) Воск используется пчелами в строительстве сот.
Липиды могут образовывать комплексы с другими биологическими молекулами — белками и сахарами.
Белки, или протеины (от греч. protos – первый) – самые многочисленные, разнообразные и имеющие первостепенное значение органические соединения. Белки – макромолекулы, так как имеют большие размеры.
Химический состав молекул белка: углерод, кислород, водород, азот, сера, также могут быть фосфор, железо, цинк, медь.
Белки - это полимеры, состоящие из повторяющихся низкомолекулярных мономеров. Аминокислоты – мономеры белковых молекул. Известно около 200 аминокислот, встречающихся в живых организмах, но только 20 из них входят в состав белков. Это так называемые основные, или белокобразующие аминокислоты. 20 аминокислот обеспечивают многообразие белков. У растений все необходимые аминокислоты синтезируются из первичных продуктов фотосинтеза. Человек и животные не способны синтезировать ряд аминокислот и должны получать их в готовом виде вместе с пищей. Такие аминокислоты называются незаменимыми. К ним относятся лизин, валин, лейцин, изолейцин, треонин, фенилаланин, триптофан, метионин, аргинин и гистидин (всего 10).
Строение аминокислоты:
| Аминогруппа (–NH2 ) | Карбоксильная группа (-СООН) | Радикал (-R) |
| Основные свойства | Кислотные свойства | Различное строение у разных аминокислот |
Между аминогруппой одной аминокислоты и карбоксильной группой другой аминокислоты образуется ковалентная связь, которая называется пептидная связь, а молекула белка – полипептид.

В растворе аминокислоты могут выступать в роли как кислот, так и оснований, т. е. они являются амфотерными соединениями. Карбоксильная группа -СООН способна отдавать протон, функционируя как кислота, а аминная - NH2 — принимать протон, проявляя таким образом свойства основания.
Структура белков. Каждому белку в определенной среде свойственна особая пространственная структура. При характеристике пространственной (трехмерной) структуры выделяют четыре уровня организации молекул белков.
| лиэ—глу—тре—ала—ала—ала—лиз—фен—глу—арг—глн—гиc—мет—асп—сер— сер—тре—сер—ала—ала—сер—сер—сер—асн—тир—цис—асн—глу—мет—мет— лиз—сер—арг—асн—лей—тре—лиз—асп—арг—цис—лиз—про—вал—асн—тре— |
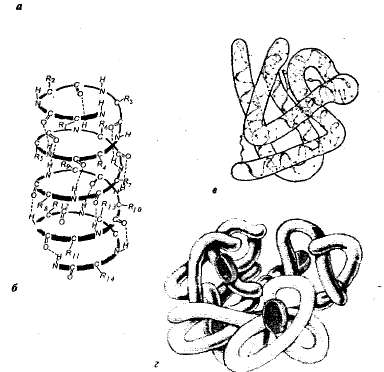
Уровни структурной организации белка: а — первичная структура — аминокислотная последовательность белка; б — вторичная структура — полипептидная цепь закручена в виде спирали; в — третичная структура белка ; г — четвертичная структура гемоглобина.
Место синтеза белков в клетке: на рибосомах.
Локализация белков в клетке и организме: присутствуют во всех органоидах и цитоплазматическом матриксе.
Пространственная структура белка:
Первичная структура белка – последовательность аминокислот, соединенных друг с другом пептидными связями в полипептидную цепь. От первичной структуры зависят все свойства и функции белков. Замена одной-единственной аминокислоты в составе молекул белка или нарушение порядка в их расположении обычно влечет за собой изменение функции белка.
Вторичная структура белковой молекулы достигается ее спирализацией: полипептидная цепь, состоящая из последовательно соединенных аминокислот, закручивается в спираль, образуются непрочные водородные связи между – СО- и – NН- группами.
При образовании третичной структуры спирализованная белковая молекула еще многократно сворачивается, образуя шарик – глобулу. Прочность третичной структуры определяется различными связями, например, дисульфидными связями (-S-S-), ионные, водородные, гидрофобное взаимодействие.
Четвертичная структура - это соединение, состоящее из нескольких молекул белка, имеющих третичную структуру. Химические связи - ионные, водородные, гидрофобное взаимодействие.
И так, первичная структура – это линейная структура, в виде полипептидной цепи; вторичная – спиральная, за счет водородных связей; третичная – глобулярная; четвертичная – объединение нескольких молекул белка с третичной структурой.
Свойство белка – денатурация - нарушение природной структуры белка, которая бывает обратимая, если не разрушена первичная структура, и необратимая, если первичная структура разрушена.
Воздействие факторов среды
(температура, химические вещества, излучение и др.)
 |
Денатурация белка (разрушение структур)
Ренатурация – полное восстановление структуры белка.
Под влиянием различных химических и физических факторов (обработка спиртом, ацетоном, кислотами, щелочами, высокой температурой, облучением, высоким давлением и т. д.) происходит изменение вторичной, третичной и четвертичной структур белка вследствие разрыва водородных и ионных связей. Процесс нарушения естественной структуры белка называется денатурацией. При этом наблюдается уменьшение растворимости белка, изменение формы и размеров молекул, потеря ферментативной активности и т. д. Процесс денатурации может быть полным или частичным. В некоторых случаях переход к нормальным условиям среды сопровождается самопроизвольным восстановлением естественной структуры белка. Такой процесс называется ренатурацией.
Простые и сложные белки. По химическому составу выделяют белки простые и сложные. К простым относятся белки, состоящие только из аминокислот, а к сложный — белки, содержащие белковую часть и небелковую - ионы металлов, остаток фосфорной кислоты, углеводы, липиды и др.
Функции белков:
1) Ферментативная, или каталитическая. Катализаторы – это вещества, ускоряющие химические реакции. Ферменты – это катализаторы биохимических реакций. Ферменты ускоряют реакции в организме в десятки и сотни тысяч раз. Они высокоспецифичны, так как каждый фермент катализирует только определенную реакцию.
Ферменты = Биокатализаторы (ускорители химических реакций, протекающих в клетках)
2) Структурная. Белки входят в состав всех мембран и органоидов клетки (например, в соединении с РНК белок образует рибосомы).
3) Энергетическая. При распаде 1 г белков до конечных продуктов (СО2, Н2О и азотсодержащие вещества) выделяется 17,6 кДж.
4) Запасающая. Эту функцию выполняют белки – источники питания (белок яйца – альбумин,
белок молока – казеин, клетки эндосперма и яйцеклетки).
5) Защитная. Все живые клетки и организмы имеют защитные системы. У человека и животных - это иммунная защита. В лимфоцитах образуются антитела – защитные белки, которые обезвреживают чужеродные тела. Другой пример защитной функции – свертывание белка фибриногена в крови, что приводит к образованию сгустка крови – тромба, который закупоривает сосуд, кровотечение прекращается. Механическую защиту обеспечивают роговые образования – волосы, рога, копыта. В состав этих образований входят белки. Растения тоже образуют защитные белки, например, алкалоиды, благодаря которым покровы растений становятся более прочными и устойчивыми.
6) Регуляторная. Многие белки – гормоны, регулирующие физиологические процессы (белковую природу имеют инсулин и глюкагон). Клетки поджелудочной железы вырабатывают гормон инсулин, регулирующий содержание глюкозы в крови.
 Поджелудочная железа
Поджелудочная железа
 Гормон инсулин
Гормон инсулин
Глюкоза (в крови) à Гликоген (в клетках печени)
7) Транспортная. Функция транспортных белков заключается в присоединении химических элементов или биологически активных веществ и переносе их к тканям и органам.
Гемоглобин (находится в эритроцитах)
 |
Состояние гемоглобина
 |  |
Гемоглобин + кислород Гемоглобин + углекислый газ
8) Двигательная. Сократительные белки участвуют во всех видах движения, к которым способны клетки и организмы. Примеры: движение жгутиков и ресничек у простейших одноклеточных животных, сокращение мышц у многоклеточных животных (белки миозин и актин обеспечивают сокращение мышечных клеток), движение листьев у растений.
9) Сигнальная. Белки, встроенные в мембрану клетки, осуществляют прием сигналов из
внешней среды и передачу информации в клетку. Такие белковые молекулы способны
изменять свою третичную структуру в ответ на действия факторов внешней среды.
10) Токсическая (токсины, обеспечивающие защиту от врагов и умерщвление добычи).
| Функции белка | Характеристика |
| 1. Структурная | Белки входят в состав клеточных мембран и органоидов |
| 2. Энергетическая | При окислении 1 г белков выделяется 17,6 кДж |
| 3. Запасающая | Белки – запасной питательный и энергетический материал |
| 4. Каталитическая, ферментативная | Белки – ферменты, ускоряющие химические реакции |
| 5. Регуляторная | Многие белки – гормоны, регулирующие физиологические процессы |
| 6. Транспортная | Перенос различных веществ (гемоглобин + кислород) |
| 7. Двигательная | Сократительные белки обеспечивают движение (хромосомы к полюсам клетки) |
| 8. Защитная | Защищают организм от чужеродных тел |
| 9. Сигнальная | Осуществляют прием сигналов из внешней среды и передачу информации в клетку |
| 10. Токсическая | Токсины обеспечивают защиту от врагов и умерщвление добычи |
Белки используются как источник энергии редко, поскольку они выполняют ряд других важных функций. Белки обычно используются, когда истощаются такие источники, как углеводы и жиры. Углеводы и жиры откладываются в запас; когда в пище не хватает какого-либо органического соединения, возможно превращение в организме одних органических соединений в другие: белков в жиры и углеводы, углеводы и жиры друг в друга. Но углеводы и жиры не могут превращаться в белки.

 БЕЛКИ
БЕЛКИ

 УГЛЕВОДЫ ЖИРЫ
УГЛЕВОДЫ ЖИРЫ
Аминокислоты, которые образуются при расщеплении белковых молекул, необходимы для построения новых белков. Недостаток белков в пище является невосполнимым, так как они образуются только из аминокислот. Поэтому белковое голодание опасно для организма.