По общей жесткости
- очень мягкие < 1,5
- мягкие 1,5 – 3,0
- умеренно жесткие 3,0 – 6,0
- жесткие 6,0 – 9,0
- очень жесткие > 9,0
Химический состав воды выражают формулой Курлова М.Г. Это псевдодробь, в числителе которой расположены анионы в % в убывающем порядке, в знаменателе – катионы в том же порядке. Ионы содержащиеся в количестве менее 10% в формулу не включаются. Слева от дроби указывается общая минерализация в г/л с округлением до первого десятичного знака, справа температура воды в ゚С и pH.
Используя данные химического анализа, запишите формулу Курлова, определите вид жесткости и дайте наименование воды.
Данные химического анализа воды
| Сухой остаток, мг/л | pH | Температура, °С | Содержание основных ионов, мг/л | |||||
| HCO-3 | SO2-4 | Cl- | Na+ | Ca2+ | Mg2+ | |||
| 7,3 |
Для начала необходимо сделать пересчет основных ионов в мг-экв. /л и %-экв./л с делением на анионы и катионы
Для пересчета ионов из мг/л в мг.экв./л нужно перемножить мг/л на переводные коэффициенты
| Ионы | HCO-3 | SO2-4 | Cl- | Na+ | Ca2+ | Mg2+ |
| коэффициенты | 0,0164 | 0,0208 | 0,0282 | 0,0435 | 0,0499 | 0,0822 |
Чтобы перевести мг.экв/л в %-экв/л необходимо учесть, что суммарное содержание анионов и суммарное содержание катионов равно 100%. Составляя простую пропорцию получаем процентное содержание каждого иона.
| анионы | содержание | катионы | содержание | ||||
| мг/л | мг-экв/л | %-экв/л | мг/л | мг-экв/л | %-экв/л | ||
| HCO-3 | 15,25 | Na+ | 4,05 | ||||
| SO2-4 | 1,58 | Ca2+ | 9,68 | ||||
| Cl- | 0,68 | Mg2+ | 3,70 | ||||
| Итого | 17,51 | Итого | 17,43 |
Общая жесткость определяется как суммарное содержание катионов кальция и магния в мг-экв/л.
9,68 + 3,70 = 13,38 по этому показателю данная вода классифицируется как очень жесткая.
Формула Курлова для данной воды будет выглядеть следующим образом:
М1,0 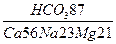 t°12 pH 7,3
t°12 pH 7,3
Учитывая общую минерализацию, химический состав, pH, t и жесткость дают наименование воде. Формула Курлова читается слева на право: