рефераты конспекты курсовые дипломные лекции шпоры
- Раздел Энергетика
- /
- А. ОРИЕНТАЦИОННАЯ СОСТАВЛЯЮЩАЯ ИЛИ ДИПОЛЬ-ДИПОЛЬНОЕ ВЗАИМОДЕЙСТВИЕ – электростатическое взаимодействие полярных молекул при сближении (рис.а
Реферат Курсовая Конспект
А. ОРИЕНТАЦИОННАЯ СОСТАВЛЯЮЩАЯ ИЛИ ДИПОЛЬ-ДИПОЛЬНОЕ ВЗАИМОДЕЙСТВИЕ – электростатическое взаимодействие полярных молекул при сближении (рис.а
А. ОРИЕНТАЦИОННАЯ СОСТАВЛЯЮЩАЯ ИЛИ ДИПОЛЬ-ДИПОЛЬНОЕ ВЗАИМОДЕЙСТВИЕ – электростатическое взаимодействие полярных молекул при сближении (рис.а - раздел Энергетика, ...


Силы Ван-дер-Ваальса (голланд.ученый, 1873 г.) – силы межмолекулярного взаимодействия (взаимодействия между молекулами), проявляющиеся на расстояниях, превосходящих размеры частиц.

а. ОРИЕНТАЦИОННАЯ СОСТАВЛЯЮЩАЯ ИЛИ ДИПОЛЬ-ДИПОЛЬНОЕ ВЗАИМОДЕЙСТВИЕ – электростатическое взаимодействие полярных молекул при сближении (рис.а)
Еор увеличивается с увеличением mмол и уменьшением расстояния между молекулами.
|
 |
Чем выше температура, тем Еор –меньше.
c. дисперсионная составляющая(эффект Лондона)
-электростатическое взаимодействие мгновенных диполей, возникающих за счет флуктуации электрической плотности между неполярными молекулами (рис.с). В результате согласованного (синхронного) движения мгновенных диполей энергия системы понижается.
Едис – энергия взаимодействия мгновенных диполей пропорциональна поляризуемости молекул и обратно пропорциональна расстоянию между центрами частиц.
Для неполярных молекул - дисперсионная –единственная из составляющих вандерваальсовых сил.
В системе, состоящей из:
◄ полярных молекул:
åЕв = Еор + Еинд + Едис
◄ полярных и неполярных молекул:
åЕв = Еинд + Едис
◄ неполярных молекул:
åЕв = Едис
| вещество | mдиполя | Поляризуемость, М3×1030 | Энергия взаимодействия, кДж/моль | Ткип,К | |||
| ориентационная | Индукционная | Дисперсионная | Суммарная | ||||
| H2 Ar Xe HCl HBr HI NH3 | 1,03 0,78 0,38 1,52 | 0,8 1,64 4,16 2,64 3,62 5,42 2,23 | 3,3 1,1 0,6 13,3 | 1,0 0,70 0,3 1,5 | 0,17 8,5 18,4 16,8 28,5 60,6 14,7 | 0,17 8,5 18,4 21,1 30,3 61,5 29,5 | 20,2 239,6 |
Aring;Ев – на 1-2 порядка ниже Е хим.св.→ Таблица.
С увеличением размера молекул в ряду Аr – Хе и НСl – НI растет их поляризуемость и Едис →Таблица.
Еор вносит значительный вклад в åЕв для молекул с большим mдип. → Таблица.
С увеличением åЕв возрастет Ткип жидкостей, а также теплота их парообразования. → Таблица.

|
 |  |
М е ж м о л е к у л я р н а я внутримолекулярная
Межмолекулярная Н-связь
А – Н + В – R ® А – Н….В – R
водород способен глубоко внедряться в электронную оболочку соседнего отрицательно поляризованного атома.
Атомы А и В могут быть одинаковыми
Нd+-Fd- + Нd+-Fd- ® H-F….H-F
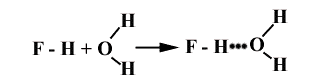 |
могут быть разными
Внутримолекулярная Н-связь
► Энергия водородной связи ЕН-свимеет промежуточное значение между энергией ковалентной связи Е хим.св.и…ДОНОРНО – АКЦЕПТОРНОЕ ВЗАИМОДЕЙСТВИЕ
МЕЖДУ МОЛЕКУЛАМИ
Осуществляется, если одна из молекул имеет атом со свободными орбиталями, а другая – атом с внешней парой неподеленных электронов.
Пример:
Между различными молекулами
:NH3 + BF3 = NH3.BF3
Суммарная валентность азота равна 4 и бора равна 4.
Между одинаковыми молекулами
AlCl3 + AlCl3 = Al2Cl6

ВЫВОД: Таким образом между молекулами существуют неспецифические (силы Ван дер Вальса) и специфические (водородные связи, донорно-акцепторные) взаимодействия.
– Конец работы –
Используемые теги: ОРИЕНТАЦИОННАЯ, составляющая, ДИПОЛЬ-ДИПОЛЬНОЕ, взаимодействие, электростатическое, взаимодействие, полярных, молекул, сближении, рис0.136
Если Вам нужно дополнительный материал на эту тему, или Вы не нашли то, что искали, рекомендуем воспользоваться поиском по нашей базе работ: А. ОРИЕНТАЦИОННАЯ СОСТАВЛЯЮЩАЯ ИЛИ ДИПОЛЬ-ДИПОЛЬНОЕ ВЗАИМОДЕЙСТВИЕ – электростатическое взаимодействие полярных молекул при сближении (рис.а
Что будем делать с полученным материалом:
Если этот материал оказался полезным для Вас, Вы можете сохранить его на свою страничку в социальных сетях:
| Твитнуть |
Хотите получать на электронную почту самые свежие новости?







Новости и инфо для студентов