Характеристика и классификация природных вод
СТОЧНЫЕ ВОДЫ ТЭС И АЭС И МЕТОДЫ ИХ ОЧИСТКИ
Характеристика и классификация природных вод
Во многих теплоэнергетических процессах большую роль играет вода. Она используется на электростанциях как теплоноситель, растворитель, энергоноситель (например, для транспорта золы и шлака) и др.
Природная вода формируется под воздействием естественных природных процессов. Качественные и количественные показатели ее соответствуют естественным параметрам среднемноголетнего уровня. В зависимости от содержания солей природные воды подразделяются на:
– пресные, с содержанием солей менее 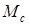 < 1 г/л;
< 1 г/л;
– солоноватые, при 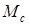 = 1…10 г/л;
= 1…10 г/л;
– соленые, при 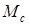 = 10…50 г/л;
= 10…50 г/л;
– рассолы, при 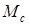 > 50 г/л.
> 50 г/л.
Пресные воды, в свою очередь могут иметь: малую минерализацию при 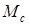 < 200 мг/л; среднюю –
< 200 мг/л; среднюю – 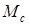 = 200…500 мг/л и повышенную –
= 200…500 мг/л и повышенную – 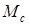 =500…1000 мг/л.
=500…1000 мг/л.
По преобладающему аниону все воды делятся на гидрокарбонатные, сульфатные и хлоридные. Жесткость природной воды определяется наличием в ней солей кальция и магния. Общая жесткость воды обусловливается карбонатной и некарбонатной жесткостью. Карбонатная жесткость связывается с присутствием в воде гидрокарбонатов (бикарбонатов) кальция СаНСО3 и магния МgНСО3, а некарбонатная определяется наличием сульфатов, хлоридов, нитратов кальция и магния СаSO4, MgSO4, CaCl2, MgCl2, CaNO3, MgNO3.
Физические характеристики чистой воды представлены в табл.11.1 [6]. С увеличением температуры плотность, вязкость, теплоемкость и поверхностное натяжение воды уменьшаются.
Таблица 11.1