рефераты конспекты курсовые дипломные лекции шпоры
- Раздел Энергетика
- /
- Электронные плотности в поле сил химической связи и между сближенными на то же расстояние несвязанными атомами, заметно отличаются
Реферат Курсовая Конспект
Электронные плотности в поле сил химической связи и между сближенными на то же расстояние несвязанными атомами, заметно отличаются
Электронные плотности в поле сил химической связи и между сближенными на то же расстояние несвязанными атомами, заметно отличаются - раздел Энергетика, 1. Основы Физико-Химического Материаловедения 1.1. Химическая Связь ...
1. ОСНОВЫ ФИЗИКО-ХИМИЧЕСКОГО МАТЕРИАЛОВЕДЕНИЯ
1.1. Химическая связь и строение твёрдых тел
При сближении атомов может произойти перекрытие их электронных оболочек. Возникающие при этом электростатические взаимодействия приводят к возникновению химических связей между атомами, и образованию многоатомных соединений (молекул, ионов, радикалов). Химическая связь возможна если:
1. Полная энергия многоатомной системы меньше, чем сумма энергий несвязанных атомов, из которых она образована.
2. Электронные плотности в поле сил химической связи и между сближенными на то же расстояние несвязанными атомами, заметно отличаются.
При образовании связи валентные электроны распределяются так, что силы притяжения и отталкивания между атомами уравновешиваются. Это равновесное расстояние между атомами соответствует длине химической связи.
Согласно классической теории валентности различают: ионную, ковалентную, металлическую и молекулярную (Ван-дер-Ваальсову) связи. Это объясняет разнообразие свойств веществ. Простой количественной характеристики химической связи нет. Так, Есв (энергия разделения твёрдого тела на атомы или молекулы) позволяет выделить только неимение прочную молекулярную связь (Есв »10 кДж/моль). Остальные типы связи по Есв практически не различимы (для всех Есв= 400¸1000 кДж/моль). Например, ионный NaCl имеет Есв= 650; ковалентный алмаз – 700; металлический Fe – 400 кДж/моль. Т.е. этот признак нельзя класть в основу классификации веществ.
Классический и квантово-механический подходы к объяснению типа химической связи объединяются, если положить в основу такой классификации пространственное распределение электронов т.е. то, как атомы делят между собой валентные электроны. Пространственное распределение электронов в кристаллах с различным типом химической связи на рис.1.1 (тёмные участки - области локализации валентных электронов).
а) модель ионного кристалла. Все валентные электроны находятся в 8-ми электронной оболочке аниона, что исключает их перемещение. Это диэлектрики. Образование такой связи возможно между атомами с различной электроотрицательностью. По мере уменьшения электроотрицательности происходит переход к ионно-ковалентным кристаллам (CdS) (возле Cd2+ имеется небольшая плотность ионов). KCl®AllBlV®Alll BV ®
б) чисто ковалентная связь – равномерное распределение электронов возле соседних атомов. Устойчивая 8-ми электронная оболочка образуется за счёт спарившихся электронов соседних атомов. Электронная плотность в направлении связи достаточно велика, т.е. наблюдается частичная коллективизация электронов, что ухудшает электрические свойства. Поэтому ковалентные кристаллы даже с долей ионной связи являются полупроводниками. Для них характерна прочность, твердость и 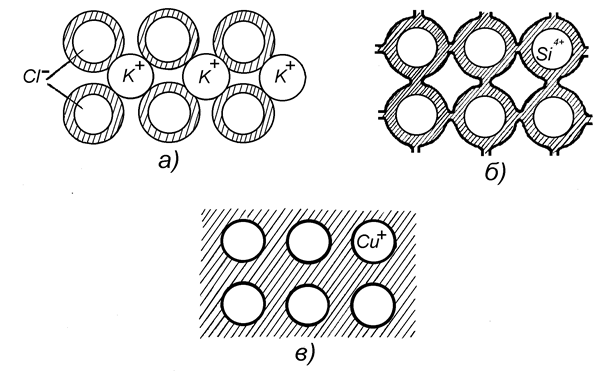 низкая пластичность. Переход от ковалентной к металлической связи Si®Ge®Pb;
низкая пластичность. Переход от ковалентной к металлической связи Si®Ge®Pb;
Рис.1.1. Распределение валентных электронов в химических связях
в) прочность металлической связи (полная коллективизация электронов) обусловлена притяжением положительных атомных остовов к свободным электронам. Ковалентный кристалл не образуется из-за малого количества валентных электронов. Большое число свободных электронов, ненаправленность валентных связей объясняют специфические свойства металлов – блеск, непрозрачность, прочность, пластичность, высокие электро- и теплопроводность. Обычно металлы кристаллизуются в структурах с плотной упаковкой атомов.
Все материалы могут находиться в трёх агрегатных состояниях: газовом, жидком, и твёрдом (4-е плазма). Критерием агрегатного состояния является соотношение средней потенциальной энергии взаимодействия атомов (молекул) в веществе к их кинетической энергии e (р,Т) = Евз/Екин.
Газ – агрегатное состояние вещества, в котором частицы слабо связаны и хаотически движутся, заполняя весь объём. Для них e (р,Т)<<1.
Жидкости сочетают свойства газов и твёрдых тел e (р,Т) »1. Тепловое движение молекул жидкости – сочетание малых колебаний около положения равновесия и перескоков из одного положения равновесия в другое, чем обусловлена текучесть. Жидкости не обладают упругостью формы и практически несжимаемы.
Твёрдое тело характеризуется стабильностью формы, т.к. атомы совершают лишь малые тепловые колебания возле фиксируемых положений равновесия e (р,Т) >>1. Это система сильно взаимодействующих частиц, пространственное упорядочение которых во многом определяет физические свойства вещества.
Кристаллы – твёрдые тела с 3-хмерной периодической атомной структурой (кристаллической решёткой), имеющие при равновесных условиях образования форму правильных симметричных многогранников. Если для жидкостей и некристаллических твёрдых тел характерен ближний порядок в расположении соседних частиц, то кристаллы имеют дальний порядок, т.е. строгую повторяемость во всех направлениях одного и того же структурного элемента.
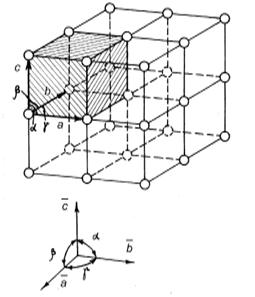
Строение кристаллов характеризуется элементарной ячейкой – минимальным объёмом кристаллической решётки, путём трансляции (параллельного переноса) которой можно построить всю решётку. Рёбра элементарных ячеек обозначаются a, b и c и называют периодами кристаллической решётки или векторами трансляций. Углы между ними обозначаются a, b и g (рис.1.2). Каждая атомная плоскость кристаллической решётки, пересекаясь с осями координат, построенных на векторах  , отсекает на них отрезки соответствующие целым числам периодов. Обратные им числа h k l называют кристаллографическими индексами или индексами Миллера. Грани кристалла имеют индексы (100), (010), (001).
, отсекает на них отрезки соответствующие целым числам периодов. Обратные им числа h k l называют кристаллографическими индексами или индексами Миллера. Грани кристалла имеют индексы (100), (010), (001).
 |
 По признакам симметрии элементарной ячейки все кристаллы группируются в 7 сингоний, которые отличаются соотношениями периодов решётки и углами между векторами элементарных трансляций.
По признакам симметрии элементарной ячейки все кристаллы группируются в 7 сингоний, которые отличаются соотношениями периодов решётки и углами между векторами элементарных трансляций.
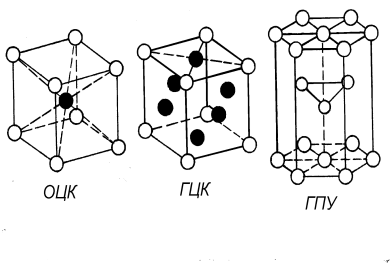 |
Рис.1.2. Элементарная ячейка Рис.1.3. Структуры металлов и сплавов
Каждая сингония включает несколько пространственных групп симметрии (их всего 230, систематизированы Е.С.Фёдоровым). Структура всех известных кристаллов соответствует какой-либо из этих групп.
Большинство металлов кристаллизуется в высокосимметричных решётках с плотной упаковкой атомов: кубических объемно центрированной (ОЦК) и гранецентрированной (ГЦК) и гексагональной плотной упаковке (ГПУ) (см. рис.1.3). ОЦК решётку имеют: Pb, K, Na, W, V, Cr, Feα и др.; ГЦК: Ni, Cu, Ag, Au, Pt, Fe и др.; ГПУ – Mg, Cd, Be, Zn и др. Периоды решётки a, b, c для большинства металлов 0,1 – 0,7 нм. Наибольшей плотностью упаковки обладает ГЦК и ГПУ (с/а = 1,633) решётки (~74%).
Даже наиболее симметричные ГЦК и ОЦК решётки обладают анизотропией, неоднородностью физических свойств в разных кристаллографических направлениях. Это связано с тем, что плотность атомов по различным плоскостям неодинакова, например в плоскости (100) ОЦК-решетки ¼*4 = 1 атом; (110) – 2, в ГЦК наибольшая плотность в плоскости (111) (рис.1.4). Кубические кристаллы изотропные по отношению к прохождению света, электро- и теплопроводности, но анизотропные в отношении к упругим, электрооптическим, пьезоэлектрическим свойствам. Наибольшая степень анизотропии характерна для кристаллов низких сингоний.
 |
(100) (110) (111)
Рис.1.4. Основные кристаллографические плоскости кубической решетки
Некоторые кристаллические фазы являются метастабильными (относительно устойчивыми). Полиморфизм – свойство веществ находиться в нескольких кристаллических модификациях с различной структурой. Feα (ОЦК) и Feγ (ГЦК); Соα (ГЦК) и Соβ (ГПУ) и др. Изоморфизм – свойство различных, но родственных по химическому составу веществ кристаллизуется в одинаковых структурах при одинаковом типе химической связи.
Большинство твёрдых металлов являются поликристаллическими, т.е. состоят из множества ориентирных хаотично мелких кристаллов (кристаллитов). Крупные одиночные кристаллы называются монокристаллами. Поликристаллы являются псевдоизотропными. Если есть преимущественная ориентация (текстура), возникает анизотропия.
Некристаллические твёрдые материалы характеризуются отсутствием дальнего порядка в расположении атомов, ионов, молекул. Среди них выделяют стеклообразные вещества, в которых при нагревании наблюдается обратимый переход из твёрдого в высокоэластичное состояние. Стеклообразные вещества метастабильны, при внесении в их расплав центров кристаллизации можно сформировать кристаллическую фазу.
Аморфные вещества образуются при очень быстром охлаждении расплава или в плёнках, осажденных на холодную подложку. Состояние квазистабильно и при нагреве переходит в кристаллическое. Многие аморфные металлические сплавы (например, железа) обладают комплексом ценных для практического использования свойств и находят все большее применение в технике.
1.2. Дефекты кристаллической решётки. Их влияние на свойства материалов
Дефектами называют нарушения совершенной решётки идеального кристалла. Классификация структурных дефектов проводится по их пространственной протяжённости. Различают: точечные (нульмерные), линейные (одномерные), поверхностные (2-х мерные) и объёмные (3-х мерные) дефекты.
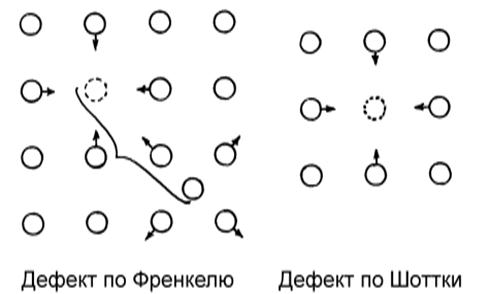 |
Точечные дефекты имеют атомарные размеры, поэтому их называют атомными. К ним относятся: дефекты по Френкелю, представляющие собой комплекс вакансия (отсутствие атома в узле) – междуузельный атом и дефекты по Шоттки – вакансия (рис.1.5). Первые образуются, когда атом уходит из своего узла в междуузлие, вторые, когда он оставляет вакансию и выходит на поверхность. Точечные дефекты принципиально отличаются от всех других тем, что они находятся в тепловом равновесии с решёткой.
Рис.1.5. Структура точечных дефектов
Их концентрация определяется выражениями:
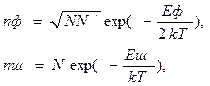
где N и N’ – концентрации атомов и междуузлий, соответственно; Еф, Еш – энергии образования дефектов. Видимо, что при любой температуре>0K имеется определённая равновесная концентрация этих дефектов. Поэтому эти неупорядоченности структуры называются собственными или термическими. С ростом температуры nф и nш растёт и при Т ≈ Тпл могут составлять ~1% от числа атомов. Точечные дефекты влияют на электрические, магнитные свойства, массоперенос (диффузию).
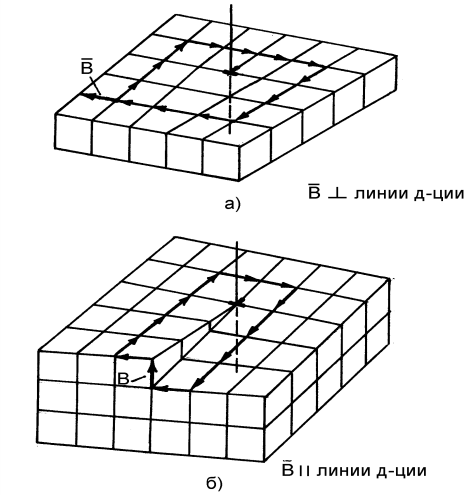 |
К линейным дефектам относятся краевые и винтовые дислокации. Под дислокацией понимают линию, отделявшую область кристалла, претерпевшую сдвиг от несдвинутой. Вектор Бюргерса
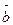 (рис.1.6) даёт величину и направление сдвига и является мерой дислокации. Различают полные
(рис.1.6) даёт величину и направление сдвига и является мерой дислокации. Различают полные  (
(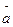 - период решётки) и частичные b<a дислокации. Дислокации возникают при механической нагрузке и входе роста кристалла, а не за счёт чисто теплового движения атомов в бездефектном материале.
- период решётки) и частичные b<a дислокации. Дислокации возникают при механической нагрузке и входе роста кристалла, а не за счёт чисто теплового движения атомов в бездефектном материале.
Рис.1.6. Краевая (а) и винтовая (б) дислокации
Точечные и линейные дефекты взаимодействуют между собой. Скопление вакансий может приводить к появлению дислокации, а при аннигиляции дислокаций разного знака могут возникнуть вакансии или микрокаверны. Дислокации могут двигаться вдоль плоскостей скольжения и перпендикулярно к ним, что повышает способность материала пластически деформироваться.
Дислокации являются геттерами (накопителями) других дефектов и примесных атомов. Они влияют на прочность и пластичность, электрические, магнитные и оптические свойства, определяют характер роста кристаллов.
К поверхностным дефектам относятся границы зёрен, дефекты упаковки и двойники. Границами зёрен разделяются участки кристалла с разной ориентацией. Различают малоугловые (разориентация от минут до 10 градусов) границы, состоящие из дислокаций и многоугловые (более 10 градусов), когда на границе образуется жидкообразный слой. Дефекты упаковки (нарушение порядка следования слоёв при построении структуры) наблюдаются преимущественно в металлических слоистых решётках с плотной упаковкой атомов.
Двойники, возникающие при росте (двойники роста) или при механическом воздействии (механическое двойникование), представляет собой зеркальное отражение участка кристалла в двойниковой плоскости (рис.1.7).
 |
К объёмным дефектам относятся микротрещины, микрокаверны, поры, инородные включения, скопление точечных дефектов (кластеры).
Рис.1.7. Структура двойника
К структурно нечувствительным относятся: плотность и модуль упругости (определяется силами межатомных взаимодействий), тепловые свойства (Тпл, al, l и др.), магнитные свойства диа- и парамагнетиков, ядерные и некоторые оптические свойства.
Структурно-чувствительными являются: сопротивление разрушению, пластичность, r полупроводников и металлов, магнитные свойства ферро- и ферримагнетиков, коэффициенты поглощения и пропускания и др..
Что касается прочности свойств реальных металлов и сплавов, то они значительно меньше теоретических значений, рассчитанных по силам межатомных взаимодействий. Например, для монокристалла Fe теоретическое сопротивление сдвигу 2300 МПа, а экспериментально измеренное – 40 МПа. Для Al фактическое сопротивление сдвигу в 500 раз меньше расчётного. Лишь в бездислокационных нитевидных монокристаллах (усах) достигнуты физические (ρ, μ) и механические (δВ, ε) свойства, приближающиеся к нижнему пределу теоретических значений.
Относительно невысокое значение скалывающих напряжений связано с тем, что процесс пластической деформации в реальных кристаллах развивается не одновременно по всему объёму, а последовательно посредством перемещения дислокаций. Для этого требуются значительно меньше напряжения, поскольку через критическое положение в этом случае перемещается только один атом. Как видно из рис.1.8 движение дислокаций поперёк кристалла соответствует относительному смещению двух его частей на одно межатомное расстояние. Винтовые дислокации так же способны двигаться под действием внешних сил.

Рис.1.8. Участие дислокации в пластической деформации кристалла
Значительное снижение прочности вызывается наличием внутренних и поверхностных трещин, раковин, границ и двойников. При нагрузке в области этих дефектов возникают пики напряжений, что приводит к местному преодолению связей, т.е. зарождению разрушения или деформации.
Для повышения прочности материала, кроме выращивания бездефектных монокристаллов, применяется легирование, термо- и механотермическая обработки. Это даёт возможность ограничить движение дислокаций, увеличивая число дефектов, т.е. заставляя более эффективно работать атомные связи. Зависимость σВ (предела прочности) от числа дефектов структуры изображена на рис.1.9, где І – теоретическая σВ и прочность нитевидных бездефектных монокристаллов (усов); ІІ – чистые неупрочненные металлы; ІІІ – упрочненные легированием и термообработкой металлы.
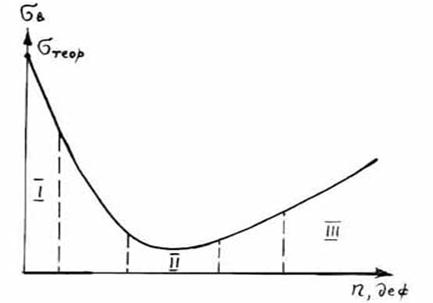
Рис.1.9. Влияние дефектов на прочностные свойства материалов
Методы исследования структуры и состава
Микроскопические методы, в основу которых положены законы геометрической оптики, заключаются в непосредственном наблюдении структуры поверхности или… Исследование поверхности специально изготовленных (шлифование, полирование и… Разрешающая способность оптических методов сравнима с длиной волны излучения. Для видимого света она не превышает 0,2…Основные свойства материалов
Классификация свойств
Электронная промышленность использует самую широкую номенклатуру материалов от конструкторских (металлических и неметаллических) до материалов с особыми физическими свойствами (сверхчистых, особо прочных, сверхпроводящих, функциональных и др.). От правильности выбора материала для конкретного применения во многом зависят характеристики изделия. Чтобы облегчить решение такой многопараметрической задачи, как выбор материала, вводиться классификация свойств, учитывающая конструкторско-технологическую специфику (рис.1.13).
В соответствии с этой классификацией все свойства и характеристики разделяют на физико-химические и потребительские. Физико-химические свойства в свою очередь делят на функциональные (служебные) и технологические (способность к обработке).
Функциональные свойства определяют пригодность материала для создания изделий высокого качества, работающих на определенном принципе действия. В зависимости от принципа действия изделия и его назначения набор функциональных свойств может быть различным, но основными являются электрические, механические, теплофизические, оптические, магнитные, химические свойства.


 Свойства материалов
Свойства материалов




 Физико-химическиеПотребительские
Физико-химическиеПотребительские




 Функциональные Технологические экономические
Функциональные Технологические экономические
 экологические
экологические


 электрические обрабатываемость: гигиенические
электрические обрабатываемость: гигиенические


 механические резанием, давлением эстетические
механические резанием, давлением эстетические

 теплофизические литьем и др.
теплофизические литьем и др.

 химические свариваемость
химические свариваемость

 оптические паяемость
оптические паяемость

 магнитные адгезионная способность
магнитные адгезионная способность
Рис.1.13. Классификация свойств материалов
Свойства, характеризующие поведение материала при его обработке, называются технологическими. В зависимости от методов обработки (механическая, термическая, электрофизикохимическая и др.) большое значение могут приобретать функциональные свойства (твёрдость, пластичность, теплостойкость, способность образовывать покрытия, теплопроводность и др.). Если комплекс этих свойств благоприятен для обработки материала (не требуется слишком высоких температур и давлений, вакуума, дорогих инструментальных и вспомогательных материалов), а технико-экономические показатели его обработки достаточно высоки – материал технологичен.
Деление свойств и характеристик на функциональные и технологические во многом условно. Так, Тпл (размягчения) может определить верхнюю границу рабочих температур изделия, т.е. быть функциональной характеристикой, так и быть показателем обрабатываемости материала, особенно термическим методами.
Потребительские свойства и характеристики материалов, как правило, вытекают из физико-химических и технологических и являются их следствием. Малотехнологичный материал непременно будет и дорогим экологически вредным.
Механические свойства материалов
Механические свойства, определяемые при статических испытаниях. Статическими называются испытания, при которых прилагаемая нагрузка постоянна или… Модуль Юнга определяет жёсткость материала, т.е. сопротивляемость упругой… При чистом сдвиге (по двум взаимно перпендикулярным площадкам действуют только касательные напряжения): τ = G…Механические свойства, определяемые при динамических и циклических испытаниях
По образцу прямоугольного сечения, имеющему царапину, U или V-образный надрез в перпендикулярном его длине направлении, наносится удар маятником.… Рис.1.16. Испытания на ударную вязкость (а), форма образца (б)Длительная прочность и триботехнические характеристики
Материалов
Рис.1.21. Зависимость предела длительной прочности от времени нагружения Предел длинной прочности – максимальное напряжение, не вызывающее разрушения материала при заданной температуре за…Сопротивление материалов коррозии и теплофизические свойства
Для оценки сопротивления материалов коррозии используют такие параметры как фронт коррозии; скорость коррозии (продвижение ее фронта); техническая… Виды коррозииЭлектрофизические свойства материалов
В нормальном состоянии электроны могут иметь только определённые значения энергии, т.е. занимать разрешённые энергетические уровни. Эти уровни… Электрическое сопротивление постоянному току, приводящие к переходу…Магнитные свойства материалов
Характеристикой намагничивания материалов является намагниченность, равная сумме магнитных моментов атомов единице объёма: (для однородного… В зависимости от знака и величины χ материалы делятся на диамагнетики,… Диамагнетизм – свойство материалов намагничиваться во внешнем магнитном поле в направлении противоположном полю.…Технологические свойства материалов
Обрабатываемость резанием характеризуют: качеством обработки (шероховатостью обработанной поверхности и точностью размеров); стойкостью инструмента;… Обрабатываемость давлением определяют при технологических испытаниях… Обрабатываемость давлением порошковых материалов характеризуют их текучестью, уплотняемостью и формуемостью. От…Кристаллизация материалов
Движущая сила кристаллизации и зародышеобразование
Рис.1.28. К понятию перенагрева и движущей силы процесса кристаллизации Температура Т, при которой F для жидкого и твердого состояния одинаковы называется равновесной температурой…Неравновесная и вторичная кристаллизации
В реальных условиях охлаждения это невозможно – состав в пределах каждого кристалла и различных кристаллов будет неодинаковым. Рассмотрим (рис.1.33)… В основе вторичной кристаллизации (новая кристаллическая фаза образуется из… разования и роста центров кристаллизации. Различают нормальный и мартенситный механизмы роста. Первый наблюдается при…ВВЕДЕНИЕ В ТЕОРИЮ СПЛАВОВ
Фазы сплавов
Жидкий раствор – однородная смесь двух и более компонентов, которые равномерно распределены в виде отдельных атомов, ионов или молекул. Твердым раствором называют фазу, состоящую из двух и более компонентов, один… Твердые растворы внедрения образуют переходные металлы с неметаллическими элементами, имеющими атомы малого R (главное…Диаграмма состояния сплавов с неограниченной растворимостью.
Правило отрезков (рычага)
Рис.1.30. Кривые охлаждения и диаграмма состояния сплавов с неограниченной… Для чистых металлов А и В, горизонтальный участок соответствует Ти обусловлен выделению скрытой теплоты…Диаграммы состояния сплавов с ограниченной растворимостью
Эвтектикой называют высокодисперсную механическую смесь нескольких твердых фаз, одновременно кристаллизирующихся при постоянной температуре… Рис.1.31. Диаграмма состояния сплавов с… эвтектическим превращениемДиаграммы состояния сплавов, образующих химические соединения с полиморфным и эвтектоидным превращением
Рис.1.32. Диаграмма состояния сплавов, компоненты которых образуют химическое соединение ется при перитектическом взаимодействии расплава Жс твердой фазой состава В: Ж+В. Эта фаза при температуре…Связь между структурой и свойствами сплавов
При образовании в сплавах химических соединений и эвтектик зависимость свойство-состав в месте сингулярной точки… а) б) Рис.1.34. Диаграмма состояния и зависимость свойство-состав в сплавах сДиаграммы состояния тройных сплавов
Рис. 1.35. Концентрационный треугольник Значение температур фазовых превращений откладывается по граням призмы, построенной на концентрационном треугольнике.…– Конец работы –
Используемые теги: Электронные, плотности, поле, сил, химической, связи, между, сближенными, расстояние, несвязанными, атомами, заметно, отличаются0.153
Если Вам нужно дополнительный материал на эту тему, или Вы не нашли то, что искали, рекомендуем воспользоваться поиском по нашей базе работ: Электронные плотности в поле сил химической связи и между сближенными на то же расстояние несвязанными атомами, заметно отличаются
Что будем делать с полученным материалом:
Если этот материал оказался полезным для Вас, Вы можете сохранить его на свою страничку в социальных сетях:
| Твитнуть |
Хотите получать на электронную почту самые свежие новости?







Новости и инфо для студентов