рефераты конспекты курсовые дипломные лекции шпоры
- Раздел Энергетика
- /
- Гидратация ионов
Реферат Курсовая Конспект
Гидратация ионов
Гидратация ионов - раздел Энергетика, Лекция №4. ТЕОРИЯ ЭЛЕКТРОЛИТИЧЕСКОЙ ДИССОЦИАЦИИ Ионы, Связанные С Молекулами Воды, Называются Гидратированными. В Растворах М...
Ионы, связанные с молекулами воды, называются гидратированными. В растворах могут содержаться только гидратированные ионы. Эти ионы могут содержать как постоянное, так и переменное количество воды.
К гидратам постоянного состава относится ион водорода, который может удерживать одну молекулу воды, такой ион называют ион гидроксония.
Н+Сl- + H2Oo → H3O+ + Cl-
ион
гидроксония
Механизм образования иона гидроксония – донорно-акцепторный. Протон водорода имеет свободную ячейку, а атом кислорода в молекуле воды – личную электронную пару, которую отдает в личное пользование с протоном водорода, то есть молекула воды – донор, протон – акцептор.
С точки зрения ТЭД кислоты – это электролиты, при диссоциации которых образуются катионы водорода и анионы кислотных остатков.
Основность кислоты – это величина, показывающая число катионов водорода, образующихся при диссоциации.
Основания – э то электролиты, при диссоциации которых образуются катионы металлов и анионы гидроксогрупп.
Кислотность оснований – это величина, показывающая, сколько гидроксид-ионов образуется при диссоциации.
Электролиты, которые при диссоциации одновременно образуют катионы водорода и гидроксид-ионы называются амфотерными или амфолитами.
Соли – это электролиты, при диссоциации которых образуются катионы металлов (а также, катионов аммония NH4+) и анионы кислотных остатков.
Все оксиды неэлектролиты.
С точки зрения ТЭД все уравнения делятся на:
1. молекулярные
2. краткие ионные
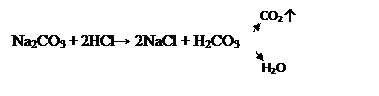 3. полные ионные.
3. полные ионные.
|
Пример:
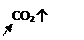 |
|

 (полное ионное уравнение)
(полное ионное уравнение)
|

|
|
|
Не расписывают на ионы слабые электролиты (малодиссоциируемые вещества), газы, осадки, оксиды. Чтобы перейти от полного к краткому ионному уравнению, надо вычеркнуть одинаковые ионы в левой и правой частях уравнения.
Признаки течения реакций до конца:
1. В результате реакции образуется осадок.↓
Пример:
 BaCl2 + H2SO4 → BaSO4↓ + 2HCl
BaCl2 + H2SO4 → BaSO4↓ + 2HCl
Ba2+ + 2Cl- + 2H+ + SO42- → BaSO4↓ + 2H+ + 2Cl-
Ba2+ + SO42 → BaSO4↓
2. Образуются газы.↑
3. Образуются малодиссоциируемые вещества.
4. Реакции, в результате которых образуются комплексные соединения.
– Конец работы –
Эта тема принадлежит разделу:
Лекция №4. ТЕОРИЯ ЭЛЕКТРОЛИТИЧЕСКОЙ ДИССОЦИАЦИИ
ТЕОРИЯ ЭЛЕКТРОЛИТИЧЕСКОЙ ДИССОЦИАЦИИ... План... Основные положения теории электролитической диссоциации...
Если Вам нужно дополнительный материал на эту тему, или Вы не нашли то, что искали, рекомендуем воспользоваться поиском по нашей базе работ: Гидратация ионов
Что будем делать с полученным материалом:
Если этот материал оказался полезным ля Вас, Вы можете сохранить его на свою страничку в социальных сетях:
| Твитнуть |
Хотите получать на электронную почту самые свежие новости?







Новости и инфо для студентов