Энтропия.
Это одно из наиболее сложных понятий термодинамики. Физический
смысл его мы рассмотрим в дальнейшем, а пока дадим математическоеопределение.
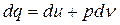
Рассмотрим частный случай идеального газа: 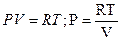
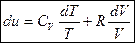 (4.12)
(4.12)
Формула (4.12) не является полным дифференциалом, поэтому умножим левую и правую часть на интегрирующий множитель (1/Т)
 (4.13)
(4.13)
(4.13) - полный дифференциал
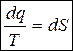 (4.14)
(4.14)
(4.14) - здесь вводится новый параметр - S. Клаузиус назвал его энтропией. В переводе это означает - «преобразование» (4.15)
Т.е. энтропия является функцией состояния, также как и внутренняя энергия.

Энтропия является аддитивной величиной (экстенсивной), т.е. ее можно складывать. Пример аддитивных величин: S,U,V,m и др.
Величины, которые нельзя складывать, называют неаддитивными (интенсивными)
Пример: Т, Р, ρ, v.
Формулу (4.13) проинтегрируем:
 если
если  , то
, то
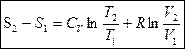 (4.16)
(4.16)
Формула (4.16) служит для вычисления изменения энтропии.
В координатах (T,S) площадь между кривой процесса и осью энтропии численно равна теплоте, поэтому такую диаграмму называют тепловой.
