Валентным электроном
Атомы щелочных металлов имеют один внешний электрон и заполненные внутренние оболочки. Этот внешний электрон движется в электрическом поле атомного остатка, т.е. ядра и заполненных электронных оболочек.
Если n (главное квантовое число) велико, то электрон движется далеко от атомного остатка и находится в центральном поле одного заряда (равного заряду +е). В этом случае спектральные термы атома подобны спектральным термам атома водорода.
Если же электрон подходит близко к атомному остатку, то он своим полем поляризует атомный остаток и движется в электрическом поле, образованном точечным зарядом и диполем.
Спектральные термы щелочных атомов выражаются формулой:
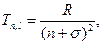
где R – постоянная Ридберга, n – главное квантовое число, σ – поправка, зависящая от орбитального квантового числа 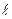 . Таким образом, у щелочных металлов энергия валентного электрона зависит не только от главного квантового числа, но и от орбитального квантового числа
. Таким образом, у щелочных металлов энергия валентного электрона зависит не только от главного квантового числа, но и от орбитального квантового числа 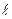 , поэтому при одном и том же n энергетические уровни для s, p, d, f и т.д. состояний валентного электрона будут различны.
, поэтому при одном и том же n энергетические уровни для s, p, d, f и т.д. состояний валентного электрона будут различны.
В ионах щелочных металлов реализуются не все возможные электронные переходы, а лишь разрешенные, которые удовлетворяют правилу отбора Δ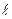 = ±1, где Δ
= ±1, где Δ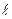 – разность значений орбитальных квантовых чисел, соответствующих двум состояниям валентного электрона.
– разность значений орбитальных квантовых чисел, соответствующих двум состояниям валентного электрона.
В спектрах испускания щелочных металлов наблюдается главная серия, которая возникает при переходах оптического, т.е. валентного, электрона из различных возбужденных p – состояний в основные, невозбужденные s – состояния. При переходе электрона в ближайшее s – состояние из p – состояния спектральная линия главной серии имеет максимальную интенсивность. Например, для Li эта линия соответствует переходу 2р → 2s. Для всех линий главной серии энергия переходов определяется выражением:
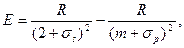
где m = 2, 3, 4, …
Здесь σs и σр - поправки, соответствующие конечному s и начальному р состояниям электрона (ридберговские поправки).
Кроме главной серии (наблюдаемой и при излучении, и при поглощении) наблюдаются также резкая, диффузная и основная серии. Резкая серия имеет резкие линии, диффузная – размытые.
Для натрия спектральные серии могут быть представлены переходами:
резкая серия 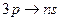 , n = 4, 5, …
, n = 4, 5, …
главная серия 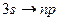 , n = 3, 4, …
, n = 3, 4, …
диффузная серия 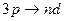 , n = 3, 4, …
, n = 3, 4, …
основная серия 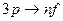 , n = 4, 5, …
, n = 4, 5, …
Исследования оптических спектров ионов щелочных металлов показали, что момент импульса атомного остатка равен нулю, т.е. момент импульса атома щелочного металла равен моменту его валентного электрона. При возбуждении атома щелочного металла и при испускании им света изменяется только состояние валентного электрона.