Системы и механизмы защиты организма от ксенобиотиков
Для сохранения гомеостаза биологические объекты в процессе эволюции выработали специальные системы и механизмы биохимической детоксикации. Механизмы защиты от воздействия ксенобиотиков у разных видов биологических объектов могут быть разными. Однако системы защиты организма одинаковы, и их классифицируют по назначению и механизмам действия.
По назначению выделяют:
- системы, служащие для ограничения токсического воздействия ксенобиотиков(барьеры, тканевые депо);
- системы, служащие для устранения токсического воздействия ксенобиотиков (транспортные и ферментные системы).
Механизмы действия систем защиты зависят от путей проникновения ксенобиотиков в организм.
Барьеры. В организме животных и человека имеется две системы барьерной защиты:
- барьеры, мешающие ксенобиотикам войти во внутреннюю среду организма;
- барьеры, защищающие особо важные органы (мозг, центральную нервную систему, железы внутренней секреции и др.).
Роль барьеров, защищающих внутреннюю среду организма, выполняют кожа и эпителий внутренней поверхности желудочно-кишечного тракта и дыхательных путей. Кожа животных и человека составляет более четверти массы тела (у среднестатистического человека до 20 кг). Кожный покров состоит из трех основных слоев: эпидермиса (верхнего слоя кожи), дермы (внутреннего слоя, или собственно кожи) и подкожной жировой клетчатки (рис. 9). Верхний слой кожи имеет сложную структуру и состоит из рогового, прозрачного, зернистого, шиповидного и зародышевого слоев. Функцию барьера выполняют глубинная часть рогового и прозрачного слоев. Основной структурный компонент барьеров – структурные белки. Роговое вещество образовано a-кератинами (от гр. keras рог), содержащими в молекуле остатки всех 20 природных аминокислот.
Прозрачный слой образован одно- и многослойными пластинами клеток. Каждая клетка окружена тончайшей жировой пленкой – липидной мембраной, непроницаемой для растворимых в воде веществ. Однако вещества, хорошо растворяющиеся в липидах, могут преодолевать такой барьер. Основной структурный компонент липидной мембраны – глицеролипидный.
Липиды (от гр. lipos жир) – жироподобные вещества, входящие в состав всех живых клеток. В соответствии с химическим строением различают три основные группы липидов:
- жирные кислоты и продукты их ферментативного окисления;
- глицеролипиды (содержат в молекуле остаток глицерина);
- липиды, не содержащие в молекуле остаток глицерина (кроме первых).
Способность кожных барьеров защищать внутреннюю среду организма от проникновения в него ксенобиотиков зависит от:
- природы ксенобиотиков (состава, химических свойств, реакционной способности, гидрофильности и т.п.) Гидрофильные вещества растворяются в водных растворах ткани, а жирорастворимые – в липидах. Кожные барьеры защищают внутреннюю среду организма от попадания в нее водорастворимых веществ, от воздействия водных растворов кислот, гидроксидов, солей. Однако органические растворители и вещества, растворяющиеся в них, проникают через эти барьеры. Особенно опасны вещества, обладающие дифильным характером.;
- размеров молекул (частиц) ксенобиотика определяют возможность их проникновения во внутреннюю среду организма через кожу и кожные протоки потовых и сальных желез. Основным путем при этом является впитывание через кожу. Большие молекулы (белковые) остаются на поверхности кожи, не проникая вглубь, а частицы с малыми размерами могут проникать внутрь.;
- возраста организма Проницаемость кожи для воды не меняется с возрастом.
В тех случаях, когда ксенобиотики проникают через роговой слой и липидные мембраны, эпителий внутренней поверхности желудочно-кишечного тракта и дыхательных путей и поступают в кроветок, функцию барьеров, защищающих особо важные органы, выполняют гистогематические барьеры (от гр. histos ткань + haima кровь), расположенные между тканью и кровью. Некоторые ксенобиотики могут повреждать клетки, образующие гистогематические барьеры. Сильнее всего гистогематические барьеры повреждают ионы переходных металлов, образующие органические комплексы с белками, аминокислотами (ионы кадмия, цинка, хрома, ртути).
Для поддержания жизнедеятельности организма происходит замена старых барьерных клеток на новые. Красные кровяные клетки полностью обновляются ежемесячно, роговое вещество удаляется с кожи ежедневно (до 6 г), а полностью кожный покров обновляется в течение месяца. Эпителий внутренней поверхности желудочно-кишечного тракта и дыхательных путей обновляется еженедельно.
Депо для ксенобиотиков. Некоторые ксенобиотики накапливаются в определенных тканях организма и могут длительное время там сохраняться. Тканевые депо, собирая ксенобиотик в одной ткани, защищают от него внутреннюю среду организма и способствуют сохранению гомеостаза. Однако если ксенобиотик задерживается в депо надолго и его концентрация значительно возрастает с течением времени, то его отравляющее действие из хронического перейдет в острое.
Способность ксенобиотиков накапливаться в определенных тканях или органах определяется их составом, строением и физико-химическими свойствами.
Неэлектролиты, метаболически относительно инертные и обладающие хорошей липоидорастворимостью, накапливаются во всех органах и тканях. При этом в первой фазе поступления яда в организм определяющим будет кровоснабжение органа, которое лимитирует достижение динамического равновесия кровь ткань. Однако в дальнейшем основным фактором, влияющим на распределение яда, является сорбционная емкость органа (статическое равновесие). Для липоидорастворимых веществ наибольшей емкостью обладает жировая ткань и органы, богатые липидами (костный мозг и др.). Для многих липоидорастворимых веществ жировая ткань является основным депо, удерживающим яд как в больших количествах, так и в течение более длительного времени, чем другие ткани и органы. При этом длительность сохранения ядов в жировом депо определяется их физико-химическими свойствами. Например, десатурация жировой ткани после отравления животных бензолом происходит в течение 30-48 ч, а инсектицидом ДДТ – в течение многих месяцев.
Для распределения ионов металлов в организме, в отличие от органических неэлектролитов, не выявлено общих закономерностей, связывающих физико-химические свойства последних с их распределением. Однако в общем ионы металлов имеют тенденцию накапливаться больше всего в тех же тканях и органах, где они обнаруживаются в больших количествах в норме как микроэлементы. Кроме того, избирательное депонирование ионов металлов обнаруживается в тканях, где имеются полярные группы, способные отдавать электроны и образовывать координационные связи с атомами металлов, и в органах с интенсивным обменом веществ. Например, щитовидная железа поглощает марганец, кобальт, никель, хром, мышьяк, рений; надпочечники и поджелудочная железа – марганец, кобальт, хром, цинк, никель; гипофиз – марганец, свинец, молибден; семенники поглощают кадмий и цинк.
Депонирование ионов большинства переходных металлов в организме обусловлено преимущественно их способностью образовывать различные органические комплексы с белками и аминокислотами. Ионы таких металлов, как цинк, кадмий, кобальт, никель, таллий, медь, олово, рутений, хром, ртуть, распределяются в организме равномерно. Они обнаруживаются при интоксикации во всех тканях. При этом наблюдается некоторая избирательность их накопления. Избирательное депонирование в любой форме ртути и кадмия происходит в почках, что связывают со специфическим сродством этих металлов к SH-группе ткани почек. В форме грубодисперсных коллоидов некоторые малорастворимые редкоземельные металлы избирательно задерживаются в таких органах, как печень, селезенка, костный мозг, богатых ретикулоэндотелиальными клетками. В костной ткани избирательно накапливаются ионы тех металлов, неорганические соединения которых хорошо диссоциируют в организме, а также ионы металлов, образующих прочные связи с фосфором и кальцием. К таким металлам относятся свинец, бериллий, барий, стронций, галлий, иттрий, цирконий, уран, торий. Кроме того, свинец при длительном его вдыхании в максимальных количествах обнаруживается также в печени, почках, селезенке и сердечной мышце.
Выделение ионов металлов из организма подчиняется экспоненциальному закону. После прекращения поступления содержание их в организме быстро нормализуется. Во многих случаях выделение протекает неравномерно, многофазно, причем каждая фаза имеет свою экспоненциальную кривую. Например, большая часть вдыхаемых паров ртути удаляется из организма почками в течение нескольких часов, но удаление ее остаточных количеств затягивается на несколько дней; выделение остаточных количеств урана затягивается до 900 ч, а выделение цинка длится более 150 суток.
Транспортные системы. По своему назначению в организме животных и человека транспортные системы подразделяются на две группы. К первой группе относятся транспортные системы, очищающие внутреннюю среду всего организма. Вторую группу составляют транспортные системы, выводящие ксенобиотик из наиболее важного одного органа.
Транспортные системы первой группы находятся во многих органах, но наиболее мощные из них – в клетках печени и почечных канальцев.
Пища и другие вещества в желудке перевариваются лишь частично. В основном пищеварительный процесс протекает в тонком кишечнике. Переваренная пища и небольшие молекулы и ионы ксенобиотиков переходят через стенки тонкого кишечника в кровь и с кроветоком поступают в печень. Непереваренная пища и молекулы или ионы ксенобиотиков, не прошедшие через стенки тонкого кишечника, выводятся из организма.
В клетках печени структурный белок-переносчик идентифицирует вредные вещества и отделяет их от полезных. Полезные для организма вещества (глюкоза, запасаемая в виде гликогена, и другие углеводы, аминокислоты и жирные кислоты) выбрасываются в кровь для переноса к тем клеткам, жизнедеятельность которых они обеспечивают. Небольшая часть молекул глюкозы и аминокислот возвращается в печень для превращения их в необходимые крови белки.
Балластные вещества и некоторые ксенобиотики переносятся желчью в кишку и выводятся из организма. Другие ксенобиотики претерпевают в печени химические превращения, делающие их менее токсичными и более растворимыми в воде, легко выводимыми из организма.
В процессе выведения из организма ксенобиотиков и продуктов их превращения определенную роль выполняют легкие, органы пищеварения, кожа, различные железы. Наибольшее значение при этом имеют почки. Определяющую в процессах выведения функцию почек используют при отравлениях усилением мочеотделения для быстрейшего удаления из организма токсичных веществ. Однако многие ксенобиотики (ртуть и др.) оказывают при этом повреждающее воздействие на почки. Кроме того, в почках могут задерживаться продукты превращения ксенобиотиков. Например, при отравлениях этиленгликолем в процессе его окисления в организме образуется щавелевая кислота и в почечных канальцах выпадают кристаллы оксалата кальция, препятствующие мочеотделению.
Транспортные системы второй группы имеются, например, в желудочках головного мозга. Они выводят ксенобиотики из ликвора (жидкости, омывающей мозг) в кровь.
Механизм вывода ксенобиотиков транспортными системами обеих групп одинаков. Транспортные клетки образуют слой, одна сторона которого граничит с внутренней средой, а другая – с внешней. Липидная мембрана клеток этого слоя не пропускает водорастворимые ксенобиотики во внутреннюю среду клетки. Но в этой мембране имеется специальный транспортный белок – белок-переносчик, который идентифицирует вредное вещество, образует с ним транспортный комплекс и проводит его через липидный слой из внутренней среды во внешнюю.
Основная масса ксенобиотиков выводится двумя транспортными системами – для органических кислот и для органических оснований.
Число молекул белка-переносчика в мембране ограничено. При высокой концентрации ксенобиотиков в крови все молекулы белка-переносчика в мембране могут быть заняты, и тогда процесс переноса становится невозможным. Кроме того, некоторые ксенобиотики повреждают или даже убивают транспортные клетки.
Транспорт ионов металлов осуществляется преимущественно кровью в связанном с белковыми фракциями крови виде. В транспорте многих ионов металлов (например, свинца, хрома, мышьяка) большая роль принадлежит эритроцитам.
Ферментные системы. В процессах детоксикации попавших в кроветок ксенобиотиков определяющую роль выполняют ферментные системы, превращающие токсичные ксенобиотики в менее токсичные, более растворимые в воде и легче выводимые из организма соединения. Такие химические превращения протекают под воздействием ферментов, катализирующих разрыв какой-либо химической связи в молекуле ксенобиотика или, наоборот, взаимодействие молекул ксенобиотика с молекулами других веществ.
Наиболее мощные ферментные системы находятся в клетках печени. В большинстве случаев ферментные системы печени обезвреживают ксенобиотики, попавшие в кровь, оттекающую от кишечника и поступающую в печень, и предотвращают их поступление в общий кроветок. Типичным примером процесса детоксикации ксенобиотиков ферментными системами печени является биохимическое превращение в организме малорастворимого в воде бензола в хорошо растворимый в воде и легковыводимый из организма пирокатехин.
Биохимическое превращение в организме бензола протекает по трем направлениям: окисление (гидроксилирование) бензола в ароматические спирты, образование конъюгатов и полное разрушение его молекулы (разрыв ароматического кольца).
Другим примером процесса детоксикации ксенобиотиков ферментными системами печени является окисление токсичного сульфита в сульфат:
2SO32– (водн) + O2 (водн) 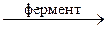 2SO42– (водн)
2SO42– (водн)
Фермент, катализирующий эту реакцию, содержит ион молибдена. Без этого микроэлемента в клетках печени большая часть пищи была бы для организма человека и животных токсичной.
Возможности ферментных систем печени обезвреживать содержащиеся в кроветоке ксенобиотики ограничены. Поскольку процессы детоксикации связаны с расходованием важнейших для жизнедеятельности клеток веществ, то эти процессы могут вызвать их дефицит в организме. Вследствие этого появляется опасность развития вторичных болезненных состояний из-за дефицита необходимых метаболитов. Например, детоксикация многих ксенобиотиков зависит от запасов в печени гликогена, поскольку из него образуется глюкуроновая кислота. При поступлении в организм больших доз ксенобиотиков, обезвреживание которых осуществляется посредством образования глюкуроновой кислоты (например, бензольных производных), снижается содержание гликогена (основного легкомобилизуемого резерва углеводов). Однако есть вещества, которые под воздействием ферментов печени способны отщеплять молекулы глюкуроновой кислоты и тем самым способствовать обезвреживанию ядов. Одним из таких веществ является глицирризин, входящий в состав солодкового корня.
Кроме того, при попадании в кроветок ксенобиотиков в больших дозах функции печени могут подавляться. Перегрузка печени ксенобиотиками может привести также к их накоплению в жировых тканях организма и хроническому отравлению.