рефераты конспекты курсовые дипломные лекции шпоры
- Раздел Электроника
- /
- Типы химических связей, образующихся между токсикантами и молекулами-мишенями организма
Реферат Курсовая Конспект
Типы химических связей, образующихся между токсикантами и молекулами-мишенями организма
Типы химических связей, образующихся между токсикантами и молекулами-мишенями организма - раздел Электроника, С. А. Куценко Основы токсикологии, Санкт-Петербург, 2002 При Взаимодействии Токсиканта С Биологическими Структурами-Мишенями Могут Обр...
При взаимодействии токсиканта с биологическими структурами-мишенями могут образовываться различные типы химических связей (таблица 3).
Таблица 3 – различные типы связей, формирующихся между токсикантами и молекулами-мишенями организма
| Вид связи | Пример | Энергия связи (кдж/мол) |
| Ионная | 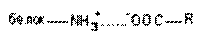
| |
| Ковалентная | 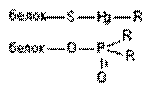
| 40 – 600 |
| Донорно-акцепторная | 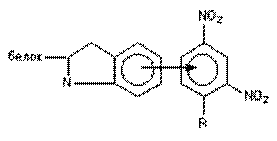
| 4 – 20 |
| Ион-дипольная | 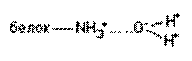
| 8 – 20 |
| Диполь-дипольная | 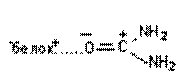
| 4 – 12 |
| Водородная | 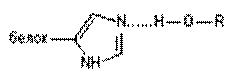
| 4 – 28 |
| Ван-дер-Ваальса | 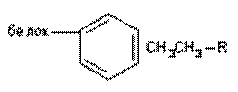
| 1 – 4 |
| Гидрофобная | 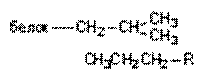
| 1 – 6 |
Ионная связь. В водных растворах многие вещества диссоциируют с образованием ионов. Между положительно и отрицательно заряженными ионами токсиканта и эндогенными ионами-мишенями начинают действовать силы электростатического притяжения. Вследствие притяжения возникает химическая связь. Связь такого типа называется электровалентной или ионной. Образованные катионами и анионами вещества не несут электрического заряда.
А– + В+  АВ
АВ
Токсические последствия подобного взаимодействия в организме развиваются в случае образования не растворимого в воде комплекса иона-токсиканта с биологически значимым ионом-мишенью. Например, при интоксикации фторидами, ион фтора может вступать во взаимодействие с ионом кальция. В итоге образуется нерастворимый фторид кальция. Развивающаяся гипокальциемия имеет определенное значение для развития и проявления интоксикации. Аналогичным образом действует щавелевая кислота, образующаяся в организме в процессе метаболизма этиленгликоля при интоксикации последним:
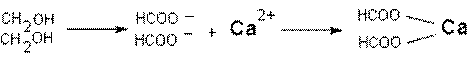
Поскольку степень диссоциации многих веществ в водном растворе существенно зависит от рН среды, количество образовавшихся за счет ионной связи комплексов токсикант-мишень также зависит от этого показателя.
Ковалентная связь. Для образования ковалентной связи, взаимодействующие атомы должны иметь на внешней электронной орбите неспаренные электроны. Эти электроны занимают одну и ту же орбиталь, а образовавшаяся общая пара формирует силу притяжения между атомами. В результате образования такой общей пары электронов каждый из взаимодействующих атомов приобретает «завершенный набор» электронов и образовавшееся соединение становится стабильным. Энергия ковалентной связи велика и составляет 200 – 400 кдж/мол
Высокая стабильность связи этого типа означает практически необратимый характер присоединения токсиканта к структуре-мишени. Примерами веществ, образующих с биомолекулами подобную связь, являются ФОС (взаимодействуют с серином, входящим в структуру активного центра ацетилхолинэстеразы), иприты (взаимодействуют с пуриновыми основаниями нуклеиеновых кислот), а также целый ряд других распространённых токсикантов (метилбромид, метилхлорид, этиленоксид и др.). Вследствие прочности образовавшейся связи, разрушение комплекса токсикант-биомишень возможно только с помощью специальных средств (например, реактиваторов ХЭ при интоксикации ФОС). Восполнение содержания поврежденной токсикантом биологической структуры возможно также за счет синтеза её de novo. Так, восстановление активности АХЭ в тканях лабораторных животных отравленных зоманом проходит со скоростью синтеза энзима нервными клетками.
Координационная связь – это ковалентная связь, в которой обобществленною пару электронов предоставляет только один из участвующих в связи атомов. Один из атомов является донором, а другой акцептором электронной пары, поэтому эту связь называют также донорно-акцепторной. Акцепторами часто являются катионы металлов, или атомы переходных металлов (Zn, Cu, Fe), входящих в состав молекулы. Таким образом, в частности, оксид углерода взаимодействует с железом гемоглобина, с образование карбоксигемоглобина.
Водородная связь. Ковалентная связь между атомом водорода и электроотрицательным атомом (кислород, азот, сера и т.д.) более или менее поляризована
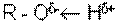
Вследствие этого атом водорода приобретает незначительный положительный заряд. Если в близи такого атома находится молекула или группа, содержащая анион или электроотрицательный атом, между ними образуется слабая связь, называемая водородной.
Водородная связь может образовываться как между молекулами, так и между атомами внутри молекул. Энергия связи не велика и в водном растворе составляет около 20 кдж/мол. Её прочность во многом зависит от строения взаимодействующих веществ, в частности, от степени электроотрицательности атомов, связанных с водородом. Электроотрицательность атомов возрастает в ряду:
Н = P < C = S = I < Br < Cl = N < O < F
2,1 2,1 2,5 2,5 2,5 2,8 3,0 3,0 3,4 4,0
Водородные связи имеют очень большое значение для поддержания пространственной структуры белков, нуклеиновых кислот и других высокомолекулярных соединений. Вещества, способные разрушать водородную связь, могут нарушать пространственную структуру макромолекул (явление интерколации: встраивание молекул акридина, этидиумбромида между плоскостями, образуемыми витками спирали молекулы ДНК).
В состав молекул токсикантов также входят группы, способные участвовать в образовании водородных связей. Если эти группы (Х–Н) являются структурными элементами «активного» радикала токсиканта, то они участвуют в образовании сложной связи вещества с молекулой-мишенью. Поскольку водородные связи являются по сути электростатическими, их сила ослабевает в присутствии веществ, обладающих свойствами диэлектриков («неэлектролитов»).
Связи Ван-дер-Ваальса. Форма электронного облака молекул квазистабильна, то есть не изменяется до тех пор, пока на неё не действуют внешние силы. Под влиянием электромагнитных полей электронные облака молекул деформируются. При этом безразлично вызвано ли появление деформируящих сил воздействием внешних полей или поле сформировано близлежащими ионами, диполями, аполярными молекулами. Степень деформированности электронного облака зависит от энергетических характеристик воздействующих полей и поляризуемости самой молекулы. Способность электронного облака к деформации (поляризуемость) зависит от размеров молекулы. У больших молекул она больше, чем у малых, поскольку сместить электроны, находящиеся на значительном удалении от ядра атома, легче.
Деформирующее воздействие полейпревращает неполярные молекулы в диполи, так как центры максимальной плотности положительного и отрицательного зарядов молекулы несколько разъединяются в пространстве. Сформировавшийся диполь называют индуцированным или временным, поскольку он перестает существовать сразу после прекращения действия деформирующих сил. Две близлежащие неполярные молекулы могут взаимно индуцировать образование временных диполей и, таким образом взаимодействовать друг с другом. Силы взаимодействия, формирующиеся между временными диполями, называются силами Лондона – Ван-дер-Ваальса. Энергия образующейся связи мала, однако она существенно возрастает при увеличении числа участков контакта между взаимодействующими молекулами. Со стороны токсиканта это могут быть ароматические, гетероциклические, алкильные радикалы; со стороны рецептора – неполярные участки молекул аминокислот (лейцин, валин, аланин, пролин и др.). Вклад каждой –СН2– группы алкильной цепи во взаимодействие оценивается в 2 – 4 кдж/мол. При тесном контакте больших неполярных молекул энергия связи может достичь очень больших величин. Поэтому при образовании комплекса токсикант-биомишень силы Ван-дер-Ваальса могут обеспечивать очень прочную фиксацию ксенобиотика. Действующая сила, ответственная за формирование связи, обратно пропорциональна седьмой степени расстояния между взаимодействующими молекулами. Поэтому она не может обеспечить притяжение молекул токсиканта, свободно циркулирующих в биосредах, к рецептору. В этом процессе первостепенную роль играют силы электростатического взаимодействия. Однако после того как контакт между токсикантом и рецептором осуществился силы Ван-дер-Ваальса обеспечивают его ориентацию и плотную фиксацию.
Гидрофобное взаимодействие. Гидрофобные связи формируются в водной среде, когда молекулы взаимодействующих веществ контактируют друг с другом неполярными (гидрофобными) участками. В отличии от взаимодействия Ван-дер-Ваальса и донорно-акцепторного взаимодействия, которые также формируются при взаимодействии неполярных групп, образование гидрофобных связей обусловлено свойствами воды, без участия которой взаимодействие происходить не может. В соответствии с теорией, молекулы воды связаны друг с другом водородными связями, образуя трехмерную структуру (кластер), напоминающую структуру льда. На границе поверхности, разделяющей неполярную молекулу и молекулы воды, образование такой структуры затрудняется. При контакте двух неполярных молекул, растворенных в воде, общая площадь поверхности, разделяющей воду и эти молекулы уменьшается. Вследствие этого, мобилизуется часть молекул воды, организованных в кластер. В противоположность всем другим химическим связям и взаимодействиям гидрофобная связь, таким образом, обусловлена преобразованием растворителя (воды), а не растворенных взаимодействующих веществ. Движущей силой образования связи является рост энтропии целостной системы растворитель – растворенные молекулы. Структурная организация гидрофобных, взаимодействующих молекул возрастает (уменьшение энтропии), но при этом существенно дезорганизуется (энтропия возрастает) структура растворителя (воды).
Гидрофобные связи имеют большое значение при взаимодействии неполярных молекул ксенобиотиков с клеточными и внутриклеточными мембранами, для образования их комплексов с белками, при этом возможно нарушение конформации макромолекул.
В процессе взаимодействия низкомолекулярного вещества с биомишенью практически всегда формируется несколько типов связей (рисунок 3), поскольку молекула токсиканта, как правило, включает полярный (иногда даже ионизированный), и неполярный фрагменты.
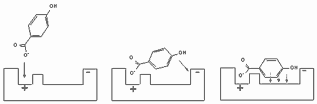
Рисунок 3 – Этапы взаимодействия молекулы токсиканта с биомишенью
Ионные связи, за счет которых осуществляется притяжение молекулы к биомишени, мало специфичны (аналогично ион-дипольному и диполь-дипольному взаимодействию). Взаимодействие между неполярными группами также неспецифично. Однако, если в структуре мишени (например, рецепторе для эндогенных биорегуляторов) полярные и неполярные группы пространственно организованы, между этими участками и особыми участками молекулы токсиканта образуются специфичные связи, обусловленные пространственной организацией молекулы токсиканта. Такое взаимодействие можно сравнить с ориентацией намагниченых стрелок в магнитном поле. После ориентации молекулы с помощью ионного (диполь-дипольного) взаимодействия между ней и рецептором формируется тесный контакт, и образуются связи за счет водородных сил и сил Ван-дер-Ваальса. Образующийся комплекс тем более прочен, чем более комплементарна молекула токсиканта рецептору.
– Конец работы –
Эта тема принадлежит разделу:
С. А. Куценко Основы токсикологии, Санкт-Петербург, 2002
ПРЕДИСЛОВИЕ АВТОРА... В этой книге изложены основные представления современной токсикологии Цель к... В ХХ веке в связи с бурным развитием промышленности и внедрением бесчисленного количества химических веществ...
Если Вам нужно дополнительный материал на эту тему, или Вы не нашли то, что искали, рекомендуем воспользоваться поиском по нашей базе работ: Типы химических связей, образующихся между токсикантами и молекулами-мишенями организма
Что будем делать с полученным материалом:
Если этот материал оказался полезным ля Вас, Вы можете сохранить его на свою страничку в социальных сетях:
| Твитнуть |
Хотите получать на электронную почту самые свежие новости?







Новости и инфо для студентов