Первая фаза метаболизма
Разнообразие чужеродных химических веществ, способных подвергаться в организме метаболическим превращениям, является следствием многообразия энзимов, участвующих в l фазе биотрансформации и их низкой субстратной специфичности. Многие из энзимов существуют в нескольких формах (изоферменты), различающихся по своим физико-химическим свойствам (молекулярная масса, электрофоретическая подвижность, абсорбцией света с разними длинами волн), отношению к индукторам и ингибиторам (см. ниже) и активностью в отношении субстратов различного строения.
Энзимы l фазы, участвующие в процессе биотрансформации ксенобиотиков, можно классифицировать в соответствии с типом активируемой ими реакции:
1. Оксидазы смешанной функции: цитохромР-450 (Р-450) и флавинсодержащие монооксигеназы (ФМО);
2. Простогландинсинтетазы - гидропероксидазы (ПГС) и другие пероксидазы;
3. Алкогольдегидрогеназы и альдегиддегидрогеназы;
4. Флавопротеинредуктазы;
5. Эпоксидгидролазы;
6. Эстеразы и амидазы.
Примеры веществ, подвергающихся метаболизму при участии указанных энзимов, приведены в таблице 2.
Таблица 2. Примеры веществ, подвергающихся биотрансформации при участии энзимов l фазы
| Энзимы и реакции | Вещества |
| 1. ЦитохромР-450 -эпоксид/гидроксилирование -N,O,S-деалкилирование -N,S,P-окисление -десульфурация -дегалогенирование -нитро-восстановление -азо-восстановление 2. ФМО -N,S,P-окисление -десульфурация 3. Простогландинсинтетаза -дегидрирование -N-деалкилирование -эпоксид/гидроксилирование -окисление 4. Алкогольдегидрогеназа -окисление -восстановление 5. Альдегиддегидрогеназа -окисление 6. Эстеразы, амидазы -гидролиз 7. Эпоксидгидролазы -гидролиз | Алдрин, афлатоксины Этилморфин, метилмеркаптан Тиобензамид, 2-ацетиламинофторид Паратион, сероуглерод СCl4, хлороформ Нитробензол О-аминоазотолуол Никотин, тиомочевина Ацетаминофен Диметиланилин Бенз(а)пирен Билирубин Метанол, этанол, гликоли Альдегиды, кетоны Альдегиды Параоксон, зарин Ареноксиды |
Особое значение для биотрансформации ксенобиотиков имеют микросомальные энзимы. Как уже указывалось, морфологическим эквивалентом микросом в интактных клетках является гладкий эндоплазматический ретикулум. Ферменты микросом не принимают участие в окислении большинства эндогенных соединений, таких как аминокислоты, нуклеотиды, сахара и т.д., для которых существуют специфические пути превращения. Однако в метаболизме некоторых эндогенных соединений (например, стероидов) микросомальные оксидазы принимают участие наряду со специфическими ферментными комплексами. Под влиянием этих энзимов могут метаболизировать некоторые жирные кислоты, простогландины и т.д. Кофакторы микросомальных монооксигеназ, принимающих участие в метаболических превращения ксенобиотиков, представлены на рисунке 6.
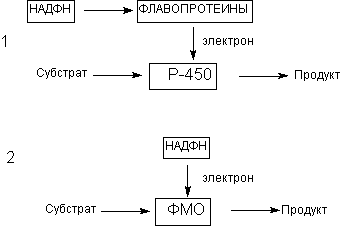
Рисунок 6. Кофакторы энзимов l фазы метаболизма ксенобиотиков: (1) цитохромР-450 зависимые оксидазы (Р-450); (2) флавинсодержащие монооксигеназы (ФМО)
В ходе микросомального окисления часто образуются реакционноспособные промежуточные продукты. Некоторые из них нестабильны и подвергаются дальнейшему превращению, другие достаточно устойчивы.
В таблице 3 представлены некоторые примеры биопревращений, приводящих к образованию реактивных продуктов.
Таблица 3. Примеры биотрансформации ксенобиотиков с образованием активных промежуточных продуктов в ходе l фазы метаболизма
| Исходное вещество | Продукт реакции | Класс соединения | Энзимы |
 хлороформ хлороформ
| 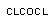 фосген фосген
| ацилгалоген | Р-450 |
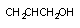 аллиловый спирт аллиловый спирт
| 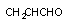 акролеин акролеин
| ненасыщенный альдегид | алкоголь дегидрогеназа |
 дихлорэтан дихлорэтан
| 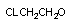 хлорацетальдегид хлорацетальдегид
| альдегид | Р-450 |
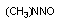 диметил нитрозамин диметил нитрозамин
| 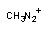 ион метилдиазониума ион метилдиазониума
| алкил диазониум | Р-450 |
 гексан гексан
| 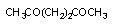 гександион гександион
| дикетон | Р-450 алкоголь дегидрогеназа |
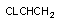 винилхлорид винилхлорид
|  хлорэтиленэпоксид хлорэтиленэпоксид
| эпоксид | Р-450 |
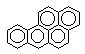 бенз(а)пирен бенз(а)пирен
| 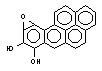 бензпирендиолэпоксид бензпирендиолэпоксид
| диол эпоксид | Р-450 эпоксидгидролаза пероксидаза |
 бензол бензол
| 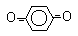 бензохинол бензохинол
| хинол | Р-450 пероксидаза |
| CCL4 тетрахлор метан | CCL3* тетрахлорметил-радикал | алкильный радикал | Р-450 |
 р-аминофенол р-аминофенол
|  р-бензохинонимин р-бензохинонимин
| хинонимин | пероксидаза |
3.1. Окислительно-восстановительные превращения