Взаимосвязь структуры и свойств материалов
Свойства материала определяются его структурой, которая по степени локальности может быть разделена на следующие ступени:
- макроструктура, составляющие которой различаются невооруженным глазом или при небольших увеличениях до 50 крат. Примером макроструктуры является зеренное строение сплавов, структура первичной кристаллизации, состоящая из дендритных (древовидных кристаллов, строение излома и т.д.;
- микроструктура, характеризует фазовый состав; форму, распределение, объемное соотношение и дисперсность фазовых составляющих, различима она только при увеличениях оптического или электронного микроскопов от ´50 до ´30000 и более.
- кристаллическая структура – индивидуальна для каждой из твердых фаз и характеризует закономерность периодически повторяющегося расположения атомов, ионов или молекул в пространстве. Экспериментально может изучаться с помощью дифракции рентгеновских лучей.
Фазой называется однородная по химическому составу и свойствам часть сплава, отделенная от остальной части системы границей раздела, при переходе через которую состав и свойства резко меняются.
Основной характеристикой твердой фазы является индивидуальная, присущая только этой фазе кристаллическая структура.
Для описания кристаллической структуры используют математическую модель пространственную решетку, в узлах которой располагаются атомы или ионы данного вещества. Пространственную решетку можно воспроизвести с помощью элементарной ячейки – наименьшего повторяющегося объёма и основных векторов трансляций 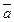
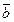
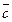 , направленных вдоль атомных рядов с наибольшей плотностью атомов. Длина вектора трансляции равна кратчайшему расстоянию между двумя одинаковыми атомами в этом ряду. Элементарная ячейка представляет собой параллелепипед, ребра которого являются трансляциями,
, направленных вдоль атомных рядов с наибольшей плотностью атомов. Длина вектора трансляции равна кратчайшему расстоянию между двумя одинаковыми атомами в этом ряду. Элементарная ячейка представляет собой параллелепипед, ребра которого являются трансляциями, 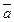
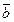
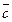 , а вершины - узлами решетки. Такие ячейки являются примитивными. В центре ячейки или в центре её граней тоже могут располагаться узлы, заполненные такими же атомами, что и в вершинах. В этом случае ячейки называются объёмно-, гране- или базоцентрированными. Транслируя (повторяя) элементарную ячейку по векторам
, а вершины - узлами решетки. Такие ячейки являются примитивными. В центре ячейки или в центре её граней тоже могут располагаться узлы, заполненные такими же атомами, что и в вершинах. В этом случае ячейки называются объёмно-, гране- или базоцентрированными. Транслируя (повторяя) элементарную ячейку по векторам 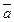
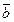
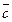 бесконечное число раз можно воспроизвести всю бесконечную пространственную решетку. Элементарная ячейка является полномочным представителем своей решетки и, поэтому для описания кристаллической структуры достаточно изучить строение ячейки.
бесконечное число раз можно воспроизвести всю бесконечную пространственную решетку. Элементарная ячейка является полномочным представителем своей решетки и, поэтому для описания кристаллической структуры достаточно изучить строение ячейки.
 Все многообразие кристаллических структур охватывается семью трасляционными группами
Все многообразие кристаллических структур охватывается семью трасляционными группами 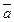
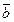
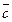 , – семью сингониями: триклинной, моноклинной, ромбической, ромбоэдрической, гексагональной, тетрагональной и кубической.
, – семью сингониями: триклинной, моноклинной, ромбической, ромбоэдрической, гексагональной, тетрагональной и кубической.
Каждая из сингоний характеризуется соотношением модулей элементарных трансляций a0, b0, c0 и углами между ними - a, b, g, и может быть представлена в виде трехосной системы координах XYZ.
В кристаллической структуре в разных направлениях и в разных плоскостях атомы располагаются на разных расстояниях друг от друга, соответственно, различна энергия их взаимодействия, зависящая от расстояния между атомами и типа химической связи. Поэтому кристаллические тела обладают анизотропией свойств, т.е. свойства кристалла в разных направлениях и в разных плоскостях различны. Наибольшее значение для формирования свойств кристаллов имеют направления и плоскости кристаллической решетки с наибольшей ретикулярной (решетчатой) плотностью атомов. Чтобы однозначно определить положение таких плоскостей в пространстве решетки используют кристаллографическое индицирование относительно осей координат той сингонии, к которой принадлежит данная кристаллическая структура.
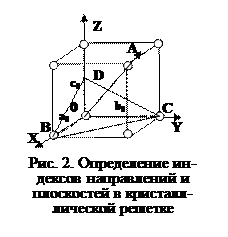 Символы направления [uvw] и плоскости (hkl) определяют их наклон к осям координат XYZ. У параллельных направлений и параллельных плоскостей символы одинаковы. Индексы направления [uvw] и индексы плоскости (hkl) представляют собой три взаимно простых, целых и малых числа. Индексы направления соответствуют координатам узла, лежащего на данном направлении, если оно проходит через начало координат. Например, направление 0А в примитивной кубической ячейке имеет индексы как у узла «А» – [111], напомню, что измерения по осям координат производятся в осевых отрезках a0, b0 и c0. Индексы плоскости соотносятся как величины обратные отрезкам, отсекаемым на осях координат плоскостью. Например, плоскость BCD имеет символ (112), т. к.
Символы направления [uvw] и плоскости (hkl) определяют их наклон к осям координат XYZ. У параллельных направлений и параллельных плоскостей символы одинаковы. Индексы направления [uvw] и индексы плоскости (hkl) представляют собой три взаимно простых, целых и малых числа. Индексы направления соответствуют координатам узла, лежащего на данном направлении, если оно проходит через начало координат. Например, направление 0А в примитивной кубической ячейке имеет индексы как у узла «А» – [111], напомню, что измерения по осям координат производятся в осевых отрезках a0, b0 и c0. Индексы плоскости соотносятся как величины обратные отрезкам, отсекаемым на осях координат плоскостью. Например, плоскость BCD имеет символ (112), т. к.
h : k : l = 1/0B : 1/0C : 1/0D = 1/1: 1/1: 1/(1/2) = 1 : 1 : 2.
В реальных кристаллах всегда присутствуют дефекты кристаллической структуры. Важнейшие дефекты, определяющие свойства кристаллических материалов – это вакансии, межузельные и примесные атомы, а также дислокации.
Вакансия представляет собой незаполненный (пустой) узел кристаллической решетки. Межузельный атом – лишний атом, расположенный в непредусмотренном кристаллической решеткой месте между узлами. Примесный атом располагается в узле решетки, но является атомом другого химического элемента. Вакансии определяют многие свойства твердых веществ, например, обеспечивают диффузионное перемещение атомов в кристаллической решетке – массоперенос, без которого невозможны нормальные фазовые превращения металлов и сплавов в твердом состоянии. Межузельные и узловые примесные атомы обеспечивают образование твердых растворов – основных фаз металлических сплавов. От концентрации и химической природы примесных атомов зависят свойства твердых растворов, в частности их упрочнение. Наибольшее упрочняющее действие оказывают атомы, расположенные в межузлиях, так они в наибольшей степени искажают кристаллическую решетку вокруг себя.
Дислокации относятся к линейным дефектам кристаллической решетки. Краевую дислокацию можно представить себе как лишнюю кристаллическую полуплоскость (экстраплоскость), обрывающуюся внутри кристалла. Аналогично обрывку страницы в книге. Край экстраплоскости, обычно, прямой является линией дислокации. Под действием приложенного напряжения линия дислокации может перемещаться в некоторой плоскости скольжения вплоть до выхода на поверхность кристалла, где образуется ступенька, высота которой равна межатомному расстоянию – этот процесс является элементарным актом пластической деформации. Макропластическая деформация представляет собой результат скольжения большого количества дислокаций. Торможение движения дислокаций какими-либо препятствиями, например, скоплением примесных атомов, неподвижными (закрепленными) дислокациями или границами зерен в поликристаллических материала, соответствует упрочнению материала, так как повышает сопротивление материала пластической деформации.
|
Металлическая связь в кристаллах осуществляется электростатическим взаимодействием между положительно заряженными катионами, расположенными в узлах кристаллической решетки и свободными, обобществленными для всех катионов кристалла электронами, образующими электронный газ, в который погружена решетка.
Присутствие в металлических кристаллах свободных электронов определяет многие свойства металлов, в частности, хорошую электронную проводимость. Под действием разности потенциалов свободные электроны приходят в направленное движение, осуществляя электрический ток.
Свободные электроны определяют и хорошую теплопроводность металлов. Повышение температуры увеличивает кинетическую энергию электронов, которые, свободно перемещаясь в решетке и сталкиваясь с катионами, расположенными в узлах, передают им часть знергии, повышая энтальпию, т. е. теплоту.
Плотнейшая упаковка и высокая степень симметрии определяют пластичность металлов. У металлов с ГЦК и ОЦК структурой большое количество систем легкого скольжения, обеспечивающей благоприятную ориентацию хотя бы одной из них относительно деформирующей нагрузки. Вследствие высокой симметрии, выраженной в большом количестве симметрично равных направлений и плоскостей в которых атомы располагаются одинаково, анизотропия свойств у металлов и сплавов с кубической структурой проявляется слабо.
В состав металлических сплавов наряду с металлическими компонентами обычно входят и неметаллы, элементы с очень высоким потенциалом ионизации и высокой электроотрицательностью. Атомы таких элементов образуют кристаллические фазы с ковалентным или молекулярным типом связи. Ковалентные связи осуществляются общей для двух соседних взаимодействующих атомов парой валентных электронов. Каждый атом структуры может взаимодействовать с ограниченным числом соседей, в фазах металлических сплавов обычно с 4. Соответственно ковалентные кристаллы имеют рыхлую структуру со связями сильными, но строго направленными в сторону ближайших соседей, небольших по числу.
В этой связи ковалентные кристаллы имеют высокую твердость, например алмаз, развитую анизотропию свойств. Они являются полупроводниками, так как свободных электронов нет. Электронная или дырочная проводимость в ковалентных кристаллах обеспечивается усреднением электронной плотности атомов основного вещества и примесей.
В железоуглеродистых сплавах, например, фазой с преимущественно ковалентными связями является цементит химическое соединение Fe3C, обладающее высокой твердостью и хрупкостью. °С