Понятие о свойствах металлов.
1. Большое число различных металлов, которые применяют в технике, можно разделить на черные и цветные.
Черные металлы имеют темно-серый цвет, большую плотность, высокую температуру плавления, относительно высокую твердость и во многих случаях обладают полиморфизмом.
Цветные металлы имеют красную, желтую, белую окраску; обладают большой пластичностью, малой твердостью, относительно низкой температурой плавления; для них характерно отсутствие полиморфизма.
К черным металлам относят железо и его сплавы, к цветным – все остальные металлы и их сплавы.
В зависимости от содержания углерода чёрные сплавы делят на стали и чугуны.
Сталями называют сплавы железа с углеродом, в которых углерода содержится до 2,14%, а чугунами – свыше 2,14%.
Цветные металлы подразделяют на тяжелые (медь, свинец, олово, никель и др.), легкие (алюминий, магний и др.), редкие (молибден, вольфрам, ванадий и др.) и благородные (золото, платина, серебро).
2.Все тела состоят из атомов. Тела, в которых атомы расположены беспорядочно, называют аморфными (стекло, канифоль, воск, смола и др.). Кристаллические тела (все металлы и металлические сплавы), характеризуются упорядоченным расположением атомов. В металлах и металлических сплавах атомы находятся в узлах пространственных кристаллических решеток.
В процессе кристаллизации металлов и сплавов могут образовываться кристаллические решетки разного типа. Наиболее распространенными являются объемно- центрированная кубическая (К, V, Сr, Fеα, Мо, W), гранецентрированная кубическая (Аl, Feγ, Ni, Сu, Аg, Аu, Рb) и гексагональная решетки (Ве, Мg, Со, Zn, Тi). Гранецентрированная кубическая и гексагональная решетки характеризуются наиболее плотной упаковкой атомов и их компактным размещением (рис.12).
Расстояния между соседними атомами в кристаллической решетке (параметр решётки) исключительно малы. Для их измерения пользуются особой единицей – ангстремом (А°), который равен 1А° = 10-8 см, или нанометром (1 нм = 10-9 см).

Рис. 12. Расположение атомов в кристаллических решетках:
а – объемно-центрированная кубическая; б – гранецентрированная кубическая; в – гексагональная
3.Некоторые металлы в твердом состоянии (железо, марганец, кобальт и др.) в зависимости от температуры нагрева могут иметь кристаллические решетки различного строения и, следовательно, обладать различными свойствами. Это явление называется аллотропией, или полиморфизмом. Кроме того, известен полиморфизм под влиянием температуры и давления. При нагреве до 2000 °С и давлении ~ 1010 Па углерод в форме графита перекристаллизовывается в алмаз.
Аллотропические формы принято обозначать буквами греческого алфавита: альфа, бета, гамма и т. д.
К металлам, не претерпевающим аллотропических превращений в твердом состоянии при нагревании и охлаждении, относятся алюминий, магний, медь и др. Большое число технически важных металлов (олово, цинк, никель, кобальт и др.) подвержено аллотропическим изменениям.
4.Кристаллизацией называется образование кристаллов в металлах и сплавах при переходе из жидкого состояния в твёрдое (первичная кристаллизация), а также перекристаллизация в твёрдом состоянии (вторичная кристаллизация).
Процесс кристаллизации металла складывается из двух элементарных процессов: образования центров кристаллизации (зародышей) и роста кристаллов из этих центров. При температуре кристаллизации в жидком металле сначала образуются центры кристаллизации, причем их роль играют разные примеси, мельчайшие шлаковые и неметаллические включения. После образования зародышей атомы жидкого металла, расположенные беспорядочно, начинают располагаться вокруг этих зародышей и образуют кристаллы правильной геометрической формы. Так как кристаллизация начинается одновременно во многих местах и рост кристаллов идет по всем направлениям, то смежные кристаллы, сталкиваясь между собой, мешают свободному росту каждого. Это приводит к тому, что кристаллы приобретают неправильную внешнюю форму, несмотря на их упорядоченное внутреннее строение. Кристаллы неправильной формы принято называть кристаллитами, полиэдрами, или зернами. Образовавшиеся реальные кристаллы имеют те или иные несовершенства (дефекты) кристаллического строения, которые принято классифицировать по характеру их измерения в пространстве на точечные (нульмерные), линейные (одномерные), поверхностные (двухмерные), объемные (трехмерные).
Наиболее распространены точечные. К ним относят вакансии (узлы в кристаллической решетке, свободные от атомов), межузельные атомы (атомы, находящиеся вне узлов кристаллической решетки), а также примесные атомы, (рис.13).
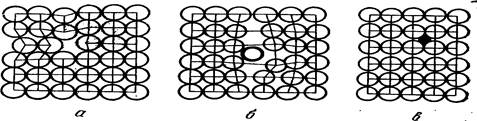
Рис. 13. Точечные дефекты в кристаллической решетке:
а – вакансия; б – межузельный атом; в – примесный атом внедрения
5.При наблюдении за охлаждением и нагревом чистого металла могут быть построены кривые охлаждения и нагревания в координатах температура – время.
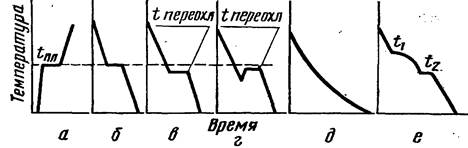
Рис. 14. Кривые нагревания и охлаждения чистого металла, аморфного тела и сплава:
а – кривая нагревания; б – кривая охлаждения без переохлаждения; в – кривая с переохлаждением; г – кривая с петлей переохлаждения; д – кривая охлаждения аморфного тела; е – кривая охлаждения сплава
Горизонтальный участок а кривой соответствует температурной остановке – температуре затвердевания или расплавления чистого металла.
Вследствие поглощения металлом скрытой теплоты плавления температура остается постоянной (tпл), что отмечено на графике горизонтальным участком кривой нагревания (рис. 14, а). Только после того как металл расплавился полностью, его температура повышается по наклонному участку кривой.
6.У металлов выделяют следующие свойства:
-физические (цвет, плотность, температура плавления, электро- и теплопроводность);
-химические (окисляемость, растворимость, коррозионная стойкость, жароупорность);
-технологические (прокаливаемость, жидкотекучесть, ковкость, свариваемость, обрабатываемость резанием);
-механические (прочность, твердость, упругость, вязкость, пластичность, хрупкость).