Диаграммы состояния двойных сплавов. Критические точки и линии.
1.Металлическими сплавами называются соединения двух или нескольких металлов и неметаллов, у которых сохраняются металлические свойства. Сплавы можно получить сплавлением компонентов в жидком состоянии, спеканием в твердом состоянии (порошковая металлургия), электролизом, возгонкой и другими способами.
Компонент – это химически индивидуальное вещество (т.е. компонентами являются химические элементы и химические соединения).
Фазы – это физически однородные части сплава, отделенные поверхностью раздела. Фазы могут быть жидкие, твердые и газообразные. Газовая смесь состоит всегда из одной фазы. Металлические сплавы в расплавленном состоянии состоят в большинстве случаев из одной фазы, а при затвердевании они состоят из жидкой и твердой фаз.
Системой называют совокупность веществ в твёрдом, жидком и газообразном состояниях. Системы бывают простые и сложные. Простая система состоит из одного компонента, а сложная система – из нескольких.
2.Структурными составляющими сплавов являются:
Механическая смесь представляет собой мельчайшую смесь кристаллов (отдельные фазы составляющих компонентов), не растворяющихся в твердом состоянии.
Химические соединения, получающиеся при образовании некоторых сплавов, имеют постоянный состав, особую кристаллическую решетку и особые физико-химические свойства. Им свойственны повышенная твердость, хрупкость и постоянная температура плавления.
Твердые растворы образуются при проникновении атомов растворяющегося элемента в кристаллическую решетку растворителя. Растворителем называют тот металл, кристаллическая решетка которого сохраняется как основа.
Различают растворы замещения и внедрения. В первом случае атомы растворимого элемента замещают в решетке атомы растворителя (рис. 19, а), во втором случае атомы растворимого элемента располагаются между атомами растворителя (рис. 19, б).
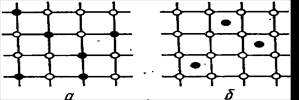
Рис.19 Расположение атомов (ионов) в твёрдых растворах:
а – твердый раствор замещения; б – твердый раствор внедрения
3.Диаграмма состояния представляет собой графическую зависимость между фазовым составом, температурой и концентрацией составляющих сплав компонентов. Она позволяет определять температуры плавления и затвердевания, структуры сплавов при разных температурах в условиях равновесия и те процессы, которые претерпевают сплавы при охлаждении и нагревании. По вертикальной оси диаграммы откладывают температуру, по горизонтальной – концентрацию компонентов в сплаве.
Теперь воспользуемся критическими точками для построения диаграммы состояния системы сплавов свинец – сурьма. Отложим в масштабе по абсциссе точки по составу сплавов, принимая, что слева будет чистый свинец, а справа – чистая сурьма (рис. 20).
Выше линии АВС все сплавы системы находятся в жидком состоянии. Линия АВС – линия ликвидуса (ликвидус – от лат. «жидкий»). Ниже линии DВЕ все сплавы системы находятся в твердом состоянии. Линия DВЕ – линия солидуса (солидус – от лат. «твердый»). Проследим процесс кристаллизации сплавов системы и получающуюся структуру.

Рис.20 Диаграмма состояния двойного сплава «свинец – сурьма»
В точке В при массовом содержании 13 % SЬ, 87 % РЬ и при температуре 246 °С кристаллизация свинца и сурьмы происходит одновременно; образуется тонкая механическая смесь кристаллов свинца и сурьмы (двух фаз). Эта смесь называется эвтектикой (эвтектика – от греч. «легкоплавящийся»), а сплав соответствующего состава – эвтектическим. Эвтектический сплав имеет самую низкую температуру плавления.
Сплавы с массовым содержанием SЬ меньше 13 % называют доэвтектическими, а SЬ больше 13 % - заэвтектическими.
Тема 9. Железоуглеродистые сплавы. Диаграмма состояния «железо-цементит».