Модели атома Томсона и Резерфорда
1. Согласно классическим представлениям атом мог бы испускать монохроматическую волну в том случае, когда электрон в атоме совершает гармонические колебания и следовательно, удерживается около положения равновесия квазиупругой силой  , где
, где  - вектор смещения электрона от равновесного положения.
- вектор смещения электрона от равновесного положения.
В 1903 году Томсон предложил первую модель строения атома, называемую моделью пудинга. Согласно этой модели атом представляет собой равномерно заряженную каплю положительно заряженной жидкости, внутри которой расположены, как изюминки в пудинге, отрицательно заряженные электроны. Суммарный электрический заряд такой системы равен нулю, т.е. атом электрически нейтрален.
Внутри равномерно заряженного шара с объемной плотностью  , где
, где 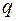 - заряд шара,
- заряд шара, 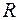 - его радиус, напряженность поля определяется формулой
- его радиус, напряженность поля определяется формулой
 ,
,
где  - радиус-вектор, проведенный из центра сферы в произвольную точку внутри шара. Следовательно, на электрон, находящийся на расстоянии
- радиус-вектор, проведенный из центра сферы в произвольную точку внутри шара. Следовательно, на электрон, находящийся на расстоянии 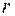 от центра шара, будет действовать сила
от центра шара, будет действовать сила
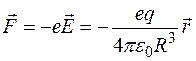 .
.
Электрон, выведенный из положения равновесия, будет совершать колебания на частоте
 .
.
Этим соотношением можно воспользоваться для оценки размеров атома водорода ( )
)
 .
.
Длине волны 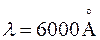 соответствует частота
соответствует частота 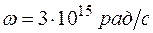 . Поэтому для атома водорода получается значение
. Поэтому для атома водорода получается значение  , что по порядку величины совпадает с газокинетическими размерами атома.
, что по порядку величины совпадает с газокинетическими размерами атома.
Но данная модель не смогла объяснить спектральный состав излучения. По классическим представлениям можно было объяснить появление в спектре излучения гармоник на частотах, кратных основной 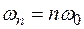 . Но частоты излучения атома не подчиняются такому закону, а подчиняются принципу Ритца.
. Но частоты излучения атома не подчиняются такому закону, а подчиняются принципу Ритца.
В дальнейшем выяснилась полная несостоятельность такой модели, так что она имеет только исторический интерес как одно из звеньев на пути развития представлений о строении атома.
2. Распределение положительных и отрицательных электрических зарядов внутри атома можно выяснить, производя опытное зондирование внутренних областей атома. Такое зондирование впервые провел Ленард с помощью пучка электронов и убедился, что атом, имея размеры порядка  внутри является прозрачным для пронизывающих его частиц. Однако окончательное доказательство этого факта и создание планетарной модели атома было дано Резерфордом в 1911 году. Его сотрудники Гейгер и Марсден изучали рассеяние
внутри является прозрачным для пронизывающих его частиц. Однако окончательное доказательство этого факта и создание планетарной модели атома было дано Резерфордом в 1911 году. Его сотрудники Гейгер и Марсден изучали рассеяние 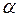 -частиц, испускаемых радиоактивным источником. Эти
-частиц, испускаемых радиоактивным источником. Эти 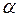 -частицы обладают большой кинетической энергией и движутся с большими скоростями порядка
-частицы обладают большой кинетической энергией и движутся с большими скоростями порядка 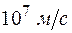 . В их опытах пучок
. В их опытах пучок 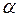 -частиц направлялся в вакууме на тонкую металлическую фольгу и рассеивался ею.
-частиц направлялся в вакууме на тонкую металлическую фольгу и рассеивался ею.
Рассеянная 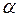 -частица при ударе о флуоресцирующий экран из сернистого цинка оставляла на нем вспышку света (сцинтилляцию). Отдельные сцинтилляции можно наблюдать в темноте через лупу или микроскоп. экспериментаторы производили подсчет таких сцинтилляций.
-частица при ударе о флуоресцирующий экран из сернистого цинка оставляла на нем вспышку света (сцинтилляцию). Отдельные сцинтилляции можно наблюдать в темноте через лупу или микроскоп. экспериментаторы производили подсчет таких сцинтилляций.
 Подавляющее число
Подавляющее число 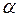 -частиц рассеивалось на небольшие углы порядка
-частиц рассеивалось на небольшие углы порядка 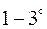 . Угловое распределение таких частиц хорошо описывается кривой случайных ошибок Гаусса. Однако наблюдались также отдельные
. Угловое распределение таких частиц хорошо описывается кривой случайных ошибок Гаусса. Однако наблюдались также отдельные 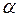 -частицы, отклоняющиеся на большие углы, доходившие до
-частицы, отклоняющиеся на большие углы, доходившие до  . Относительное число таких частиц было ничтожно мало. Тем не менее, Резерфорд посчитал, что такие большие отклонения
. Относительное число таких частиц было ничтожно мало. Тем не менее, Резерфорд посчитал, что такие большие отклонения 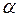 -частиц невозможно объяснить накоплением множества случайных отклонений.
-частиц невозможно объяснить накоплением множества случайных отклонений.
Резерфорд посчитал, что каждое большое отклонение появляется в результате единичного акта взаимодействия практически точечного силового центра с близко пролетающей 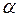 -частицей. Резерфорд предположил, что таким силовым центром является ядро атома, в котором сосредоточена вся масса атома, имеющее положительный заряд. Немного раньше Резерфорд показал, что
-частицей. Резерфорд предположил, что таким силовым центром является ядро атома, в котором сосредоточена вся масса атома, имеющее положительный заряд. Немного раньше Резерфорд показал, что 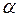 -частицы представляют собой ядра атомов гелия. (
-частицы представляют собой ядра атомов гелия. (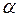 -частицу можно получить двукратной ионизацией атома гелия). Электростатическое взаимодействие между двумя ядрами и вызывает рассеяние
-частицу можно получить двукратной ионизацией атома гелия). Электростатическое взаимодействие между двумя ядрами и вызывает рассеяние 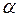 -частиц на большие углы.
-частиц на большие углы.
В результате анализа этих экспериментов Резерфорд и предложил в качестве гипотезы планетарную модель строения атома. В центре атома находится массивное положительно заряженное ядро с зарядом 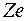 , а вокруг ядра на больших расстояниях от него движется
, а вокруг ядра на больших расстояниях от него движется  легких электронов. Атом в целом электрически нейтрален.
легких электронов. Атом в целом электрически нейтрален.