рефераты конспекты курсовые дипломные лекции шпоры
- Раздел Промышленность
- /
- Микроскопический анализ металлов
Реферат Курсовая Конспект
Микроскопический анализ металлов
Микроскопический анализ металлов - раздел Промышленность, Федеральное Агентство По Образованию Государственное Образовательное Учре...
Федеральное агентство по образованию
Государственное образовательное учреждение
высшего профессионального образования
«Омский государственный технический университет»
МАТЕРИАЛОВЕДЕНИЕ
ОмскМикроскопический анализ металлов
Цель работы: ознакомление с микроскопическим анализом металлов и сплавов, с устройством и возможностями металлографического микроскопа;освоение одной из стандартных методик микроскопического анализа сплавов.
Содержание работы
Основными методами изучения строения металлов и сплавов являются микро- и макроскопические анализы.
Макроанализ
Наиболее простым методом выявления строения металла является изучение излома. В отличие от аморфного тела металлы имеют зернистый (кристаллический)… Рис. 1.1. Макроструктура: а – излом слитка сурьмы; б – макроструктура сварного соединенияМикроанализ
· для определения количества и типа структурных составляющих металлов и сплавов; · для оценки формы, размера и характера расположения зерен; · для определения характера и качества предшествующей обработки (термической обработки, литья, обработки давлением,…Приготовление микрошлифа
Шлифование поверхности вручную или на специальных шлифовальных станках начинают на шкурке с наиболее крупным абразивным зерном, затем постепенно… Полирование проводят на специальном полировальном станке на вращающемся круге,… Для выявления микроструктуры полированную поверхность образца подвергают травлению, т. е. действию растворов кислот,…Микроскопы металлографические
По расположению оптических систем и устройств различают вертикальные и горизонтальные микроскопы. Вертикальные микроскопы МИМ–6 и МИМ–7 при… Изображение предмета увеличивается в микроскопе дважды: в объективе и окуляре.… . (1.1)Проведение испытаний
, (1.3) где К – количество делений шкалы окуляра-микрометра в данном опыте; N –… Далее определяется средний диаметр зернаПорядок выполнения работы
Подготовка микроскопа к визуальному наблюдению
· Винтами установить отверстие съёмной шайбы над объективом. · Над отверстием съемной шайбы установить микрошлиф полированной… · Поворотом стопорного винта освободить макрометрический винт.Определение цены деления
· подготовить микроскоп к наблюдению; · установить объект-микрометр на столик микроскопа таким образом, чтобы… ·изображение шкалы объекта-микрометра отыскать в поле зрения окуляра, для чего, удерживая рукоятки грубой подачи,…Определение величины зерна стали
· микрошлиф поместить на столик микроскопа; · добиться чёткого изображения структуры; · просмотреть несколько участков шлифа; выбрать участок с наиболее крупными зернами;Контрольные вопросы
1. Задачи макроскопического анализа.
2. Задачи микроскопического анализа.
3. Приготовление объекта исследования и правила обращения с ним.
4. Принцип работы металлографического микроскопа.
5. Укажите на микроскопе и объясните назначение предметного столика.
6. Порядок настройки микроскопа на визуальное наблюдение.
7. Объясните, с какой целью осуществляется смена оптики.
8. Как определить увеличение микроскопа?
9. Цель и порядок определения цены деления окуляра-микрометра.
10. Как определить размер зерна стали окуляром-микрометром?
Отчет по лабораторной работе № 1
Микроскопический анализ металлов
2. Ознакомление с устройством микроскопа. Оптическая схема Обозначения: _________________________________ … 3. Принцип работы микроскопа:… …Лабораторная работа № 2
Изучение процесса кристаллизации
Цель работы: изучение процесса кристаллизации капель раствора четырёх солей; сравнение строение закристаллизовавшейся капли раствора нитрата свинца со строением слитка спокойной стали.
Содержание работы
Теоретические основы процесса кристаллизации металлов
Согласно законам термодинамики, устойчивым состоянием при определённых внешних условиях будет то состояние, которое обладает меньшим уровнем… Рис. 2.1. Изменение свободной энергии жидкого Gж и твёрдого Gт состояния в зависимости от температуры: Ткр −…Кристаллизация солей
Водные растворы этих солей приготавливаются почти насыщенными с тем, чтобы незначительное испарение воды привело их к состоянию перенасыщения и… Наблюдение за процессом кристаллизации солей производится с помощью…Порядок выполнения работы
2. Предметное стекло с нанесенной на него каплей соли установить на предметный столик так, чтобы капля была в центре отверстия предметного… 3. Произвести грубую настройку на фокус, для чего смотреть одним глазом в… 4. Вращением микрометрического винта произвести тонкую настройку на фокус.Контрольные вопросы
1. На рис. 2.1 укажите:
· теоретическую температуру кристаллизации (плавления) металла;
· фактическую температуру кристаллизации (плавления) металла;
· необходимое условие, при котором начнётся процесс кристаллизации (процесс плавления) металла;
·  область температур, в которых металл будет находиться в агрегатных состояниях:
область температур, в которых металл будет находиться в агрегатных состояниях:
а) жидком при охлаждении;
б) твёрдом при охлаждении;
в) твёрдом при нагреве;
г) жидком при нагреве.
2. На рис. 2.3 укажите, при какой величине переохлаждения металл закристаллизуется наиболее крупнозернистым (наиболее мелкозернистым).
3. Укажите среду закристаллизовавшегося раствора соли: а) Рb(NO3)2,
б) NH4Cl; в) К2Сr2O7; г) NaCl. Объясните особенности её строения.
4. Укажите форму и схему строения закристаллизовавшейся капли водного раствора соли, схожую со структурой слитка спокойной стали. Объясните особенности ее строения.
Отчет по лабораторной работе №2
Изучение процесса кристаллизации
2. Изменение свободной энергии жидкости и твердого тела в зависимости от температуры. … 3. Принципиальная схема зависимости ЧЗ и СК от степени переохлаждения. …Лабораторная работа № 3
Построение диаграммы состояния «Свинец – олово»
термическим методом
Цель работы: нахождение термическим методом критических точек свинца, олова и трёх сплавов из свинца и олова и построение по полученным кривым охлаждения диаграммы состояния «Свинец – олово».
Содержание работы
Общие сведения
У кристаллических тел при переходе из одного состояния в другое, при протекании фазовых превращений выделяется или поглощается теплота и физические свойства при этом меняются скачкообразно.
Температуры, при которых происходят те или иные физико-химические изменения в сплаве, называются критическими температурами, а соответствующие им точки на кривых охлаждения – критическими точками.
Для определения критических точек сплава достаточно через короткие, но равные промежутки времени измерять температуру медленно охлаждающегося от жидкого состояния до комнатной температуры сплава, затем, построив по этим данным кривую охлаждения в координатах «Температура − время», отыскать на ней точки перегиба, которые и будут являться критическими точками данного сплава.
В сплавах в зависимости от характера взаимодействия металлов друг с другом в твёрдом состоянии образуются твёрдые фазы и протекают различные фазовые превращения: образование твердых растворов, химических соединений, смесей.
По критическим точкам чистых металлов и сплавов строятся диаграммы фазового равновесия. Эти диаграммы в удобной графической форме показывают фазовый состав сплава в зависимости от температуры и концентрации компонентов и дают наглядное представление о процессах, происходящих в сплавах системы при нагреве и охлаждении.
Различают следующие основные типы диаграмм состояния:
· диаграмму для случая полной нерастворимости компонентов в твердом состоянии (образование смесей), рис. 3.1а;
· диаграмму для случая неограниченной растворимости компонентов в твердом состоянии (неограниченные твердые растворы), рис. 3.1б;
· диаграмму для случая ограниченной растворимости компонентов в твердом состоянии (ограниченные твердые растворы), рис. 3.1в;
· диаграмму для случая, когда компоненты образуют химическое соединение, рис. 3.1г.
Сплавы, образующие диаграмму первого типа (рис. 3.1а), в твердом состоянии представляют собой смеси из зерен чистых металлов А и В.
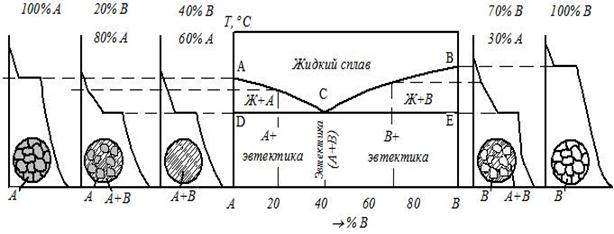
а)
Рис. 3.1. Диаграммы состояния сплавов (начало)
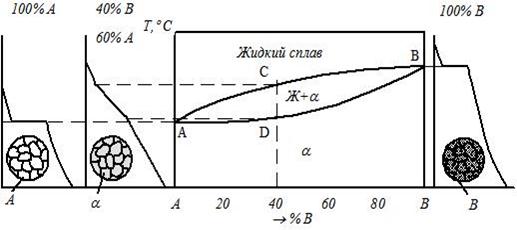
б)

в)
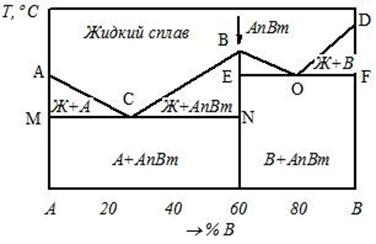
г)
Рис. 3.1. Диаграммы состояния сплавов (окончание)
В сплавах на рис. 3.1в металлы А и В образуют два типа растворов: твёрдый раствор компонента В в компоненте А – α-твёрдый раствор и твёрдый раствор компонента А в компоненте В – β-твёрдый раствор.
Совокупность точек начала кристаллизации всех сплавов системы (линия АСВ в рис. 3.1а–в) называется ликвидус. Выше этой линии все сплавы находятся в жидком состоянии.
Совокупность точек конца кристаллизации всех сплавов системы
(линия DСE на рис. 3.1а, ADB – на рис. 3.1б, АDCEB – на рис. 3.1 в) называется солидус. Ниже этой линии все сплавы находятся в твердом состоянии.
Сплавы, представленные на рис. 3.1б, ниже линии солидус при любой концентрации имеют только одну фазу – зерна твердого раствора компонента В в компоненте А.
Сплав двух металлов А и В определенной концентрации, образующийся в точке С (рис. 3.1а, в), называется эвтектическим. Такой сплав кристаллизуется подобно чистому металлу при постоянной температуре, образуя смесь кристаллов двух твёрдых растворов, называемую эвтектикой.
Сплавы с концентрацией металла В меньше эвтектической называются доэвтектическими, а с концентрацией металла В больше эвтектической − заэвтектическими сплавами.
Рассмотрим кривую охлаждения доэвтектического сплава (рис. 3.2).
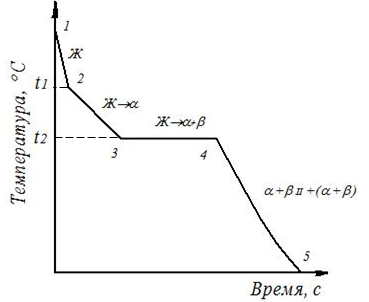
Рис. 3.2. Кривая охлаждения доэвтектического сплава
На участке 1 – 2 идет охлаждение жидкого сплава по физическим законам. В точке 1 начинается процесс кристаллизации, за счёт выделения скрытой теплоты кристаллизации уменьшается скорость охлаждения сплава и на кривой охлаждения образуется перегиб. Температура t1 – критическая точка начала кристаллизации из жидкости α-твёрдого раствора. Этот процесс продолжается до точки 3. В точке 3 начинается кристаллизация эвтектики – смеси двух фаз, выделяющихся из жидкого раствора эвтектической концентрации. Кристаллизация эвтектики происходит при постоянной температуре (участок 3 – 4) и заканчивается в точке 4 при температуре t2 по реакции Ж → (α + β). Температура t2 – критическая точка конца первичной кристаллизации сплава.
На участке 4 – 5 при охлаждении сплава понижается растворимость компонента В в компоненте А. Это приводит к выпадению вторичных кристаллов βII из α-твёрдого раствора: α → βII.
В результате описанных процессов в сплаве образуется конечная структура, состоящая из первичных кристаллов α-твёрдого раствора, эвтектики (α + β) и вторичных кристаллов βII-твёрдого раствора.
Построение диаграммы состояния
Порядок выполнения работы
2. По полученным данным построить кривую охлаждения. Для более четкого выявления перегибов на кривой охлаждения в работе будет предложен масштаб для… 3. По перегибам на кривой охлаждения определить критические точки и… 4. Найденные значения критических точек из табл. 3.2 перенести на поле диаграммы состояния «Свинец – олово», приняв…Контрольные вопросы
1. На чём основан термический анализ?
2. Укажите на диаграмме «Свинец – олово» точки начала и конца первичной кристаллизации: а) доэвтектического сплава; б) эвтектического сплава; в) заэвтектического сплава; г) фазовый состав в областях, находящихся выше и ниже этих точек.
3. Укажите на диаграмме «Свинец – олово» точку конца вторичной кристаллизации: а) доэвтектического сплава; б) заэвтектического сплава.
4.Укажите линию начала кристаллизации жидкого раствора:
а) в α-твёрдый раствор; б) в β-твёрдый раствор.
5. Укажите линию, показывающую предельную растворимость:
а) олова в свинце; б) свинца в олове.
6. Укажите процессы кристаллизации, обусловленные понижающейся растворимостью олова и свинца при охлаждении.
7. Укажите на диаграмме «Свинец – олово» области существования:
а) α-твёрдого раствора; б) β-твёрдого раствора; в) (α + β); г) α + Ж;
д) β +Ж.
8. Укажите структурный состав в различных областях диаграммы.
Отчет по лабораторной работе №3
1. Цель работы. 2. Схема установки проведения эксперимента. Описание …Лабораторная работа № 4
Микроструктура железоуглеродистых сплавов
в равновесном состоянии
Цель работы: изучение микроструктуру сталей и чугунов в равновесном состоянии и установление связи между структурой и свойствами.
Содержание работы
1.1. Фазы и структуры диаграммы «Железо – цементит»
Под равновесным состоянием понимается состояние, при котором все фазовые превращения в сплаве полностью закончились в соответствии с диаграммой состояния. Это происходит только при медленном охлаждении. Основой для определения фазовых и структурных составляющих железоуглеродистых сплавов в равновесном состоянии является диаграмма состояния «Железо – цементит» (рис. 4.1). В сплавах железа с углеродом образуются следующие фазы и структуры.

Рис. 4.1. Диаграмма состояния «Железо – цементит»
Феррит –твердый растворвнедрения углерода в Feα – мягкая, пластичная фаза (σВ = 300 МПа, δ = 40%, ψ = 70%, 650–1000 HB). Различают низкотемпературный и высокотемпературный феррит. Предельная концентрация углерода в феррите при 0 °С – 0,006 %, при 727 °С – 0,02%, в высокотемпературном феррите – 0,1%. Феррит магнитен до 768 °С. Кристаллическая решетка – кубическая объемноцентрированная.
Аустенит–твердый растворвнедрения углерода в Feγ –более твердый, чем феррит,и пластичный (δ = 40–50%, 2000–2500 НВ), не магнитен. Предельная концентрация углерода достигает 2,14% при 1147 °С. Кристаллическая решетка – кубическая гранецентрированная.
Цементит –химическое соединение Fe3C –имеет высокую твердость (8000 НВ), но практически нулевую пластичность. Температура плавления цементита около 1250 °С. Полиморфных превращений не испытывает, но при низких температурах слабоферромагнитен. Кристаллическая решетка ромбическая.
Перлит–эвтектоидная смесь феррита и цементита является прочной структурной составляющей (σВ = 800–900 МПа, δ = 16%, 1800 HB).
Ледебурит–эвтектическая смесь аустенита и цементита в интервале температур 1147–727°С, а ниже линии SK (727 °С) – смесь перлита и цементита. Ледебурит имеет высокую твердость (> 6000 HB), но хрупок.
Графит – аллотропическая модификация углерода. Имеет гексагональную решетку. Твёрдость и прочность графита очень малы.
Классификация железоуглеродистых сплавов
Структура сплавов в равновесном состоянии определяется содержанием углерода. По содержанию углерода на диаграмме «Железо – цементит»все сплавы принято делить на три группы: техническое железо, стали и чугуны.
Техническим железом называются сплавы с содержанием углерода от 0 до 0,02%. При концентрации углерода до 0,006% сплавы являются однофазными и имеют структуру феррита.
Сплавы с содержанием углерода от 0,006 до 0,02 % являются двухфазными. Это объясняется тем, что концентрация углерода в сплавах превышает его растворимость в феррите при комнатной температуре. В процессе охлаждения феррит любого сплава, имеющего концентрацию углерода свыше 0,006%, оказывается перенасыщенным. Равновесного состояния феррит достигнет за счет выделения цементита.
Сталями называются сплавы железа с углеродом, концентрация которого находится в пределах от 0,02 до 2,14 %.
Процессы, протекающие при первичной кристаллизации, на структуру сталей влияния не оказывают. Окончательная структура сталей формируется из аустенита. При 727 °С (рис. 4.1, линия РSК) все стали претерпевают эвтектоидное превращение:
А0,8 % С → П (Ф0,02 % С + Ц6,67 % С).
Продуктом данного превращения является перлит – эвтектоидная смесь феррита и цементита.
По структуре в равновесном состоянии стали делятся:
· на доэвтектоидные (концентрация углерода от 0,02 до 0,8%), при комнатной температуре состоящие из двух фаз – феррита и цементита, структура таких сталей – феррит+перлит;
· эвтектоидную (концентрация углерода 0,8%), также состоящую из двух фаз – феррита и цементита, структура – перлит;
· заэвтектоидные (концентрация углерода от 0,8 до 2,14%), имеющие структуру перлит+цементит, образованную из двух фаз: феррита и цементита.
Чугуны – железоуглеродистые сплавы, содержащие более 2,14% углерода. Если весь углерод находится в химически связанном состоянии (в виде химического соединения Fe3C), то такой чугун называется белым. Своим названием такой чугун обязан цвету излома.
Для белых чугунов характерно эвтектическое превращение при температуре 1147 °С (рис. 4.1, линия ЕСF), в результате которого образуется ледебурит – эвтектическая смесь аустенита и цементита:
Ж4,3% С → Л2,14% С + Ц6,67 % С.
При температуре 727 °С происходит превращение аустенита в перлит, и после этого ледебурит будет состоять из перлита и цементита.
По структуре в равновесном состоянии чугуны делятся:
· на доэвтектические (от 2,14% до 4,3% углерода). Фазовый состав − феррит и цементит; структурный состав − ледебурит, перлит, цементит вторичный;
· эвтектический (4,3% углерода). Фазовый состав − феррит и цементит; структурный состав − ледебурит;
· заэвтектические (от 4,3 до 6,67% углерода). Фазовый состав − феррит и цементит; структурный состав − ледебурит, цементит первичный.
Все рассматриваемые выше сплавы состоят из одинаковых фаз − феррита и цементита, но имеют разную структуру, а именно структура определяет свойства сплавов.
Белый чугун обладает хорошими литейными свойствами, но высокая твёрдость исключает его механическую обработку. Поэтому белый чугун не является конструкционным материалом. Высокие литейные свойства обеспечиваются углеродом, и в то же время углерод, соединяясь с железом, образует твёрдый цементит.
Чтобы сохранить высокие литейные свойства и понизить твёрдость чугуна, нужно, не уменьшая концентрации углерода, добиться резкого уменьшения цементитной составляющей в структуре. Для этого необходимо, чтобы весь или большая часть углерода выделилась в свободном виде в форме графита. Эту задачу решают введением в сплав кремния и медленным охлаждением отливки.
Серыми чугунами называются сплавы железа с углеродом, в которых весь или большая часть углерода находится в структурно-свободном состоянии в виде пластинчатого (лепесткового) графита. Поскольку серые чугуны, как минимум, трёхкомпонентные сплавы, то диаграмма «Железо − цементит» для определения структуры сплавов не пригодна. В серых чугунах различают металлическую основу и графитовые включения.
По металлической основе серые чугуны подразделяются:
· на ферритные серые чугуны со структурой феррит и графит пластинчатый;
· феррито-перлитные серые чугуны со структурой феррит, перлит, графит пластинчатый;
· перлитные серые чугуны со структурой перлит и графит пластинчатый.
Серые чугуны имеют хорошие литейные свойства, прекрасно обрабатываются резанием, но имеют низкую прочность и плохо сопротивляются ударным нагрузкам. Низкая прочность серого чугуна объясняется формой графита. Пластинчатый графит служит концентратором напряжения, выполняя роль надреза.
Чтобы сохранить достоинства серого чугуна и повысить его прочность, нужно изменить форму графита − пластины превратить в глобули. Эту проблему решают модифицированием − введением в расплав малых количеств магния или церия.
Высокопрочными чугунами называются сплавы железа с углеродом, в которых весь углерод или большая его часть находится в структурно-свободном состоянии в форме шаровидного графита.
По металлической основе высокопрочные чугуны делятся:
· на ферритные высокопрочные чугуны со структурой феррит и графит шаровидный;
· феррито-перлитные высокопрочные чугуны со структурой феррит, перлит и графит шаровидный;
· перлитные высокопрочные чугуны со структурой перлит и графит шаровидный.
Ковкими чугунами называются сплавы железа с углеродом, в которых весь или большая часть углерода находится в структурно свободном состоянии в виде графита хлопьевидного. Получают ковкие чугуны путём отжига белых чугунов.
По металлической основе ковкие чугуны подразделяются:
· на ферритные ковкие чугуны со структурой феррит и графит хлопьевидный;
· феррито-перлитные ковкие чугуны со структурой феррит, перлит и графит хлопьевидный;
· перлитные ковкие чугуны со структурой перлит и графит хлопьевидный.
Влияние концентрации углерода на свойства железоуглеродистых сплавов
С увеличением содержания углерода снижаются технологические свойства стали, увеличивается усадка, ухудшаются жидкотекучесть, ковкость и…Структура и свойства железоуглеродистых сплавов
Феррит является пластичной и мягкой составляющей (800 НВ, δ = 40%). Цементит – твёрдый и хрупкий (8000 НВ, δ = 0%). Наличие на границах… Рис. 4.4. Технические (двухфазное) железоПорядок выполнения работы
2. Указать фазы и структурные составляющие в различных областях диаг-раммы. 3. Подготовить к работе металлографический микроскоп. Изучение микроструктуры… 4. Просмотреть предложенные шлифы, выбрать наиболее характерные участки и зарисовать в отчете. Определить тип сплава,…Контрольные вопросы
1. Определение феррита, аустенита, цементита, графита.
2. Определение перлита, ледебурита.
3.Что такое техническое железо, сталь, чугун?
4. Каково отличие в структуре белого чугуна от серого, высокопрочного, ковкого?
5. Как получают чугун серый, ковкий, высокопрочный?
6. Как и почему меняется твёрдость сплавов по мере увеличения концентрации углерода?
7. По микрофотографии, предложенной преподавателем, определите тип сплава (техническое железо, сталь, чугун), структурный и фазовый состав, пределы содержания углерода.
8. По диаграмме «Железо − цементит» опишите процессы, протекающие в сталях и белых чугунах при кристаллизации.
Отчет по лабораторной работе № 4
1. Цель работы. 2. Диаграмма состояния сплавов «Железо – цементит».Лабораторная работа № 5
Термическая обработка стали
Цель работы: ознакомление с практикой выполнения отжига, нормализации, закалки и отпуска на примере конструкционной стали 40Х (0,4 % углерода, 1 % хрома). Изучение влияние режимов термической обработки на твёрдость стали.
Содержание работы
Свойства стали зависят от химического состава и структуры. Термической обработкой, изменяя структуру, можно получить требуемые свойства конкретной детали. Различают основные виды термической обработки стали: отжиг, нормализацию и закалку.
Любая обработка стали состоит из нагрева, выдержки при температуре нагрева и охлаждения. Нагрев и выдержка необходимы для превращения исходной структуры в однородный аустенит. Охлаждение с различной скоростью от аустенитного состояния приводит к образованию различных структур и определяет получение требуемых свойств стали.
1.1. Основные виды термической обработки стали и их
назначение
Отжиг – нагрев стали выше линии А3 (рис. 5.1) доэвтектоидной или А1 заэвтектоидной на 30–50 °С, выдержка при этой температуре и последующее охлаждение вместе с печью. Весьма медленное охлаждение приводит сталь в равновесное состояние, снижает её твёрдость. Выполняется для исправления структуры или улучшения обрабатываемости резанием конструкционных и инструментальных сталей.
Нормализация – нагрев стали выше линии А3 (доэвтектоидной) или Аст (заэвтектоидной) на 30–50 °С, выдержка при этой температуре и последующее охлаждение – на спокойном воздухе. Более ускоренное охлаждение при нормализации несколько повышает прочность и твёрдость стали. Выполняется для исправления структуры или придания большей прочности и повышенной вязкости конструкционным и инструментальным сталям.
Закалка – нагрев стали выше линии А3 (доэвтектоидной) или А1 (заэвтектоидной) на 30–50 °С, выдержка при этой температуре и последующее ускоренное охлаждение – в воде, масле или другом охладителе. Максимально повышается твёрдость и прочность конструкционных и инструментальных сталей.
Процессы нагрева стали
Если же по какой-либо причине температура нагрева окажется ниже линии А1, то исходная структура сохраняется и свойства сталей после охлаждения не… а) б)Процессы охлаждения стали
Критерием превращения является критическая скорость закалки VКР. Это наименьшая скорость охлаждения, при которой подавляется диффузия атомов…Превращение аустенита при отжиге
При превращении перестраивается решетка с диффузионным перераспределением углерода между фазами. Образовавшаяся структура – грубодисперсная…Превращение аустенита при нормализации
При охлаждении стали 40Х в масле со скоростью V3 ≈ 150 °С/с обработка называется «закалка в масло». Поскольку V3 < VКР, то термин «закалка»…Превращение аустенита при закалке
Превращение является бездиффузионным, т. к. перемещение атомов не превышает межатомного расстояния. Содержание углерода в исходном и образовавшемся… Рис. 5.3. Зависимость твёрдости мартенсита от содержания углерода в стали: 1 – закалка от температуры выше Ас3, Аст ,…Влияние температуры отпуска на структуру стали
Низкий отпуск (150–200 °С) назначается для инструментальных сталей (0,7–1,3 % углерода) для повышения вязкости (КСU ≈ 0,2 МДж/м2) при… При нагреве до 200 °С частично снимаются внутренние напряжения, так как внутри… При повышении температуры до 300–400 °С (средний отпуск) мартенсит закалки распадается на феррит и цементит. Наличие…Порядок выполнения работы
2. Назначить режимы термической обработки: · закалку с недогревом; · закалку неполную;Контрольные вопросы
1. Определение отжига, нормализации, закалки, отпуска стали.
2. Цели выполнения этих видов термообработки.
3. Основные принципы выбора температуры нагрева, времени выдержки и скорости охлаждения для указанных видов термообработки
сталей.
4. Физический смысл критической скорости закалки.
5. Основные превращения при выполнении указанных видов термообработки.
6. Как влияет температура отпуска на механические свойства сталей?
7. Объяснить зависимость твёрдости стали от температуры нагрева при закалке; от скорости охлаждения (вода, масло, воздух, охлаждение с печью); от температуры отпуска.
8. Назначить режимы закалки и отпуска для изделий из указанной стали (30, 50, 60, У7, У8, У10, У12).
Отчет по лабораторной работе № 5
Термическая обработка стали
Химической обработке подвергались образцы из стали марки _______ Химический состав ___________________________________________ Критические точки: АС1 = ________________, АС3 __________________Лабораторная работа № 6
Микроструктуры термически обработанных
углеродистых сталей
Цель работы: изучение влияния на структуру и свойства углеродистых сталей температуры нагрева при отжиге и закалке и температуры отпуска после закалки.
Содержание работы
Термической обработкой, изменяя структуру, можно получить требуемые свойства конкретной детали. Распространёнными видами обработок являются закалка, отжиг и нормализация. Любой вид термообработки предусматривает нагрев, выдержку при температуре нагрева и охлаждение. Нагрев выполняется выше линии А3 на 30–50 °С для доэвтектоидных сталей и выше линии А1 или Аст (при нормализации) на 30–50 °С для заэвтектоидных сталей (см. рис. 5.1б).
При нагреве и выдержке исходная структура сталей превращается в однородный аустенит. Охлаждение стали выполняется в различных технологических средах, которые и определяют вид обработки: при закалке – в воде, масле, отжиге – вместе с печью, при нормализации – на спокойном воздухе. Каждая среда обеспечивает определенную скорость охлаждения.
Влияние скорости охлаждения на превращение аустенита
При скоростях охлаждения V < VКР протекает диффузионный распад аустенита в феррит и цементит. В процессе превращения перестраивается… Такое превращение имеет место при отжиге, нормализации и менее… перлит пластинчатый – грубодисперсная ферритоцементитная смесь пластинчатой формы (рис. 6.1а);Влияние температуры отжига на структуру и свойства стали
Рис. 6.3. Микроструктура стали 45 до отжига (а) и после отжига (б)Влияние температуры отпуска на структуру и свойства стали
Низкий отпуск практически не изменяет вид мартенсита. Игольчатость его строения сохраняется, но несколько увеличивается травимость кристаллов. Такая… Микрошлиф 7 – сталь после закалки и среднего отпуска. Структура –троостит…Порядок выполнения работы
1. Подготовить к работе металлографический микроскоп. Изучение микроструктуры термически обработанных сталей выполняется при определённых увеличениях микроскопа.
2. На каждом микрошлифе просмотреть несколько полей, выявить участок с наиболее характерной структурой и зарисовать в отчете.
3. Объяснить влияние температуры на структуру и свойства сталей после различных видов термической обработки.
Контрольные вопросы
1. В наборе фотографий и схем структур найдите перлит пластинчатый, сорбит закалки, троостит закалки, мартенсит закалки, мартенсит отпуска, троостит и сорбит отпуска.
2. Дайте определение каждой структуре и поясните её особенности, укажите, какой термической обработкой её получают, какую твёрдость и вязкость она обеспечивает стали У8.
3. Найдите фотографии и схемы структур стали 45 после отжига с перегревом и стали У8 после закалки с перегревом, укажите названия и особенности этих двух структур, твёрдость и вязкость сталей с такими структурами. Укажите способ исправления структуры сталей.
Отчет по лабораторной работе №6
Микроструктура термически обработанных сталей
Микроструктура термически обработанных сталей изучается на микроскопе ________________ при увеличении __________________________ 2. Результаты просмотра структур: № образца Марка стали …Библиографический список
2. Гуляев, А.П. Металловедение: учеб. для вузов / А.П. Гуляев. – 6-е изд. перераб. и доп. – М. : Металлургия, 1986. – 544 с. 3. Лахтин, Ю.М. Материаловедение: учеб. для студентов вузов / Ю. М. Лахтин,… 4. Мозберг, Р.К. Материаловедение: учеб. для студентов вузов / Р. К. Мозберг. – 2-е изд. перераб. и доп – М.: Высш.…– Конец работы –
Используемые теги: Микроскопический, анализ, металлов0.062
Если Вам нужно дополнительный материал на эту тему, или Вы не нашли то, что искали, рекомендуем воспользоваться поиском по нашей базе работ: Микроскопический анализ металлов
Что будем делать с полученным материалом:
Если этот материал оказался полезным для Вас, Вы можете сохранить его на свою страничку в социальных сетях:
| Твитнуть |
Хотите получать на электронную почту самые свежие новости?







Новости и инфо для студентов