Производство нитрата аммония
5.2.1 Свойства нитрата аммония
Нитрат аммония (аммонийная селитра) NH4NO3 – кристаллическое вещество с температурой плавления 169,6ºС, хорошо растворимое в воде. Растворимость при 20ºС равна 0,625 мас. долей, при 160ºС – 0,992 мас. долей. Нитрат аммония сильно гигроскопичен и легко поглощает влагу из атмосферы, в зависимости от температуры может существовать в пяти кристаллических модификациях, различающихся плотностью и структурой кристаллов. Вследствие высокой растворимости в воде, гигроскопичности и полиморфных превращений, сопровождающихся выделением тепла, нитрат аммония легко слеживается. Для уменьшения слеживаемости, которая затрудняет использование продукта, в промышленности используют следующие меры:
- перед складированием полученный продукт охлаждают до температуры ниже 32ºС, так как именно в интервале от 32,3ºС до -17ºС нитрат аммония находится в стабильной ромбической модификации;
- выпускают товарный продукт в гранулированном виде, обрабатывая поверхность гранул ПАВ, образующими на них гидрофобную пленку;
- вводят в состав продукта кондиционирующие добавки в виде нитрата магния и других солей, которые связывают свободную воду и препятствуют переходу одной модификации в другую.
Нитрат аммония в твердом состоянии или в виде высококонцентрированного раствора (плава) при нагревании выше 180 - 200 ºС разлагается:
NH4NO3 = N2O + 2H2O – DH, где DH = 36,8 кДж.
При быстром нагревании в замкнутом пространстве до 400 - 500ºС или инициировании нитрат аммония разлагается со взрывом по уравнению
NH4NO3 = N2 + 2H2O + 0,5O2 – 118 кДж.
Разложение ускоряется в присутствии минеральных кислот и органических веществ. На этом основано использование нитрата аммония в качестве компонента аммонийно-селитровых взрывчатых веществ – аммонитов (смеси с органическими веществами), аммотолов (смеси со взрывчатыми веществами) и аммоналов (смеси, содержащие аллюминий).
Нитрат аммония является безбалластным азотным удобрением и содержит 34,8% азота, из них 17,4% - в аммиачной (NH4+) и 17,4% - в нитратной (NO3-) форме. Поэтому стоимость транспортировки содержащегося в нем азота значительно ниже, чем при перевозке других балластных удобрений (например, сульфата аммония).
5.2.2 Физико-химические основы процесса синтеза
Производство нитрата аммония основано на реакции нейтрализации азотной кислоты газообразным аммиаком с последующим упариванием полученного раствора нитрата аммония.
Нейтрализация.Нейтрализация азотной кислоты аммиаком – это необратимый гетерогенный процесс хемосорбции, протекающий с выделением тепла по уравнению
HNO3 + NH3 = NH4NO3 – DH.
Реакция идет в диффузионной области, и ее скорость лимитируется диффузией аммиака из газа к поверхности жидкости. Количество тепла, выделяющегося при нейтрализации, складывается из теплового эффекта реакции и теплоты растворения образовавшегося нитрата аммония в воде:
Qå = Q1 – (Q2 + Q3),
| где | Q1 | – | тепловой эффект реакции нейтрализации 100% азотной кислоты с образованием твердого нитрата аммония; |
| Q2 | – | теплота разбавления азотной кислоты; | |
| Q3 | – | теплота растворения нитрата аммония. |
Таким образом, тепловой эффект процесса зависит от концентрации азотной кислоты, взятой для нейтрализации.
Подогрев компонентов (азотной кислоты и газообразного аммиака) улучшает перемешивание системы, ускоряет процесс нейтрализации и повышает концентрацию раствора нитрата аммония.
Упаривание раствора нитрата аммония.В результате нейтрализации образуется водный раствор нитрата аммония. При этом за счет теплового эффекта реакции нейтрализации часть воды испаряется в виде сокового пара. Интенсивность испарения зависит от величины теплового эффекта и температуры процесса. Поэтому концентрация образующегося раствора определяется как концентрацией азотной кислоты, так и температурой.
С ростом концентрации азотной кислоты возрастает концентрация образующегося раствора нитрата аммония и увеличивается масса выделяющегося сокового пара.
Для испарения воды и концентрирования раствора нитрата аммония можно использовать как внешнее тепло, подводимое к системе, так и теплоту нейтрализации, выделяющуюся в самом процессе (рис. 5.1.).
 Qподв
Qподв


 H2O(пар) NH4NO3 + H2O NH4NO3
H2O(пар) NH4NO3 + H2O NH4NO3

DH реакц
Рисунок 5.1 - Использование тепла при упаривании раствора
Использование теплоты нейтрализации для упаривания раствора позволяет:
- снизить затрату внешнего тепла;
- обеспечить за счет отвода тепла из системы оптимальный температурный режим процесса нейтрализации и избежать опасных перегревов;
- исключить применение сложных охладительных устройств.
При использовании азотной кислоты концентрацией 60 – 65 % и температуре процесса около 70ºС оказывается возможным за счет использования теплоты нейтрализации выпарить основную массу воды, вводимой с азотной кислотой, и получить высококонцентрированный раствор и даже плав нитрата аммония.
В соответствии с принципом использования тепла все существующие варианты технологического процесса производства нитрата аммония делятся на две группы:
1 Без упаривания раствора. Концентрирование раствора осуществляется исключительно за счет теплоты нейтрализации азотной кислоты концентрацией 65%. При этом образуется 96% плав нитрата аммония:
Q = DH; Qподв = 0.
2 С упариванием раствора. Концентрирование раствора осуществляется как за счет частичного использования теплоты нейтрализации, так и за счет подводимого извне тепла:
Q = DH + Qподв.
При этом в зависимости от концентрации азотной кислоты последующее упаривание раствора нитрата аммония может производиться:
- при 58% кислоте в 1-й ступени;
- при 50% кислоте в 2-й ступени.
5.2.3 Технологические системы производства
Технологический процесс производства нитрата аммония состоит из следующих основных стадий: нейтрализации азотной кислоты газообразным аммиаком, выпаривание нитрата аммония, кристаллизации и гранулирования плава, охлаждения, классификации и опудривания готового продукта (рис.5.2.).
В настоящее время в связи с освоением производства 58 – 60% азотной кислоты основная масса нитрата аммония производится на установках АС-67, АС-72, АС-72М, мощностью 1360 и 1575 т/сутки с упариванием в одну ступень, а также на установках безупарочного типа (рис.5.3. и 5.4.)

Рисунок 5.2 - Принципиальная схема производства нитрата аммония
Газообразный аммиак из подогревателя 1, обогреваемого конденсатом сокового пара, нагретый до 120 - 160ºС, и азотная кислота из подогревателя 2, обогреваемого соковым паром, при температуре 80 - 90ºС поступают в аппарат ИТН (с использованием теплоты нейтрализации) 3. Для уменьшения потерь аммиака вместе с паром реакцию ведут в избытке кислоты. Раствор нитрата аммония из аппарата ИТН нейтрализуют в донейтрализаторе 4 аммиаком, куда одновременно добавляется кондиционирующая добавка нитрата магния и поступает на упаривание в выпарной аппарат 5. Из него образовавшийся плав нитрата аммония через гидрозатвор-донейтрализатор 6 и сборник плава 7 направляется в напорный бак 8 и из него с помощью виброакустических грануляторов 9 поступает в грануляционную башню 10. В нижнюю часть башни засасывается атмосферный воздух, и подается воздух из аппарата для охлаждения гранул «КС» 12. Образовавшиеся гранулы нитрата аммония из нижней части башни поступают на транспортер 11 и в аппарат кипящего слоя 12 для охлаждения гранул, в который через подогреватель 13 подается сухой воздух. Из аппарата 12 готовый продукт направляется на упаковку. Воздух из верхней части башни 10 поступает в скрубберы 14, орошаемые 20% раствором нитрата аммония, где отмывается от пыли нитрата аммония и выбрасывается в атмосферу. В этих же скрубберах очищаются от непрореагировавшего аммиака и азотной кислоты газы, выходящие из выпарного аппарата и нейтрализатора. Аппарат ИТН, грануляционная башня и комбинированный выпарной аппарат – основные аппараты в технологической схеме АС-72М.
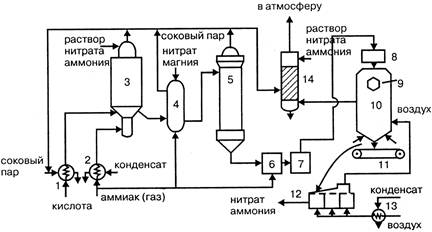
Рисунок 5.3 - Технологическая схема производства АС-72М:
1 – подогреватель аммиака; 2 – подогреватель кислоты; 3 – аппарат ИТН; 4 – донейтрализатор; 5 – выпарной аппарат; 6 – гидрозатвор-донейтрализатор; 7 – сборник плава; 8 – напорный бак; 9 – виброакустический гранулятор; 10 – грануляционная башня; 11 – транспортер; 12 – охладитель гранул «КС»; 13 – подогреватель воздуха; 14 – промывной скруббер
Аппарат ИТНимеет общую высоту 10 м и состоит из двух частей: нижней реакционной и верхней сепарационной. В реакционной части находится перфорированный стакан в который подают азотную кислоту и аммиак. При этом за счет хорошей теплоотдачи реакционной массы стенкам стакана, реакция нейтрализации протекает при температуре, более низкой, чем температура кипения кислоты. Образующийся раствор нитрата аммония закипает, и из него испаряется вода. За счет подъемной силы пара парожидкостная эмульсия выбрасывается из верхней части стакана и проходит через кольцевой зазор между корпусом и стаканом, продолжая упариваться. Затем она поступает в верхнюю сепарационную часть, где раствор, проходя ряд тарелок, отмывается от аммиака раствором нитрата аммония и конденсатом сокового пара. Время пребывания реагентов в реакционной зоне не превышает одной секунды, благодаря чему не происходит термического разложения кислоты и нитрата аммония. За счет использования теплоты нейтрализации в аппарате испаряется большая часть воды и образуется 90% раствор нитрата аммония.
Комбинированный выпарной аппарат высотой 16 м состоит из двух частей. В нижней кожухотрубной части диаметром 3м происходит упаривание раствора, проходящего через трубки, обогреваемые сначала перегретым паром, нагретым до 180ºС воздухом. Верхняя часть аппарата служит для очистки выходящей из аппарата паровоздушной смеси и частичного упаривания поступающего в аппарат раствора нитрата аммония. Из выпарного аппарата выходит плав нитрата аммония концентрацией 99,7% с температурой около 180ºС.
Грануляционная башня имеет прямоугольное сечение 11х8 м2 и высоту около 65 м. Через отверстие в нижней части в башню поступает наружный воздух и воздух из охладителя гранул. Поступающий в верхнюю часть башни плав нитрата аммония диспергируется с помощью трех виброакустических грануляторов, в которых струя плава превращается в капли. При падении капель с высоты около 50 м они затвердевают и превращаются в гранулы. Кристаллизация плава с влажностью 0,2% начинается при 167ºС и заканчивается при 140 ºС. Объем воздуха, подаваемого в башне, составляет в зависимости от времени года 300 – 500 м3/час.
В установках АС – 72М применяется магнезиальная добавка против слеживаемости продукта (нитрат магния). Поэтому операции обработки гранул ПАВ, предусмотренной в схемах АС – 67 и АС – 72, не требуется.
Принципиальными отличиями технологической схемы производства нитрата аммония безупарочным методом (рис. 5.4.) являются: использование более концентрированной азотной кислоты; проведение процесса нейтрализации при повышенном (0,4МПа) давлении; быстрый контакт нагретых компонентов.
В этих условиях на стадии нейтрализации образуется парожидкостная эмульсия, после разделения которой получают плав концентрацией 98,5%, что позволяет исключить отдельную стадию упаривания раствора.
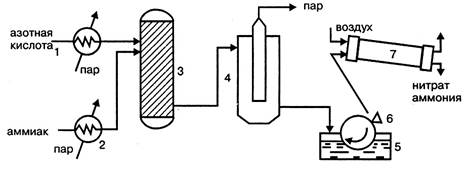
Рисунок 5.4 - Технологическая схема безупарочного метода:
1 – подогреватель азотной кислоты; 2 – подогреватель аммиака; 3 – реактор (нейтрализатор); 4 – сепаратор эмульсии; 5 – барабанный кристаллизатор; 6 – нож; 7 – барабанная сушка.
Нагретые в нагревателях 1 и 2, обогреваемые паром, выходящим из сепаратора, эмульсии 4, азотная кислота и аммиак поступают в нейтрализатор 3, где в результате реакции образуется эмульсия из водного раствора нитрата аммония и водяного пара. Эмульсия разделяется в сепараторе 4 и плав нитрата аммония подается в барабанный кристаллизатор 5, в котором нитрат аммония кристаллизируется на поверхности металлического барабана, охлаждаемого изнутри водой.
Образовавшийся на поверхности барабана слой твердого нитрата аммония толщиной около 1 мм срезается ножом 6 и в виде чешуек поступает для просушивания в барабанную сушилку 7. Подобный продукт в виде чешуек используется для технических целей.